Периодическая система - упорядоченное множество химических элементов, их естественная классификация, которая является графическим (табличным) выражением периодического закона химических элементов. Структура её, во многом сходная с современной, разработана Д. И. Менделеевым на основе периодического закона в 1869–1871 гг.
Прообразом периодической системы был «Опыт системы элементов, основанной на их атомном весе и химическом сходстве», составленный Д. И. Менделеевым 1 марта 1869 г. На протяжении двух с половиной лет ученый непрерывно совершенствовал «Опыт системы», ввел представление о группах, рядах и периодах элементов. В результате структура периодической системы приобрела во многом современные очертания.
Важным для её эволюции стало понятие о месте элемента в системе, определяемом номерами группы и периода. Опираясь на это понятие, Менделеев пришел к выводу, что необходимо изменить атомные массы некоторых элементов: урана, индия, церия и его спутников. Это было первое практическое применение периодической системы. Менделеев также впервые предсказал существование и свойства нескольких неизвестных элементов. Ученый подробно описал важнейшие свойства экаалюминия (будущего галлия), экабора (скандия) и экасилиция (германия). Кроме того, он предсказал существование аналогов марганца (будущих технеция и рения), теллура (полония), иода (астата), цезия (франция), бария (радия), тантала (протактиния). Прогнозы ученого в отношении данных элементов носили общий характер, поскольку эти элементы располагались в малоизученных областях периодической системы.
Первые варианты периодической системы во многом представляли лишь эмпирическое обобщение. Ведь был неясен физический смысл периодического закона, отсутствовало объяснение причин периодического изменения свойств элементов в зависимости от возрастания атомных масс. В связи с этим оставались нерешенными многие проблемы. Есть ли границы периодической системы? Можно ли определить точное количество существующих элементов? Оставалась неясной структура шестого периода - каково точное количество редкоземельных элементов? Было неизвестно, существуют ли еще элементы между водородом и литием, какова структура первого периода. Поэтому вплоть до физического обоснования периодического закона и разработки теории периодической системы перед ней не раз возникали серьезные трудности. Неожиданным было открытие в 1894–1898 гг. пяти инертных газов, которым, казалось, не находилось места в периодической системе. Эта трудность была устранена благодаря идее включить в структуру периодической системы самостоятельную нулевую группу. Массовое открытие радиоэлементов на стыке XIX и XX вв. (к 1910 г. их число составило около 40) привело к резкому противоречию между необходимостью их размещения в периодической системе и её сложившейся структурой. Для них было только 7 вакантных мест в шестом и седьмом периодах. Эта проблема была решена в результате установления правил сдвига и открытия изотопов.
Одна из главных причин невозможности объяснить физический смысл периодического закона и структуру периодической системы состояла в том, что было неизвестно, как устроен атом (см. Атом). Важнейшей вехой на пути развития периодической системы явилось создание атомной модели Э. Резерфордом (1911). На её основе голландский ученый А. Ван ден Брук (1913) высказал предположение, что порядковый номер элемента в периодической системе численно равен заряду ядра его атома (Z). Это экспериментально подтвердил английский ученый Г. Мозли (1913). Периодический закон получил физическое обоснование: периодичность изменения свойств элементов стала рассматриваться в зависимости от Z - заряда ядра атома элемента, а не от атомной массы (см. Периодический закон химических элементов).
В результате структура периодической системы значительно упрочилась. Была определена нижняя граница системы. Это водород - элемент с минимальным Z = 1. Стало возможным точно оценить количество элементов между водородом и ураном. Были определены «пробелы» в периодической системе, соответствующие неизвестным элементам с Z = 43, 61, 72, 75, 85, 87. Однако оставались неясными вопросы о точном количестве редкоземельных элементов и, что особенно важно, не были вскрыты причины периодичности изменения свойств элементов в зависимости от Z.
Опираясь на сложившуюся структуру периодической системы и результаты изучения атомных спектров, датский ученый Н. Бор в 1918–1921 гг. развил представления о последовательности построения электронных оболочек и подоболочек в атомах. Ученый пришел к выводу, что сходные типы электронных конфигураций внешних оболочек атомов периодически повторяются. Таким образом, было показано, что периодичность изменения свойств химических элементов объясняется существованием периодичности в построении электронных оболочек и подоболочек атомов.
Периодическая система охватывает более 100 элементов. Из них все трансурановые элементы (Z = 93–110), а также элементы с Z = 43 (технеций), 61 (прометий), 85 (астат), 87 (франций) получены искусственно. За всю историю существования периодической системы было предложено очень большое количество (>500) вариантов её графического изображения, преимущественно в виде таблиц, а также в виде различных геометрических фигур (пространственных и плоскостных), аналитических кривых (спиралей и пр.) и т. д. Наибольшее распространение получили короткая, полудлинная, длинная и лестничная формы таблиц. В настоящее время предпочтение отдается короткой форме.
Фундаментальным принципом построения периодической системы является её подразделение на группы и периоды. Менделеевское понятие рядов элементов ныне не употребляется, поскольку лишено физического смысла. Группы, в свою очередь, подразделяются на главную (а) и побочную (Ь) подгруппы. В каждой подгруппе содержатся элементы - химические аналоги. Элементы a‑ и b‑подгрупп в большинстве групп также обнаруживают между собой определенное сходство, главным образом в высших степенях окисления, которые, как правило, равны номеру группы. Периодом называется совокупность элементов, которая начинается щелочным металлом и заканчивается инертным газом (особый случай - первый период). Каждый период содержит строго определенное количество элементов. Периодическая система состоит из восьми групп и семи периодов, причем седьмой период пока не завершен.
Особенность первого периода заключается в том, что он содержит всего 2 газообразных в свободном виде элемента: водород и гелий. Место водорода в системе неоднозначно. Поскольку он проявляет свойства, общие со щелочными металлами и с галогенами, то его помещают либо в 1a‑, либо в Vlla‑подгруппу, либо в обе одновременно, заключая в одной из подгрупп символ в скобки. Гелий - первый представитель VIIIa‑подгруппы. Долгое время гелий и все инертные газы выделяли в самостоятельную нулевую группу. Это положение потребовало пересмотра после синтеза химических соединений криптона, ксенона и радона. В результате инертные газы и элементы бывшей VIII группы (железо, кобальт, никель и платиновые металлы) были объединены в рамках одной группы.
Второй период содержит 8 элементов. Он начинается щелочным металлом литием, единственная степень окисления которого +1. Далее следует бериллий (металл, степень окисления +2). Бор проявляет уже слабо выраженный металлический характер и является неметаллом (степень окисления +3). Следующий за бором углерод - типичный неметалл, который проявляет степени окисления как +4, так и −4. Азот, кислород, фтор и неон - все неметаллы, причем у азота высшая степень окисления +5 соответствует номеру группы. Кислород и фтор относятся к самым активным неметаллам. Инертный газ неон завершает период.
Третий период (натрий - аргон) также содержит 8 элементов. Характер изменения их свойств во многом аналогичен тому, который наблюдался для элементов второго периода. Но здесь есть и своя специфика. Так, магний в отличие от бериллия более металличен, так же как и алюминий по сравнению с бором. Кремний, фосфор, сера, хлор, аргон - все это типичные неметаллы. И все они, кроме аргона, проявляют высшие степени окисления, равные номеру группы.
Как видим, в обоих периодах по мере увеличения Z наблюдается отчетливое ослабление металлических и усиление неметаллических свойств элементов. Д. И. Менделеев называл элементы второго и третьего периодов (по его словам, малых) типическими. Элементы малых периодов принадлежат к числу самых распространенных в природе. Углерод, азот и кислород (наряду с водородом) - органогены, т. е. основные элементы органической материи.
Все элементы первого - третьего периодов размещаются в a‑подгруппах.
Четвертый период (калий - криптон) содержит 18 элементов. По Менделееву, это первый большой период. После щелочного металла калия и щелочноземельного металла кальция следует ряд элементов, состоящий из 10 так называемых переходных металлов (скандий - цинк). Все они входят в b‑подгруппы. Большинство переходных металлов проявляют высшие степени окисления, равные номеру группы, кроме железа, кобальта и никеля. Элементы, начиная с галлия и кончая криптоном, принадлежат к а-подгруппам. Для криптона известен ряд химических соединений.
Пятый период (рубидий - ксенон) по своему построению аналогичен четвертому. В нем также содержится вставка из 10 переходных металлов (иттрий - кадмий). У элементов этого периода есть свои особенности. В триаде рутений - родий - палладий для рутения известны соединения, где он проявляет степень окисления +8. Все элементы a‑подгрупп проявляют высшие степени окисления, равные номеру группы. Особенности изменения свойств у элементов четвертого и пятого периодов по мере роста Z имеют по сравнению со вторым и третьим периодами более сложный характер.
Шестой период (цезий - радон) включает 32 элемента. В этом периоде кроме 10 переходных металлов (лантан, гафний - ртуть) содержится еще и совокупность из 14 лантаноидов - от церия до лютеция. Элементы от церия до лютеция химически очень похожи, и на этом основании их давно включают в семейство редкоземельных элементов. В короткой форме периодической системы ряд лантаноидов включают в клетку лантана и расшифровку этого ряда дают внизу таблицы (см. Лантаноиды).
В чем состоит специфика элементов шестого периода? В триаде осмий - иридий - платина для осмия известна степень окисления +8. Астат имеет достаточно выраженный металлический характер. Радон обладает наибольшей реакционной способностью из всех инертных газов. К сожалению, из‑за того, что он сильно радиоактивен, его химия мало изучена (см. Радиоактивные элементы).
Седьмой период начинается с франция. Подобно шестому, он также должен содержать 32 элемента, но из них пока известны 24. Франций и радий соответственно являются элементами Ia‑ и IIa‑подгрупп, актиний принадлежит к IIIb‑подгруппе. Далее следует семейство актиноидов, которое включает элементы от тория до лоуренсия и размещается аналогично лантаноидам. Расшифровка этого ряда элементов также дается внизу таблицы.
Теперь посмотрим, как изменяются свойства химических элементов в подгруппах периодической системы. Основная закономерность этого изменения заключается в усилении металлического характера элементов по мере роста Z. Особенно отчетливо эта закономерность проявляется в IIIa–VIIa‑подгруппах. Для металлов Ia–IIIa‑подгрупп наблюдается рост химической активности. У элементов IVa–VIIa‑подгрупп по мере увеличения Z наблюдается ослабление химической активности элементов. У элементов b‑подгрупп характер изменения химической активности более сложен.
Теория периодической системы была разработана Н. Бором и другими учеными в 20‑х гг. XX в. и основана на реальной схеме формирования электронных конфигураций атомов (см. Атом). Согласно этой теории, по мере роста Z заполнение электронных оболочек и подоболочек в атомах элементов, входящих в периоды периодической системы, происходит в следующей последовательности:
| Номера периодов | ||||||
|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 1s | 2s2p | 3s3p | 4s3d4p | 5s4d5p | 6s4f5d6p | 7s5f6d7p |
На основании теории периодической системы можно дать следующее определение периода: период есть совокупность элементов, начинающаяся элементом со значением n, равным номеру периода, и l = 0 (s‑элементы) и заканчивающаяся элементом с тем же значением n и l = 1 (p‑элементы) (см. Атом). Исключение составляет первый период, содержащий только 1s‑элементы. Из теории периодической системы следуют числа элементов в периодах: 2, 8, 8, 18, 18, 32…
В таблице символы элементов каждого типа (s‑, p‑, d‑ и f‑элементы) изображены на определенном цветовом фоне: s‑элементы - на красном, p‑элементы - на оранжевом, d‑элементы - на синем, f‑элементы - на зеленом. В каждой клетке приведены порядковые номера и атомные массы элементов, а также электронные конфигурации внешних электронных оболочек.
Из теории периодической системы следует, что к a‑подгруппам принадлежат элементы с n, равным номеру периода, и l = 0 и 1. К b‑подгруппам относятся те элементы, в атомах которых происходит достройка оболочек, ранее остававшихся незавершенными. Именно поэтому первый, второй и третий периоды не содержат элементов b‑подгрупп.
Структура периодической системы элементов тесно связана со строением атомов химических элементов. По мере роста Z периодически повторяются сходные типы конфигурации внешних электронных оболочек. А именно они определяют основные особенности химического поведения элементов. Эти особенности по‑разному проявляются для элементов a‑подгрупп (s‑ и р‑элементы), для элементов b‑подгрупп (переходные d‑элементы) и элементов f‑семейств - лантаноидов и актиноидов. Особый случай представляют элементы первого периода - водород и гелий. Для водорода характерна высокая химическая активность, потому что его единственный 1s‑электрон легко отщепляется. В то же время конфигурация гелия (1s 2) весьма устойчива, что обусловливает его химическую бездеятельность.
У элементов а-подгрупп происходит заполнение внешних электронных оболочек атомов (с n, равным номеру периода), поэтому свойства этих элементов заметно изменяются по мере роста Z. Так, во втором периоде литий (конфигурация 2s) - активный металл, легко теряющий единственный валентный электрон; бериллий (2s 2) - также металл, но менее активный вследствие того, что его внешние электроны более прочно связаны с ядром. Далее, бор (2s 2 p) имеет слабо выраженный металлический характер, а все последующие элементы второго периода, у которых происходит построение 2p‑подоболочки, являются уже неметаллами. Восьмиэлектронная конфигурация внешней электронной оболочки неона (2s 2 p 6) - инертного газа - очень прочна.
Химические свойства элементов второго периода объясняются стремлением их атомов приобрести электронную конфигурацию ближайшего инертного газа (конфигурацию гелия - для элементов от лития до углерода или конфигурацию неона - для элементов от углерода до фтора). Вот почему, например, кислород не может проявлять высшей степени окисления, равной номеру группы: ведь ему легче достичь конфигурации неона путем приобретения дополнительных электронов. Такой же характер изменения свойств проявляется у элементов третьего периода и у s‑ и p‑элементов всех последующих периодов. В то же время ослабление прочности связи внешних электронов с ядром в a‑подгруппах по мере роста Z проявляется в свойствах соответствующих элементов. Так, для s‑элементов отмечается заметный рост химической активности по мере роста Z, а для p‑элементов - нарастание металлических свойств.
В атомах переходных d‑элементов достраиваются не завершенные ранее оболочки со значением главного квантового числа n, на единицу меньшим номера периода. За отдельными исключениями, конфигурация внешних электронных оболочек атомов переходных элементов - ns 2 . Поэтому все d‑элементы являются металлами, и именно поэтому изменения свойств d‑элементов по мере роста Z не так резки, как это наблюдается у s‑ и p‑элементов. В высших степенях окисления d‑элементы проявляют определенное сходство с p‑элементами соответствующих групп периодической системы.
Особенности свойств элементов триад (VIIIb‑подгруппа) объясняются тем, что b‑подоболочки близки к завершению. Вот почему железо, кобальт, никель и платиновые металлы, как правило, не склонны давать соединения высших степеней окисления. Исключение составляют лишь рутений и осмий, дающие оксиды RuO 4 и OsO 4 . У элементов Ib‑ и IIb‑подгрупп d‑подоболочка фактически оказывается завершенной. Поэтому они проявляют степени окисления, равные номеру группы.
В атомах лантаноидов и актиноидов (все они металлы) происходит достройка ранее не завершенных электронных оболочек со значением главного квантового числа n на две единицы меньше номера периода. В атомах этих элементов конфигурация внешней электронной оболочки (ns 2) сохраняется неизменной, а заполняется третья снаружи N‑оболочка 4f‑электронами. Вот почему лантаноиды так сходны.
У актиноидов дело обстоит сложнее. В атомах элементов с Z = 90–95 электроны 6d и 5f могут принимать участие в химических взаимодействиях. Поэтому актиноиды имеют гораздо больше степеней окисления. Например, для нептуния, плутония и америция известны соединения, где эти элементы выступают в семивалентном состоянии. Только у элементов, начиная с кюрия (Z = 96), становится устойчивым трехвалентное состояние, но и здесь есть свои особенности. Таким образом, свойства актиноидов значительно отличаются от свойств лантаноидов, и оба семейства поэтому нельзя считать подобными.
Семейство актиноидов заканчивается элементом с Z = 103 (лоуренсий). Оценка химических свойств курчатовия (Z = 104) и нильсбория (Z = 105) показывает, что эти элементы должны быть аналогами соответственно гафния и тантала. Поэтому ученые полагают, что после семейства актиноидов в атомах начинается систематическое заполнение 6d‑подоболочки. Оценка химической природы элементов с Z = 106–110 экспериментально не проводилась.
Конечное число элементов, которое охватывает периодическая система, неизвестно. Проблема её верхней границы - это, пожалуй, основная загадка периодической системы. Наиболее тяжелый элемент, который удалось обнаружить в природе,- это плутоний (Z = 94). Достигнутый предел искусственного ядерного синтеза - элемент с порядковым номером 110. Остается открытым вопрос: удастся ли получить элементы с большими порядковыми номерами, какие и сколько? На него нельзя пока ответить сколь‑либо определенно.
С помощью сложнейших расчетов, выполненных на электронных вычислительных машинах, ученые попытались определить строение атомов и оценить важнейшие свойства «сверхэлементов», вплоть до огромных порядковых номеров (Z = 172 и даже Z = 184). Полученные результаты оказались весьма неожиданными. Например, в атоме элемента с Z = 121 предполагается появление 8p‑электрона; это после того, как в атомах с Z = 119 и 120 завершилось формирование 8s‑подоболочки. А ведь появление p‑электронов вслед за s‑электронами наблюдается только в атомах элементов второго и третьего периодов. Расчеты показывают также, что у элементов гипотетического восьмого периода заполнение электронных оболочек и под-оболочек атомов происходит в очень сложной и своеобразной последовательности. Поэтому оценить свойства соответствующих элементов - проблема весьма сложная. Казалось бы, восьмой период должен содержать 50 элементов (Z = 119–168), но, согласно расчетам, он должен завершаться у элемента с Z = 164, т. е. на 4 порядковых номера раньше. А «экзотический» девятый период, оказывается, должен состоять из 8 элементов. Вот его «электронная» запись: 9s 2 8p 4 9p 2 . Иными словами, он содержал бы всего 8 элементов, как второй и третий периоды.
Трудно сказать, насколько соответствовали бы истине расчеты, проделанные с помощью компьютера. Однако если бы они были подтверждены, то пришлось бы серьезно пересмотреть закономерности, лежащие в основе периодической системы элементов и её структуры.
Периодическая система сыграла и продолжает играть огромную роль в развитии различных областей естествознания. Она явилась важнейшим достижением атомно-молекулярного учения, способствовала появлению современного понятия «химический элемент» и уточнению понятий о простых веществах и соединениях.
Закономерности, вскрытые периодической системой, оказали существенное влияние на разработку теории строения атомов, открытие изотопов, появление представлений о ядерной периодичности. С периодической системой связана строго научная постановка проблемы прогнозирования в химии. Это проявилось в предсказании существования и свойств неизвестных элементов и новых особенностей химического поведения элементов уже открытых. Ныне периодическая система представляет фундамент химии, в первую очередь неорганической, существенно помогая решению задачи химического синтеза веществ с заранее заданными свойствами, разработке новых полупроводниковых материалов, подбору специфических катализаторов для различных химических процессов и т. д. И наконец, периодическая система лежит в основе преподавания химии.
На этом уроке вы узнаете о Периодическом законе Менделеева, который описывает изменение свойств простых тел, а также формы и свойства соединений элементов в зависимости от величины их атомных масс. Рассмотрите, как по положению в Периодической системе можно описать химический элемент.
Тема: Периодический закон и Периодическая система химических элементов Д. И. Менделеева
Урок: Описание элемента по положению в Периодической системе элементов Д. И. Менделеева
В 1869 году Д.И.Менделеев на основе данных накопленных о химических элементах сформулировал свой периодический закон. Тогда он звучал так: « Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных масс элементов». Очень долго физический смысл закона Д.И.Менделеева был непонятен. Всё встало на свои места после открытия в XX веке строения атома.
Современная формулировка периодического закона: « Свойства простых веществ, также формы и свойства соединений элементов находятся в периодической зависимости от величины заряда ядра атома».
Заряд ядра атома равен числу протонов в ядре. Число протонов уравновешивается числом электронов в атоме. Таким образом, атом электронейтрален.
Заряд ядра атома в Периодической таблице - это порядковый номер элемента.
Номер периода показывает число энергетических уровней, на которых вращаются электроны.
Номер группы показывает число валентных электронов. Для элементов главных подгрупп число валентных электронов равно числу электронов на внешнем энергетическом уровне. Именно валентные электроны отвечают за образование химических связей элемента.
Химические элементы 8 группы - инертные газы имеют на внешней электронной оболочке 8 электронов. Такая электронная оболочка энергетически выгодна. Все атомы стремятся заполнить свою внешнюю электронную оболочку до 8 электронов.
Какие же характеристики атома меняются в Периодической системе периодически?
Повторяется строение внешнего электронного уровня.
Периодически меняется радиус атома. В группе радиус увеличивается с увеличением номера периода, так как увеличивается число энергетических уровней. В периоде слева направо будет происходить рост атомного ядра, но притяжение к ядру будет больше и поэтому радиус атома уменьшается .
Каждый атом стремится завершить последний энергетический уровень У элементов 1 группы на последнем слое 1 электрон. Поэтому им легче его отдать. А элементам 7 группы легче притянуть 1 недостающий до октета электрон. В группе способность отдавать электроны будет увеличиваться сверху вниз, так ка увеличивается радиус атома и притяжение к ядру меньше. В периоде слева направо способность отдавать электроны уменьшается, потому что уменьшается радиус атома.
Чем легче элемент отдает электроны с внешнего уровня, тем большими металлическими свойствами он обладает, а его оксиды и гидроксиды обладают большими основными свойствами. Значит, металлические свойства в группах увеличиваются сверху вниз, а в периодах справа налево. С неметаллическими свойствами все наоборот.

Рис. 1. Положение магния в таблице
В группе магний соседствует с бериллием и кальцием. Рис.1. Магний стоит ниже, чем бериллий, но выше кальция в группе. У магния больше металлические свойства, чем у бериллия, но меньше чем у кальция. Основные свойства его оксидов и гидроксидов изменяются также. В периоде натрий стоит левее, а алюминий правее магния. Натрий будет проявлять больше металлические свойства, чем магний, а магний больше, чес алюминий. Таким образом, можно сравнить любой элемент с соседями его по группе и периоду.
Кислотные и неметаллические свойства изменяются противоположно основным и металлическим свойствам.
Характеристика хлора по его положению в периодической системе Д.И.Менделеева.

Рис. 4. Положение хлора в таблице
. Значение порядкового номера 17 показывает число протонов17 и электронов17 в атоме. Рис.4. Атомная масса 35 поможет вычислить число нейтронов (35-17 = 18). Хлор находится в третьем периоде, значит число энергетических уровней в атоме равно 3. Стоит в 7 -А группе, относится к р- элементам. Это неметалл. Сравниваем хлор с его соседями по группе и по периоду. Неметаллические свойства хлора больше чем у серы, но меньше, чем у аргона. Хлор об-ла-да-ет мень-ши-ми неме-тал-ли-че-ски-ми свой-ства-ми, чем фтор и боль-ши-ми чем бром. Распределим электроны по энергетическим уровням и напишем электронную формулу. Общее распределение электронов будет иметь такой вид. См.Рис. 5
|
|
Рис. 5. Распределение электронов атома хлора по энергетическим уровням
Определяем высшую и низшую степень окисления хлора. Высшая степень окисления равна +7, так как он может отдать с последнего электронного слоя 7 электронов. Низшая степень окисления равна -1, потому что хлору до завершения необходим 1 электрон. Формула высшего оксида Cl 2 O 7 (кислотный оксид), водородного соединения HCl.
В процессе отдачи или присоединения электронов атом приобретает условный заряд
. Этот условный заряд называется .
- Простые
вещества обладают степенью окисления равной нулю.
Элементы могут проявлять максимальную степень окисления и минимальную . Максимальную степень окисления элемент проявляет тогда, когда отдает все свои валентные электроны с внешнего электронного уровня. Если число валентных электронов равно номеру группы, то и максимальная степень окисления равна номеру группы.

Рис. 2. Положение мышьяка в таблице
Минимальную степень окисления элемент будет проявлять тогда, когда он примет все возможные электроны для завершения электронного слоя.
Рассмотрим на примере элемента №33 значения степеней окисления.
Это мышьяк As.Он находится в пятой главной подгруппе.Рис.2. На последнем электронном уровне у него пять электронов. Значит, отдавая их, он будет иметь степень окисления +5. До завершения электронного слоя атому As не хватает 3 электрона. Притягивая их, он будет иметь степень окисления -3.
Положение элементов металлов и неметаллов в Периодической системе Д.И. Менделеева.

Рис. 3. Положение металлов и неметаллов в таблице
В побочных подгруппах находятся все металлы . Если мысленно провести диагональ от бора к астату , то выше этой диагонали в главных подгруппах будут все неметаллы , а ниже этой диагонали - все металлы . Рис.3.
1. №№ 1-4 (с.125) Рудзитис Г.Е. Неорганическая и органическая химия. 8 класс: учебник для общеобразовательных учреждений: базовый уровень/ Г. Е. Рудзитис, Ф.Г. Фельдман. М.: Просвещение. 2011 г.176с.:ил.
2. Какие характеристики атома изменяются периодичности?
3. Дайте характеристику химического элемента кислорода по его положению в Периодической системе Д.И.Менделеева.
Эфир в таблице МенделееваМировой эфир есть субстанция ВСЯКОГО химического элемента и значит - ВСЯКОГО вещества, есть Абсолютная истинная материя как Всемирная элементообразующая Сущность. Мировой эфир - это исток и венец всей подлинной Таблицы Менделеева, её начало и конец, - альфа и омега Периодической системы элементов Дмитрия Ивановича Менделеева.
В античной философии эфир (aithér-греч) наряду с землей, водой, воздухом и огнем - один из пяти элементов бытия (по Аристотелю) - пятая сущность (quinta essentia -лат.), понимаемая как тончайшая всепроникающая материя. В конце XIX века в ученых кругах получила широкое хождение гипотеза о мировом эфире (МЭ), заполняющем все мировое пространство. Он понимался как невесомая и упругая жидкость, которая пронизывает все тела. Существованием эфира пытались объяснить многие физические явления и свойства.
Предисловие.
У Менделеева было два фундаментальных научных открытия:
1 - Открытие Периодического закона в субстанции химии,
2 - Открытие взаимосвязи субстанции химии и субстанции Эфира, а именно: частицы Эфира формирует молекулы, ядра, электроны и т.д., но в химических реакциях не участвуют.
Эфир - частицы вещества размером ~ 10-100 метра (фактически - «первокирпичики» материи).
Факты. В подлинной таблице Менделеева был Эфир. Ячейка для Эфира располагалась в нулевой группе с инертными газами и в нулевом ряду как главный системообразующий фактор для построения Системы химических элементов. После смерти Менделеева таблицу исказили, убрав из неё Эфир и отменив нулевую группу, тем самым, скрыв фундаментальное открытие концептуального значения.
В современных таблицах Эфира: 1 - не видно, 2 - и не угадывается (из-за отсутствия нулевой группы).
Такой целенаправленный подлог сдерживает развитие прогресса цивилизации.
Техногенные катастрофы (напр. Чернобыль и Фукусима) были бы исключены, если бы в развитие подлинной таблицы Менделеева своевременно были вложены адекватные ресурсы. Сокрытие концептуальных знаний идёт на глобальном уровне для «опускания» цивилизации.
Результат. В школах и ВУЗах преподают обрезанную таблицу Менделеева.
Оценка ситуации. Таблица Менделеева без Эфира - то же самое, что человечество без детей - прожить можно, но развития и будущего не будет.
Резюме. Если враги человечества знания скрывают, то наша задача - эти знания раскрывать.
Вывод. В старой таблице Менделеева элементов меньше, а форсайта больше, чем в современной.
Заключение. Новый уровень возможен только при изменении информационного состояния общества.
Итог. Возврат к истинной таблице Менделеева - это уже вопрос не научный, а вопрос политический.
В чем же был основной политический смысл эйнштейновского учения? Он состоял в том, чтобы любыми путями перекрыть человечеству доступ к неисчерпаемым естественным источникам энергии, которые открывало изучение свойств мирового эфира . В случае успеха на этом пути, мировая финансовая олигархия теряла власть в этом мире, особенно в свете ретроспективы тех лет: Рокфеллеры сделали немыслимое состояние, превосходящее бюджет Соединенных Штатов, на нефтяных спекуляциях, и утрата той роли нефти, которую заняло «черное золото» в этом мире - роль крови мировой экономики - их не вдохновляла.
Не вдохновляло это и прочих олигархов - угольных и стальных королей. Так финансовый магнат Морган моментально прекратил финансирование экспериментов Николы Теслы, когда тот вплотную подошел к беспроводной передаче энергии и извлечению энергии «из ниоткуда» - из мирового эфира. После этого обладателю огромного количества воплощенных в практику технических решений не оказывал финансовой помощи никто - солидарность у финансовых воротил как у воров в законе и феноменальный нюх на то, откуда исходит опасность. Вот поэтому против человечества и была произведена диверсия под названием «Специальная Теория Относительности».
Один из первых ударов пришелся на таблицу Дмитрия Менделеева, в которой эфир стоял первым номером, именно размышления об эфире породили гениальное прозрение Менделеева - его периодическую таблицу элементов.

Глава из статьи: В.Г. Родионов. Место и роль мирового эфира в истинной таблице Д.И. Менделеева
6. Argumentum ad rem
То, что сейчас преподносят в школах и университетах под названием «Периодическая система химических элементов Д.И. Менделеева»,- откровенная ф а л ь ш и в к а.
Последний раз в неискажённом виде настоящая Таблица Менделеева увидела свет в 1906 году в Санкт-Петербурге (учебник «Основы химии», VIII издание). И только спустя 96 лет забвения подлинная Таблица Менделеева впервые восстаёт из пепла благодаря публикации диссертации в журнале ЖРФМ Русского Физического Общества.
После скоропостижной смерти Д. И. Менделеева и ухода из жизни его верных научных коллег по Русскому Физико-Химическому Обществу, впервые поднял руку на бессмертное творение Менделеева — сын друга и соратника Д. И. Менделеева по Обществу — Борис Николаевич Меншуткин. Конечно, Меншуткин действовал не в одиночку, — он лишь выполнял заказ. Ведь, новая парадигма релятивизма требовала отказа от идеи мирового эфира; и потому это требование было возведено в ранг догмы, а труд Д. И. Менделеева был фальсифицирован.
Главное искажение Таблицы — перенос «нулевой группы» Таблицы в её конец, вправо, и введение т.н. «периодов». Подчёркиваем, что такая (лишь на первый взгляд — безобидная) манипуляция логически объяснима только как сознательное устранение главного методологического звена в открытии Менделеева: периодическая система элементов в своём начале, истоке, т.е. в верхнем левом углу Таблицы, должна иметь нулевую группу и нулевой ряд, где располагается элемент «Х» (по Менделееву — «Ньютоний»),- т.е. мировой эфир.
Более того, являясь единственным системообразующим элементом всей Таблицы производных элементов, этот элемент «Х» есть аргумент всей Таблицы Менделеева. Перенос же нулевой группы Таблицы в её конец уничтожает саму идею этой первоосновы всей системы элементов по Менделееву.
Для подтверждения вышесказанного, предоставим слово самому Д. И. Менделееву.
«… Если же аналоги аргона вовсе не дают соединений, то очевидно, что нельзя включать ни одну из групп ранее известных элементов, и для них должно открыть особую группу нулевую … Это положение аргоновых аналогов в нулевой группе составляет строго логическое следствие понимания периодического закона, а потому (помещение в группе VIII явно не верно) принято не только мною, но и Браизнером, Пиччини и другими … Теперь же, когда стало не подлежать ни малейшему сомнению, что перед той I группой, в которой должно помещать водород, существует нулевая группа, представители которой имеют веса атомов меньше, чем у элементов I группы, мне кажется невозможным отрицать существование элементов более лёгких, чем водород.


Из них обратим внимание сперва на элемент первого ряда 1-й группы. Его означим через «y». Ему, очевидно, будут принадлежать коренные свойства аргоновых газов … «Короний», плотностью порядка 0,2 по отношению к водороду; и он не может быть ни коим образом мировым эфиром.
Этот элемент «у», однако, необходим для того, чтобы умственно подобраться к тому наиглавнейшему, а потому и наиболее быстро движущемуся элементу «х», который, по моему разумению, можно считать эфиром. Мне бы хотелось предварительно назвать его «Ньютонием» — в честь бессмертного Ньютона … Задачу тяготения и задачи всей энергетики (!!! — В.Родионов) нельзя представить реально решёнными без реального понимания эфира, как мировой среды, передающей энергию на расстояния. Реального же понимания эфира нельзя достичь, игнорируя его химизм и не считая его элементарным веществом; элементарные же вещества ныне немыслимы без подчинения их периодической законности»
(«Попытка химического понимания мирового эфира». 1905 г., стр. 27).

«Эти элементы, по величине их атомных весов, заняли точное место между галлоидами и щелочными металлами, как показал Рамзай в 1900 году. Из этих элементов необходимо образовать особую нулевую группу, которую прежде всех в 1900 году признал Еррере в Бельгии. Считаю здесь полезным присовокупить, что прямо судя по неспособности к соединениям элементов нулевой группы, аналогов аргона должно поставить раньше элементов 1 группы и по духу периодической системы ждать для них меньшего атомного веса, чем для щелочных металлов.
Это так и оказалось. А если так, то это обстоятельство, с одной стороны, служит подтверждением правильности периодических начал, а с другой стороны, ясно показывает отношение аналогов аргона к другим, ранее известным, элементам. Вследствие этого можно разбираемые начала прилагать ещё шире, чем ранее, и ждать элементов нулевого ряда с атомными весами гораздо меньшими, чем у водорода.
Таким образом, можно показать, что в первом ряду первым перед водородом существует элемент нулевой группы с атомным весом 0,4 (быть может, это короний Ионга), а в ряду нулевом, в нулевой группе — предельный элемент с ничтожно малым атомным весом, не способным к химическим взаимодействиям и обладающий вследствие того чрезвычайно быстрым собственным частичным (газовым) движением.
Эти свойства, быть может, должно приписать атомам всепроникающего (!!! — В.Родионов) мирового эфира. Мысль об этом указана мною в предисловии к этому изданию и в русской журнальной статье 1902 года …» («Основы химии». VIII изд., 1906 г., стр. 613 и след.)
Настоящая таблица Менделеева. Рыбников Юрий Степанович.
Запретная Физика. Теория Эфира
Полное видео лекции тут: Фальсификация таблицы Менделеева
Из комментариев:
Для химии современной периодической таблицы элементов достаточно.
Роль эфира может быть полезна в ядерных реакциях, но и это слишком не значительно.
Учёт влияния эфира наиболее близко в явлениях распада изотопов. Однако учёт этот чрезвычайно сложен и наличие закономерностей принимаются не всеми учёными.
Самое простое доказательство наличия эфира: Явление аннигиляции позитрон-электронной пары и возникновение этой пары из вакуума, а также невозможность поймать электрон в состоянии покоя. Так же электромагнитное поле и полная аналогия между фотонами в вакууме и звуковыми волнами - фононами в кристаллах.
Эфир - это дифференцированная материя, так сказать, атомы в разобранном состоянии или правильней сказать, элементарные частицы, из которых формируются будущие атомы. Поэтому ему нет места в таблице Менделеева, так как логика построения данной системы не предполагает включать в её состав не целостные структуры,которыми являются сами атомы. В противном случае, так можно и для кварков найти место, где-нибудь в минус первом периоде.
Сам эфир имеет более сложную многоуровневую структуру проявления в мировом бытии, нежели об этом знает современная наука. Как только она раскроет первые тайны этого неуловимого эфира, тогда и будут изобретены новые двигатели для всевозможных машин на абсолютно новых принципах.
Действительно,Тесла едва ли не единственный, кто был близок к разгадке тайны, так называемого эфира,но ему сознательно мешали осуществить свои замыслы. Вот так до сегодняшнего дня ещё не родился тот гений, который продолжит дело великого изобретателя и расскажет всем нам, что же на самом деле представляет из себя таинственный эфир и на какой пьедестал его можно будет поставить.
На самом деле, немецкий физик Иоганн Вольфганг Доберейнер заметил особенности группирования элементов еще в 1817 году. В те дни химики еще не полностью поняли природу атомов, описанную Джона Дальтона в 1808 году. В своей «новой системе химической философии» Дальтон объяснил химические реакции, предполагая, что каждое элементарное вещество состоит из атома определенного типа.
Дальтон предположил, что химические реакции производили новые вещества, когда атомы разъединяются или соединяются. Он полагал, что любой элемент состоит исключительно из одного вида атома, который отличается от других по весу. Атомы кислорода весили в восемь раз больше, чем атомы водорода. Дальтон считал, что атомы углерода в шесть раз тяжелее водорода. Когда элементы объединяются для создания новых веществ, количество реагирующих веществ может быть рассчитано с учетом этих атомных весов.
Дальтон ошибался насчет некоторых масс – кислород в действительности в 16 раз тяжелее водорода, а углерод в 12 раз тяжелее водорода. Но его теория сделала идею об атомах полезной, вдохновив революцию в химии. Точное измерение атомной массы стало основной проблемой химиков на последующие десятилетия.
Размышляя об этих весах, Доберейнер отметил, что определенные наборы из трех элементов (он назвал их триадами) показывают интересную связь. Бром, например, имел атомную массу где-то между массами хлора и йода, и все эти три элемента демонстрировали сходное химическое поведение. Литий, натрий и калий также были триадой.
Другие химики заметили связи между атомными массами и , но лишь в 1860-х годах атомные массы стали достаточно хорошо поняты и измерены, чтобы выработалось более глубокое понимание. Английский химик Джон Ньюландс заметил, что расположение известных элементов в порядке увеличения атомной массы приводило к повторению химических свойств каждого восьмого элемента. Эту модель он назвал «законом октав» в статье 1865 года. Но модель Ньюландса не очень хорошо держалась после первых двух октав, что заставило критиков предложить ему расставить элементы в алфавитном порядке. И как вскоре понял Менделеев, отношение свойств элементов и атомных масс были чуть более сложными.
Организация химических элементов
Менделеев родился в Тобольске, в Сибири, в 1834 году и был семнадцатым ребенком у своих родителей. Он жил яркой жизнью, преследуя разные интересы и путешествуя по дороге к выдающимся людям. Во время получения высшего образования в педагогическом институте в Санкт-Петербурге он чуть не умер от тяжелой болезни. После окончания он преподавал в средних школах (это нужно было, чтобы получать жалование в институте), попутно изучая математику и естественные науки для получения степени магистра.
Затем он работал преподавателем и лектором (и писал научные работы), пока не получил стипендию для расширенного тура исследований в лучших химических лабораториях Европы.
Вернувшись в Санкт-Петербург, он оказался без работы, поэтому написал превосходное руководство по в надежде выиграть крупный денежный приз. В 1862 году это принесло ему премию Демидова. Также он работал редактором, переводчиком и консультантом в различных химических сферах. В 1865 году он вернулся к исследованиям, получил доктора наук и стал профессором Петербургского университета.
Вскоре после этого Менделеев начал преподавать неорганическую химию. Готовясь освоить это новое (для него) поле, он остался неудовлетворен доступными учебниками. Поэтому решил написать собственный. Организация текста требовала организации элементов, поэтому вопрос их наилучшего расположения непрестанно был у него на уме.
К началу 1869 года Менделеев добился достаточного прогресса, чтобы понять, что некоторые группы подобных элементов демонстрировали регулярное увеличение атомных масс; другие элементы с примерно одинаковыми атомными массами имели схожие свойства. Оказалось, что упорядочение элементов по их атомному весу было ключом к их классификации.

Периодическая таблица Д. Менелеева.
По собственным словам Менделеева, он структурировал свое мышление, записав каждый из 63 известных тогда элементов на отдельной карточке. Затем, посредством своего рода игры в химический пасьянс, он нашел закономерность, которую искал. Располагая карточки в вертикальных столбцах с атомными массами от низкой к более высокой, он разместил элементы со схожими свойствами в каждом горизонтальном ряд. Периодическая таблица Менделеева родилась. Он набросал черновую версию 1 марта, отправил ее в печать и включил в свой учебник, который скоро должен был быть опубликован. Также он быстро подготовил работу для представления Российскому химическому обществу.
«Элементы, упорядоченные по размерам их атомных масс, показывают четкие периодические свойства», писал Менделеев в своей работе. «Все сравнения, которые я провел, привели меня к выводу, что размер атомной массы определяет природу элементов».
Тем временем, немецкий химик Лотар Мейер также работал над организацией элементов. Он подготовил таблицу, похожую на менделеевскую, возможно, даже раньше, чем Менделеев. Но Менделеев издал свою первым.
Тем не менее, гораздо более важным, чем победа над Мейером, было то, как Менделеев использовал свою таблицу, чтобы сделать о неоткрытых элементах. В подготовке свой таблицы Менделеев заметил, что некоторых карточек недоставало. Он должен был оставить пустые места, чтобы известные элементы могли выровняться правильно. Еще при его жизни три пустых места были заполнены ранее неизвестными элементами: галлий, скандий и германий.
Менделеев не только предсказал существование этих элементов, но также правильно описал их свойства в подробностях. Галлий, например, открытый в 1875 году, имел атомную массу 69,9 и плотность в шесть раз превышающую воды. Менделеев предсказал этот элемент (он назвал его экаалюминий), только по этой плотности и атомной массе 68. Его прогнозы для экакремния близко соответствовали германию (открытому в 1886 году) по атомной массе (72 предсказано, 72,3 фактически) и плотности. Он также верно предсказал плотность германиевых соединений с кислородом и хлором.
Таблица Менделеева стала пророческой. Казалось, что в конце этой игры этот пасьян из элементов раскроет . При этом сам Менделеев был мастером в использовании своей же таблицы.
Успешные предсказания Менделеева принесли ему легендарный статус мастера химического волшебства. Но сегодня историки спорят о том, закрепило ли открытие предсказанных элементов принятие его периодического закона. Принятие закона могло быть в большей степени связано с его способностью объяснять установленные химические связи. В любом случае, прогностическая точность Менделеева, безусловно, привлекла внимание к достоинствам его таблицы.
К 1890-м годам химики широко признали его закон как веху в химическом познании. В 1900-м году будущий нобелевский лауреат по химии Уильям Рамсей назвал это «величайшим обобщением, которое когда-либо проводилось в химии». И Менделеев сделал это, сам не понимая как.
Математическая карта
Во многих случаях в истории науки великие предсказания, основанные на новых уравнениях, оказывались верными. Каким-то образом математика раскрывает некоторые природные секреты, прежде чем экспериментаторы их обнаружат. Один из примеров - антиматерия, другой - расширение Вселенной. В случае Менделеева, предсказания новых элементов возникли без какой-либо творческой математики. Но на самом деле Менделеев открыл глубокую математическую карту природы, поскольку его таблица отражала значение , математических правил, управляющих атомной архитектурой.
В своей книге Менделеев отметил, что «внутренние различия материи, которую составляют атомы», могут быть ответственны за периодически повторяющиеся свойства элементов. Но он не придерживался этой линии мышления. По сути, многие годы он размышлял о том, насколько важна атомная теория для его таблицы.
Но другие смогли прочитать внутреннее послание таблицы. В 1888 году немецкий химик Йоханнес Вислицен объявил, что периодичность свойств элементов, упорядоченных по массе, указывает на то, что атомы состоят из регулярных групп более мелких частиц. Таким образом, в некотором смысле таблица Менделеева действительно предвидела (и предоставила доказательства) сложную внутреннюю структуру атомов, в то время как никто не имел ни малейшего представления о том, как на самом деле выглядел атом или имел ли он какую-нибудь внутреннюю структуру вовсе.
К моменту смерти Менделеева в 1907 году ученые знали, что атомы делятся на части: , плюс некоторый положительно заряженный компонент, делающий атомы электрически нейтральными. Ключом к тому, как эти части выстраиваются, стало открытие 1911 года, когда физик Эрнест Резерфорд, работающий в Манчестерском университете в Англии, обнаружил атомное ядро. Вскоре после этого Генри Мозли, работавший с Резерфордом, продемонстрировал, что количество положительного заряда в ядре (число протонов, которое он содержит, или его «атомное число») определяет правильный порядок элементов в периодической таблице.

Генри Мозли.
Атомная масса была тесно связана с атомным числом Мозли - достаточно тесно, чтобы упорядочение элементов по массе только в нескольких местах отличалось от упорядочения по числу. Менделеев настаивал на том, что эти массы были неправильными и нуждались в повторном измерении, и в некоторых случаях оказался прав. Осталось несколько расхождений, но атомное число Мозли прекрасно легло в таблицу.
Примерно в то же время датский физик Нильс Бор понял, что квантовая теория определяет расположение электронов, окружающих ядро, и что самые дальние электроны определяют химические свойства элемента.
Подобные расположения внешних электронов будут периодически повторяться, объясняя закономерности, которые первоначально выявила таблица Менделеева. Бор создал свою собственную версию таблицы в 1922 году, основываясь на экспериментальных измерениях энергий электронов (наряду с некоторыми подсказками из периодического закона).
Таблица Бора добавила элементы, открытые с 1869 года, но это был тот же периодической порядок, открытый Менделеевым. Не имея ни малейшего представления о , Менделеев создал таблицу, отражающую атомную архитектуру, которую диктовала квантовая физика.
Новая таблица Бора не стала ни первым, ни последним вариантом изначального дизайна Менделеева. Сотни версий периодической таблицы с тех пор были разработаны и опубликованы. Современная форма - в горизонтальном дизайне в отличие от первоначальной вертикальной версии Менделеева - стала широко популярной только после Второй мировой войны, во многом благодаря работе американского химика Гленна Сиборга.
Сиборг и его коллеги создали несколько новых элементов синтетически, с атомными числами после урана, последнего природного элемента в таблице. Сиборг увидел, что эти элементы, трансурановые (плюс три элемента, предшествовавшие урану), требовали новой строки в таблице, которую не предвидел Менделеев. Таблица Сиборга добавила строку для тех элементов под аналогичным рядом редкоземельных элементов, которым тоже не было места в таблице.
Вклад Сиборг в химию принес ему честь назвать собственный элемент - сиборгий с номером 106. Это один из нескольких элементов, названных в честь известных ученых. И в этом списке, конечно, есть элемент 101, открытый Сиборгом и его коллегами в 1955 году и названный менделевием - в честь химика, который прежде всех остальных заслужил место в периодической таблице.
Заходите на наш канал с новостями , если хотите больше подобных историй.
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА МЕНДЕЛЕЕВА
Построение периодической таблицы химических элементов Менделеева отвечает характерным периодам теории чисел и ортогональных базисов. Дополнение матриц Адамара матрицами четных и нечетных порядков создает структурный базис вложенных матричных элементов: матриц первого (Odin), второго (Euler), третьего (Mersenne), четвертого (Hadamard) и пятого (Fermat) порядков.
Несложно заметить, что порядкам 4k матриц Адамара соответствуют инертные элементы с атомной массой, кратной четырем: гелий 4, неон 20, аргон 40 (39.948) и т.п., но также и основы жизни и цифровой техники: углерод 12, кислород 16, кремний 28, германий 72.
Такое впечатление, что с матрицами Мерсенна порядков 4k –1, напротив, связано все активное, ядовитое, разрушительное и разъедающее. Но это также радиоактивные элементы – источники энергии, и свинец 207 (конечный продукт, ядовитые соли). Фтор, это, конечно, 19. Порядкам матриц Мерсенна отвечает последовательность радиоактивных элементов, называемая рядом актиния: уран 235, плутоний 239 (изотоп, который является более мощным источником атомной энергии, чем уран) и т.п. Это также щелочные металлы литий 7, натрий 23 и калий 39.

Галлий – атомный вес 68
Порядкам 4k –2 матриц Эйлера (сдвоенный Мерсенн) соответствует азот 14 (основа атмосферы). Поваренная соль образована двумя "мерсенноподобными" атомами натрия 23 и хлора 35, вместе это сочетание характерно, как раз, для матриц Эйлера. Более массивный хлор с весом 35.4 немногим не добирает до адамаровой размерности 36. Кристаллы поваренной соли: куб (! т.е. характер смирный, адамаров) и октаэдр (более вызывающий, это несомненный Эйлер).
В атомной физике переход железо 56 – никель 59, это рубеж между элементами, дающими энергию при синтезе более крупного ядра (водородная бомба) и распаде (урановая). Порядок 58 знаменит тем, что для него нет не только аналогов матриц Адамара в виде матриц Белевича с нулями на диагонали, для него нет и многих взвешенных матриц – ближайшая ортогональная W(58,53) имеет 5 нулей в каждом столбце и строке (глубокий разрыв).
В ряду, соответствующем матрицам Ферма и их замещениям порядков 4k +1, стоит волею судьбы фермий 257. Ничего не скажешь, точное попадание. Здесь же золото 197. Медь 64 (63.547) и серебро 108 (107.868), символы электроники, недотягивают, как видно, до золота и соответствуют более скромным матрицам Адамара. Медь, с ее недалеко ушедшим от 63 атомным весом, химически активна – ее зеленые окислы хорошо известны.
Кристаллы бора под сильным увеличением
С золотым сечением связан бор – атомная масса среди всех прочих элементов наиболее близка к 10 (точнее 10.8, близость атомного веса к нечетным числам тоже сказывается). Бор – достаточно сложный элемент. Бор играет запутанную роль в истории самой жизни. Строение каркаса в его структурах гораздо сложнее, чем в алмазе. Уникальный тип химической связи, которая позволяет бору поглощать любую примесь, очень плохо изучен, хотя за исследования, связанные с ним, большое количество ученых уже получили Нобелевские премии. Форма кристалла бора – икосаэдр, пять треугольников образуют вершину.
Загадка Платины. Пятый элемент, это, без сомнения, благородные металлы, такие, как золото. Надстройка над адамаровой размерностью 4k , на 1 большие.

Стабильный изотоп уран 238
Вспомним, все же, что числа Ферма встречаются редко (ближайшее – 257). Кристаллы самородного золота имеют форму, близкую к кубу, но и пентаграмма просверкивает. Его ближайший сосед, платина, благородный металл, отстоит от золота 197 по атомному весу меньше, чем на 4. Платина имеет атомный вес не 193, а несколько повышенный, 194 (порядок матриц Эйлера). Мелочь, но это переносит ее в стан несколько более агрессивных элементов. Стоит вспомнить, в связи, что при ее инертности (растворяется, разве, в царской водке), платину используют как активный катализатор химических процессов.
Губчатая платина при комнатной температуре воспламеняет водород. Характер у платины вовсе не мирный, смирнее себя ведет иридий 192 (смесь изотопов 191 и 193). Это, скорее, медь, но с весом и характером золота.
Между неоном 20 и натрием 23 нет элемента с атомным весом 22. Конечно, атомные веса – интегральная характеристика. Но среди изотопов, в свою очередь, тоже наблюдается любопытная корреляция свойств со свойствами чисел и соответствующих им матриц ортогональных базисов. В качестве ядерного топлива наибольшее применение имеет изотоп уран 235 (порядок матриц Мерсенна), в котором возможна самоподдерживающаяся цепная ядерная реакция. В природе этот элемент распространен стабильной форме уран 238 (порядок матриц Эйлера). Элемент с атомным весом 13 отсутствует. Что касается хаоса, то ограниченное количество устойчивых элементов таблицы Менделеева и сложность нахождения уровневых матриц высоких порядков ввиду замеченного у матриц тринадцатого порядка барьера коррелируют.
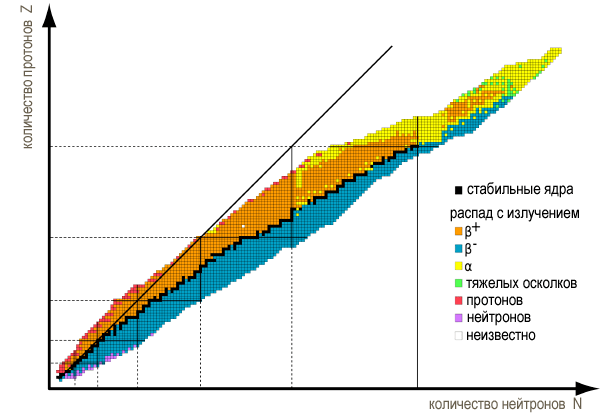
Изотопы химических элементов, островок стабильности











