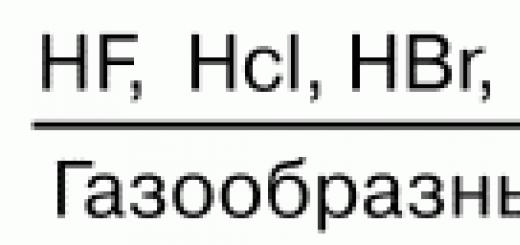Галогени- Елементи VII групи - фтор, хлор, бром, йод, астат (астат мало вивчений у зв'язку з його радіоактивністю). Галогени – яскраво виражені неметали. Лише йод у окремих випадках виявляє деякі властивості, схожі з металами.
У незбудженому стані атоми галогенів мають загальну електронну конфігурацію: ns2np5. Це означає, що галогени мають 7 валентних електронів, крім фтору.
Фізичні властивості галогенів: F2 - безбарвний газ, що важко зріджується; Cl2 – жовто-зелений, легко зріджуваний газ із різким задушливим запахом; Br2 – рідина червоно-бурого кольору; I2 – кристалічна речовина фіолетового кольору.

Водні розчини галогеноводородів утворюють кислоти. НF – фтороводородна (плавикова); НCl – хлороводнева (соляна); НBr - бромоводнева; НI – йодоводородна. Сили кислот згори донизу знижуються. Плавикова кислота є найслабшою серед галогеново-дородных кислот, а йодоводородная – найсильнішої. Це тим, що енергія зв'язку Нг зверху зменшується. У цьому напрямі зменшується і міцність молекули Н Р, що пов'язані з зростанням межядерного відстані. Розчинність малорозчинних солей у воді також зменшується:
Зліва направо розчинність галогенідів зменшується. АgF добре розчинний у воді. Усі галогени у вільному стані – окислювачі. Сила їх як окислювачів знижується від фтору до йоду. У кристалічному, рідкому та газоподібному стані всі галогени існують у вигляді окремих молекул. Атомні радіуси зростають у тому напрямку, що призводить до підвищення температури плавлення і кипіння. Фтор дисоціює на атоми краще за йод. Електродні потенціали під час переходу вниз по підгрупі галогенів знижуються. У фтору найвищий електродний потенціал. Фтор – найсильніший окисник. Будь-який вільний галоген витіснить нижчестоящий, що знаходиться в стані негативного однозарядного іона в розчині.
20. Хлор. Хлороводень та соляна кислота
Хлор (Cl) –стоїть у 3-му періоді, у VII групі головної підгрупи періодичної системи, порядковий номер 17, атомна маса 35453; відноситься до галогенів.
Фізичні властивості:газ жовто-зеленого кольору із різким запахом. Щільність 3214 г/л; температура плавлення –101 °C; температура кипіння -33,97 ° C, При звичайній температурі легко зріджується під тиском 0,6 МПа. Розчиняючись у воді, утворює хлорну воду жовтого кольору. Добре розчинний в органічних розчинниках, особливо в гексані (C6H14), у чотирихлористому вуглеці.
Хімічні властивості хлору:Електронна конфігурація: 1s22s22p63s22p5. На зовнішньому рівні 7 електронів. До завершення рівня потрібен 1 електрон, який приймає хлор, проявляючи ступінь окислення -1. Існують і позитивні ступені окислення хлору до + 7. Відомі такі оксиди хлору: Cl2O, ClO2, Cl2O6 і Cl2O7. Усі вони нестійкі. Хлор – сильний окисник. Він безпосередньо реагує з металами та неметалами:
Реагує із воднем. За звичайних умов реакція йде повільно, при сильному нагріванні або освітленні – з вибухом, за ланцюговим механізмом:
![]()
Хлор взаємодіє з розчинами лугів, утворюючи солі – гіпохлорити та хлориди:
При пропущенні хлору в розчин лугу утворюється суміш розчинів хлориду та гіпохлориту:
Хлор - відновник: Cl2 + 3F2 = 2ClF3.
Взаємодія з водою:
Хлор не взаємодіє безпосередньо з вуглецем, азотом та киснем.
Отримання: 2NaCl + F2 = 2NaF + Cl2.
Електроліз: 2NaCl + 2H2O = Cl2 + H2 + 2NaOH.
Знаходження у природі:міститься у складі мінералів: галіт (кам'яна сіль), сильвін, бішофіт; морська вода містить хлориди натрію, калію, магнію та інших елементів.
Хлороводень HCl. Фізичні властивості:безбарвний газ, важчий за повітря, добре розчинний у воді з утворенням соляної кислоти.
Отримання:в лабораторії:
У промисловості: спалюють водень у струмені хлору. Далі хлороводень розчиняють у воді і отримують соляну кислоту (див. вище).
Хімічні властивості: соляна кислота – сильна, одноосновна, взаємодіє з металами, що стоять у ряді напруги до водню: Zn + 2HCl = ZnCl2 + H2.
Як відновник реагує з оксидами та гідроксидами багатьох металів.
ВИЗНАЧЕННЯ
Галогени- Елементи VII А групи - фтор (F), хлор (Cl), бром (Br) і йод (I).
Електронна конфігурація зовнішнього енергетичного рівня галогенів ns2np5. Оскільки до завершення енергетичного рівня галогенам не вистачає всього одного електрона, в ОВР вони найчастіше виявляють властивості окислювачів. Ступені окиснення галогенів: від -1 до +7. Єдиний елемент групи галогенів – фтор – виявляє лише один ступінь окислення «-1» і є найбільш електронегативним елементом. Молекули галогенів двоатомні: F 2 Cl 2 Br 2 I 2 .
Хімічні властивості галогенів
Зі зростанням заряду ядра атома хімічного елемента, тобто. при переході від фтору до йоду окислювальна здатність галогенів знижується, що підтверджується здатністю витіснення галогенів, що стоять нижче, вищими з галогеноводородних кислот та їх солей:
Br 2 + 2HI = I 2 + 2HBr;
Cl2+2KBr = Br2+2KCl.
Найбільшу хімічну активність має фтор. Більшість хімічних елементів навіть за кімнатної температури взаємодіє з фтором, виділяючи велику кількість теплоти. У фторі горить навіть вода:
2H 2 O + 2F 2 = 4HF + O 2 .
Вільний хлор менш реакційноздатний, ніж фтор. Він безпосередньо не реагує з киснем, азотом та благородними газами. З усіма іншими речовинами він взаємодіє подібно до фтору:
2Fe + Cl 2 = 2FeCl 3;
2P + 5Cl 2 = 2PCl 5 .
При взаємодії хлору з водою на холоді відбувається оборотна реакція:
Cl 2 + H 2 O↔HCl +HClO.
Суміш, що є продуктами реакції, називають хлорною водою.
При взаємодії хлору з лугами на холоді утворюються суміші хлоридів та гіпохлоритів:
Cl 2 + Ca(OH) 2 = Ca(Cl)OCl + H 2 O.
При розчиненні хлору в гарячому розчині лугу відбувається реакція:
3Cl 2 + 6KOH = 5KCl +KClO 3 +3H 2 O.
Бром, як і хлор розчиняється у воді і, частково реагуючи з нею, утворює так звану бромну воду, тоді як йод у воді практично нерозчинний.
Йод суттєво відрізняється за хімічною активністю від інших галогенів. Він не реагує з більшістю неметалів, а з металами повільно реагує лише при нагріванні. Взаємодія йоду з воднем відбувається тільки при сильному нагріванні, реакція є ендотермічною та сильно оборотною:
Н 2 + I 2 = 2HI – 53 кДж.
Фізичні властивості галогенів
За н.у. фтор – газ світло-жовтого кольору, що має різкий запах. Отруйний. Хлор – газ світло-зеленого кольору, як і фтор має різкий запах. Сильно отруйний. При підвищеному тиску та кімнатній температурі легко переходить у рідкий стан. Бром - важка рідина червоно-бурого кольору з характерним неприємним різким запахом. Рідкий бром, а також його пари сильно отруйні. Бром погано розчиняється у воді та добре у неполярних розчинниках. Йод – тверда речовина темно-сірого кольору із металевим блиском. Пари йоду мають фіолетовий колір. Йод легко виганяє, тобто. переходить у газоподібний стан із твердого, при цьому минаючи рідкий стан.
Одержання галогенів
Галогени можна отримати при електролізі розчинів або розплавів галогенідів:
MgCl 2 = Mg + Cl 2 (розплав).
Найчастіше галогени отримують реакції окислення галогенводневих кислот:
MnO 2 + 4HCl = MnCl 2 + Cl 2 +2H 2 O;
K 2 Cr 2 O 7 + 14HCl = 3Cl 2 + 2KCl +2CrCl 3 +7H 2 O;
2KMnO 4 +16HCl = 2MnCl 2 +5Cl 2 +8H 2 O +2KCl.
Застосування галогенів
Галогени використовують як сировину для отримання різних продуктів. Так, фтор та хлор використовують для синтезу різних полімерних матеріалів, хлор також є сировиною при виробництві соляної кислоти. Бром та йод знайшли широке застосування в медицині, бром також використовується лакофарбової промисловості.
Приклади розв'язання задач
ПРИКЛАД 1
| Завдання | Розрахуйте об'єм хлору (н. у.), який прореагував з йодидом калію, якщо утворився йод масою 508 г | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Рішення | Запишемо рівняння реакції взаємодії хлору з йодидом калію: Cl 2 + 2KI = I 2 + 2KCl Молярна маса йоду, розрахована з допомогою таблиці хімічних елементів Д.І. Менделєєва, дорівнює – 254 г/моль. Знайдемо кількість речовини йоду, що утворився: v(I 2) = m(I 2)/M(I 2) At, відкритий 1940 р.
Розподіл за орбіталями електронів зовнішнього електронного шару у всіх галогенів однотипний
Мають багато спільного у будові атомів та молекул. У них завершується забудова р-оболонки зовнішнього шару, тому всі вони належать до р-елементів. Зовнішньому електронному шару атомів галогенів бракує до завершення одного електрона, тому електронегативність у цих елементів виражена яскраво і в окислювально-відновних реакціях вони поводяться в основному як окислювачі. ■ 1. Як змінюється величина атомного радіусу залежно від зростання заряду ядра атома?
Фізичні властивості галогенівУсі властивості галогенів, як фізичні, і хімічні, залежить від будови атомів елементів. Ці властивості різних галогенів багато в чому подібні, але водночас кожному галогену властивий ряд особливостей. ■ 7. Як змінюється інтенсивність фарбування галогенів із зростанням зарядів ядер?
10. Складіть та заповніть таблицю «Фізичні властивості галогенів» за таким зразком:
Фізіологічна дія галогенівВсі отруйні за своєю фізіологічною дією. Особливо отруйний фтор: при вдиханні у невеликих кількостях він викликає набряк легень, у великих – руйнування легеневої тканини та смерть. Йоднайменш отруйний із усіх галогенів. Вдихання парів йоду при його нагріванні може викликати отруєння, але працювати з пароподібним йодом доводиться рідко, наприклад при очищенні його сублімацією. Кристалічний йод руками брати не слід, тому що при попаданні на шкіру він викликає появу характерних жовтих плям. Усі роботи з галогенами слід проводити у витяжній шафі. Запишіть у зошит заходи техніки безпеки у роботі з галогенами та першої допомоги при отруєннях. Хімічні властивості галогенів
За характером хімічних властивостей, як зазначено вище, всі галогени є типовими неметалами, що мають значну електронегативність. Найбільш електронегативним елементом, що має найбільшу неметалеву активність, є фтор, найменш активний йод. Рис. 21.Горіння водню у хлорі. 1-хлор 2- Взаємодія галогенів із простими речовинами. Простежити зменшення хімічної активності від фтору до хлору можна з прикладами різних реакцій. Особливо цікава взаємодія різних галогенів із воднем. Умови реакцій у них різні. Фтористий є найбільш міцною сполукою серед галогеноводородів. З воднем бром утворює бромистий водень.
Окисні властивості галогени виявляють і при взаємодії з металами, яке протікає зазвичай дуже активно. Рис. 22. Наприклад. Сu + Сl2 = СuСl2 Тут у реакції з хлором виявляє ступінь окислення, що дорівнює +3 - Fe +3 , а рівну +2- Cu +2 . У всіх наведених випадках хлор поводиться як . Хімія Елементів Неметали VIIА-підгрупи Елементи VIIА-підгрупи є типовими неметалами з високою електронегативністю, вони мають групову назву – «галогени». Основні питання, що розглядаються в лекції Загальна характеристика неметалів VIIА-підгрупи. Електронна будова, найважливіші показники атомів. Найбільш характерні сте- пені окиснення. Особливості хімії галогенів. Прості речовини. Природні сполуки. З'єднання галогенів Галогенводневі кислоти та їх солі. Соляна та плавикова ки- слота, отримання та застосування. Галогенідні комплекси. Бінарні кисневі сполуки галогенів. Нестійкість ок- Окисно-відновні властивості простих речовин і со- єднань. Реакції диспропорціонування. Діаграми Латімера.
Хімія елементів VIIA-підгрупи Загальна характеристика
VIIА-групу утворюють р-елементи: фтор F, хлор Cl, бром Br, йод I та астат At. Загальна формула валентних електронів – ns 2 np 5 . Усі елементи VIIА-групи – типові неметали.
для формування стійкої восьмиелектронної об- лочки, тому в нихсильно виражена тенденція до приєднання електрона. Всі елементи легко утворюють прості однозаряд- ні аніони Г -. У формі простих аніонів елементи VIIА-групи знаходяться в природній воді та в кристалах природних солей, наприклад, галіту NaCl, сильвіну KCl, флюориту CaF2. Загальна групова назва елементів VIIА- групи «галогени» , тобто «що народжують солі», пов'язано з тим, що більшість їх з'єднань з металами перед- являє собою типові солі (CaF2, NaCl, MgBr2, KI), ко- тори можуть бути отримані при безпосередньому взає- дії металу з галогеном. Вільні галогени одержують із природних солей, тому назву «галогени» також перекладають, як «народжені із солей».
Мінімальний ступінь окислення (–1) є найбільш стійким у всіх галогенів. Деякі характеристики атомів елементів VIIА-групи наведено в Найважливіші характеристики атомів елементів VIIА-групи
Галогени відрізняються високою спорідненістю до електрона (максимальним у Cl) і дуже великою енергією іонізації (максимальною у F) та максимально можливу в кожному з періодів електронегативність. Фтор – самий електронегативний із усіх хімічних елементів. Наявність одного неспареного електрона в атомах галогенів обумовили- дає об'єднання атомів у простих речовинах у двоатомні молекули Г2. Для простих речовин галогенів найбільш характерні окислювач- ні властивості, найбільш сильні у F2 і що слабшають при переході до I2. Галогени характеризуються найбільшою реакційною здатністю з усіх неметалевих елементів. Фтор навіть серед галогенів виділяє ється надзвичайно високою активністю. Елемент другого періоду – фтор найбільш сильно відрізняється від інших. гих елементів підгрупи. Це загальна закономірність для всіх неметалів.
Фтор, як самий електронегативний елемент, не виявляє поло- степенів окислення. У будь-яких з'єднаннях, у тому числі з кі- слородом, фтор перебуває у ступеня окислення (-1). Всі інші галогени виявляють позитивні ступені окис- лення аж до максимальної +7. Найбільш характерні ступені окислення галогенів: F: -1, 0; Cl, Br, I: -1, 0, +1, +3, +5 +7. У Cl відомі оксиди, в яких він знаходиться в ступенях окиснення: +4 та +6. Найбільш важливими сполуками галогенів, у позитивних сте- пенях окислення, є кисневмісні кислоти та їх солі. Всі сполуки галогенів у позитивних ступенях окиснення яв- ються сильними окислювачами. моторошний ступінь окиснення.Диспропорціонування сприяє лужне середовище. Практичне застосування простих речовин і кисневих сполук ній галогенів пов'язано головним чином з їхньою окисною дією. Найширше практичне застосування знаходять прості речовини Cl2 та F2 . Найбільша кількість хлору і фтору витрачається в промисловому ор- ганічному синтезі: у виробництві пластмас, хладоагентів, розчинників, отрутохімікатів, ліків. Значна кількість хлору та йоду використовується для отримання металів та для їх рафінування. Хлор використовується також для відбілювання целюлози, для знезараження питної води та у вироб- водстві хлорного вапна та соляної кислоти. Солі оксокислот застосовують у виробництві вибухових речовин.
Широке практичне застосування знаходять кислоти – соляна та плави- Фтор і хлор належать до двадцяти найпоширеніших еле- там, значно менше в природі брому та йоду. Усі галогени перебувають у природі у ступені окислення(-1). Лише йод зустрічається у вигляді солі KIO3. яка як домішка входить у чилійську селітру (KNO3). Астат – штучно отриманий радіоактивний елемент (його немає у природі). Нестійкість At відображається в назві, що походить від грец. "Астатос" - "нестійкий". Астат є зручним – випромінювачем для радіотерапії ракових пухлин. Прості речовини Прості речовини галогенів утворені двоатомними молекулами Г2. У простих речовинах при переході від F2 до I2 зі збільшенням числа електро- тронних шарів та зростанням поляризуемості атомів відбувається посилення міжмолекулярної взаємодії, що призводить до зміни агрегатного спів- стояння за стандартних умов. Фтор (за нормальних умов) – жовтий газ, при –181о З перетворюється на рідкий стан. Хлор – жовто-зелений газ, переходить у рідину при –34о С. З кольором га- за пов'язана назва Cl, воно походить від грецького «хлорос» – «жовто- зелений». Різке підвищення температури кипіння у Cl2 порівняно з F2 вказує на посилення міжмолекулярної взаємодії. Бром - темно-червона, дуже летюча рідина, кипить при 58,8 о С. На- звання елемента пов'язане з різким неприємним запахом газу та утворено від "бромос" - "смердючий". Йод – темно-фіолетові кристали, зі слабким «металевим» бле- ском, які при нагріванні легко виганяється, утворюючи фіолетові пари;
кипіння йоду дорівнює 183о С. Від кольору парів йоду походить його назва – "іодос" - "фіолетовий". Всі прості речовини мають різкий запах і є отруйними. Вдихання їх пар викликає подразнення слизових оболонок і дихальних органів, а при великих концентраціях - задуха. Під час першої світової війни хлор застосовували як отруйну речовину. Газоподібний фтор та рідкий бром викликають опіки шкіри. Працюючи з га- логенами, слід дотримуватися запобіжних заходів. Оскільки прості речовини галогенів утворені неполярними моле- кулами, вони добре розчиняються в неполярних органічних розчинниках: спирті, бензолі, чотирихлористому вуглеці і т. п. У воді хлор, бром та йод обмежено розчинні, їх водні розчини називають хлорною, бромною та йодною водою. Краще інших розчиняється Br2 концентрація брому в наси- щенном розчині досягає 0,2 моль/л, а хлору – 0,1 моль/л. Фтор розкладає воду: 2F2 + 2H2 O = O2 + 4HF Галогени виявляють високу окисну активність і перехо- дять в галогенідні аніони. Г2 + 2e– 2Г– Особливо високою окисною активністю має фтор. Фтор окислює шляхетні метали (Au, Pt). Pt + 3F2 = PtF6 Взаємодіє навіть із деякими інертними газами (криптоном, ксеноном і радоном), наприклад, Xe + 2F2 = XeF4 В атмосфері F2 горять багато дуже стійких сполук, наприклад, вода, кварц (SiO2). SiO2 + 2F2 = SiF4 + O2
У реакціях з фтором навіть такі сильні окислювачі, як азотна та сер- ная кислота, виступають у ролі відновників, при цьому фтор окислює вхо- дить у складі О(–2). 2HNO3 + 4F2 = 2NF3 + 2HF + 3O2 H2 SO4 + 4F2 = SF6 + 2HF + 2O2 Висока реакційна здатність F2 створює труднощі з вибором кон- структурних матеріалів для роботи з ним. Зазвичай для цих цілей використовую- ють нікель та мідь, які, окислюючись, утворюють на своїй поверхні щільні захисні плівки фторидів. Назва F пов'язана з його агресивним дій- ним, воно походить від грец. "фторос" - "руйнівний". У ряді F2 , Cl2 , Br2 , I2 окисна здатність слабшає через уве- лічення розміру атомів та зменшення електронегативності. У водних розчинах окисні та відновлювальні властивості ве- ств зазвичай характеризують за допомогою електродних потенціалів. У таблиці наведено стандартні електродні потенціали (Ео, В) для напівреакцій вос- становлення галогенів Для порівняння також наведено значення Ео для кі- слорода - найпоширенішого окислювача. Стандартні електродні потенціали для простих речовин галогенів
Зменшення окисної активності Як видно з таблиці, F2 – окислювач значно сильніший, ніж О2 , тому F2 у водних розчинах не існує , він окислює воду, відновлюючись до F-. Судячи з значення Eо окислювальна здатність Cl2
також вище, ніж у О2. Дійсно, при тривалому зберіганні хлорної води відбувається її розкладання з виділенням кисню та з утворенням HCl. Але реакція йде повільно (молекула Cl2 помітно міцніша, ніж молекула F2 і енергія активації для реакцій з хлором вище), швидше відбувається диспро- порціонування: Cl2 + H2 O HCl + HOCl У воді воно не досягає кінця (К = 3,9 . 10–4 ), тому Cl2 існує у водних розчинах. Ще більшою стійкістю у воді характеризуються Br2 та I2. Диспропорціонування це дуже характерна окисно- відновлювальна реакція для галогенів. Диспропорціонування усі- ливається в лужному середовищі. Диспропорціонування Cl2 у лугу призводить до утворення аніонів Cl- і ClO-. Константа диспропорціонування дорівнює 7,5. 1015 . Cl2 + 2NaOH = NaCl + NaClO + H2 O При диспропорціонуванні йоду в лугу утворюються I-і IO3-. Ана- логічно йоду диспропорціонує Br2. Зміна продукту диспропорційно- нування обумовлено тим, що аніони ГО-і ГО2 - у Br і I нестійкі. Реакція диспропорціонування хлору використовується в промислово- сти для отримання сильного і швидко діючого окислювача гіпохлориту, білільного вапна, бертолетової солі. 3Cl2 + 6 KOH = 5KCl + KClO3 + 3H2 O
Взаємодія галогенів із металами Галогени енергійно взаємодіють з багатьма металами, наприклад: Mg + Cl2 = MgCl2 Ti + 2I2 TiI4 Галогеніди Na + , в яких метал має низький ступінь окиснення (+1, +2), – це солеподібні сполуки з переважно іонним зв'язком. Як прави- ло, іонні галогеніди – це тверді речовини з високою температурою плав- Галогеніди металів, в яких метал має високий ступінь окислення. ня, – це з'єднання з переважно ковалентним зв'язком. Багато хто з них за звичайних умов є газами, рідинами або легкоплавкими твердими речовинами. Наприклад, WF6 – газ, MoF6 – рідина, TiCl4 – рідина. Взаємодія галогенів із неметалами Галогени безпосередньо взаємодіють з багатьма неметалами: воднем, фосфором, сіркою та ін. Наприклад: H2 + Cl2 = 2HCl 2P + 3Br2 = 2PBr3 S + 3F2 = SF6 Зв'язок у галогенідах неметалів переважно ковалентний. Зазвичай ці сполуки мають невисокі температури плавлення та кипіння. При переході від фтору до йоду ковалентний характер галогеніду посилюється. Ковалентні галогеніди типових неметалів є кислотними сполуками; при взаємодії із водою вони гидролизуются із заснуванням кислот. Наприклад: PBr3 + 3H2 O = 3HBr + H3 PO3 PI3 + 3H2 O = 3HI + H3 PO3 PCl5 + 4H2 O = 5HCl + H3 PO4
Дві перші реакції використовуються для отримання бромо- та йодоводород- ної кислоти. Інтергаліди. Галогени, з'єднуючись один з одним, утворюють інтерга- ліди. У цих сполуках легший і більш електронегативний галоген знаходиться в ступені окислення (–1), а більш важкий – у позитивній сте- пені окиснення. За рахунок безпосередньої взаємодії галогенів під час нагрівання виходять: ClF, BrF, BrCl, ICl. Існують і складніші інтергаліди: ClF3, BrF3, BrF5, IF5, IF7, ICl3. Усі інтергаліди за звичайних умов – рідкі речовини із низькими температурами кипіння. Інтергаліди мають високу окисну ак- тивність. Наприклад, у парах ClF3 горять такі хімічно стійкі речовини, як SiO2, Al2 O3, MgO та ін. 2Al2 O3 + 4ClF3 = 4 AlF3 + 3O2 + 2Cl2 Фторид ClF 3 – агресивний фторуючий реагент, що діє Реє F2 . Його застосовують в органічних синтезах та для отримання захисних плівок на поверхні нікелевої апаратури для роботи з фтором. У воді інтергаліди гідролізуються з утворенням кислот. Наприклад, ClF5 + 3H2 O = HClO3 + 5HF Галогени в природі. Отримання простих речовин У промисловості галогени отримують із їхніх природних сполук. Усе процеси одержання вільних галогенів засновані на окисненні гало- нід-іонів. 2Г – Г2 + 2e– Значна кількість галогенів перебуває у природних водах як аніонів: Cl– , F– , Br – , I– . У морській воді може бути до 2,5 % NaCl. Бром та йод отримують з води нафтових свердловин та морської води.
Будова та властивості атомів. Елементи головної підгрупи VII групи Періодичної системи Д. І. Менделєєва, об'єднані під загальною назвою галогени - фтор F, хлор Сl, бром Вr, йод I, астат At (рідко зустрічається в природі) - типові неметали. Це і зрозуміло, адже їхні атоми містять на зовнішньому енергетичному рівні сім електронів, і їм не вистачає лише одного електрона, щоб завершити його. Атоми галогенів при взаємодії із металами приймають електрон від атомів металів. При цьому виникає іонний зв'язок та утворюються солі. Звідси і походить загальна назва підгрупи «галогени», тобто «солі, що народжують». Галогени - дуже сильні окисники. Фтор у хімічних реакціях виявляє лише окисні властивості, і для нього характерна лише ступінь окиснення -1 у сполуках. Інші галогени виявляють і відновлювальні властивості при взаємодії з електронегативними елементами - фтором, киснем, азотом. Їх ступеня окиснення можуть набувати значення +1, +3, +5, +7. Відновлювальні властивості галогенів посилюються від хлору до йоду, що пов'язано зі збільшенням радіусів їх атомів: атоми хлору приблизно в півтора рази менші, ніж йоду. Галогени - прості речовини. Всі галогени існують у вільному стані у вигляді двоатомних молекул з ковалентним неполярним хімічним зв'язком між атомами. У твердому стані F 2 , Сl 2 , Вr 2 , I 2 мають молекулярні кристалічні ґрати, що підтверджується їх фізичними властивостями (табл. 7). Таблиця 7
Як можна помітити, зі збільшенням молекулярної маси галогенів підвищуються їх температури плавлення та кипіння (рис. 88), зростає щільність: фтор та хлор – гази, бром – рідина, йод – тверда речовина.
Рис. 88. Це з тим, що з збільшенням розмірів атомів і галогенів (мал. 89) зростають і сили міжмолекулярного взаємодії з-поміж них.
Рис. 89. Від F 2 до I 2 посилюється інтенсивність фарбування галогенів. Кристали йоду мають металевий блиск. Хімічна активність галогенів, як неметалів, від фтору до йоду слабшає. Кожен галоген є найсильнішим окисником у своєму періоді. Окисні властивості галогенів чітко виявляються при їх взаємодії з металами. При цьому, як ви знаєте, утворюються солі. Так, фтор вже за звичайних умов реагує з більшістю металів, а при нагріванні – і із золотом, сріблом, платиною, відомими своєю хімічною пасивністю. Алюміній та цинк в атмосфері фтору займаються:
Інші галогени реагують з металами в основному при нагріванні. Так, у колбі, наповненій хлором, гарно спалахують і згоряють кристали подрібненої сурми (рис. 90), утворюючи при цьому суміш двох хлоридів сурми (III) і (V):
Рис. 90. Нагрітий порошок заліза також спалахує при взаємодії з хлором. Досвід можна провести і з сурмою, але тільки залізне тирсу потрібно попередньо розжарити в залізній ложечці, а потім висипати їх невеликими порціями в колбу з хлором. Оскільки хлор є сильним окисником, то в результаті реакції утворюється хлорид заліза (III) (рис. 91):
Рис. 91. У парах брому згорає розпечений мідний дріт:
Йод окислює метали повільніше, але у присутності води, що є каталізатором, реакція йоду з порошком алюмінію протікає дуже бурхливо.
Реакція супроводжується виділенням фіолетової пари йоду (чому?). Про зменшення окисних та збільшення відновлювальних властивостей галогенів від фтору до йоду можна судити і за їх здатністю витісняти один одного з розчинів солей.
Рис. 92. Вільний бром витісняє йод із солей:
Для фтору ця реакція не характерна, оскільки вона протікає у розчині, а фтор взаємодіє з водою, витісняючи з неї кисень:
Тут кисень виступає у незвичній собі ролі відновника. Це, мабуть, єдиний випадок, коли кисень у реакції горіння не одна з вихідних речовин, та її продуктом. Ослаблення окисних властивостей галогенів від фтору до йоду наочно проявляється при їх взаємодії з воднем. Рівняння цієї реакції можна записати у загальному вигляді: Н 2 + Г 2 = 2НГ (Г – умовне хімічне позначення галогенів). Якщо фтор взаємодіє з воднем у будь-яких умовах із вибухом, то суміш хлору з воднем реагує з вибухом тільки під час запалювання або опромінення прямим сонячним світлом, бром взаємодіє з воднем при нагріванні і без вибуху. Ці екзотермічні реакції. Реакція з'єднання кристалічного йоду з воднем слабоендотермічна, вона протікає повільно навіть при нагріванні. В результаті цих реакцій утворюються відповідно фтороводород HF, хлороводень НСl, бромоводень НВr та йодоводород HI. Відкриття галогенів. Фтор у вільному вигляді отримав уперше в 1886 р. французький хімік А. Муассан, який був удостоєний Нобелівської премії. Свою назву елемент отримав від грецького фторос – «руйнівний». Хлор відкритий шведським хіміком К. Шееле в 1774 р. Елемент отримав назву за колір простої речовини (від грец. Хлорос - жовто-зелений). Бром відкрито 1826 р. французьким хіміком А. Баларом. Елемент названий так за запах простої речовини (від грец. бромос – смердючий). Йод отриманий в 1811 р. французьким ученим Б. Куртуа, а назву отримав за колір пари простої речовини (від грец. Йодес - фіолетовий). Нові слова та поняття
Завдання для самостійної роботи
Читайте також: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||