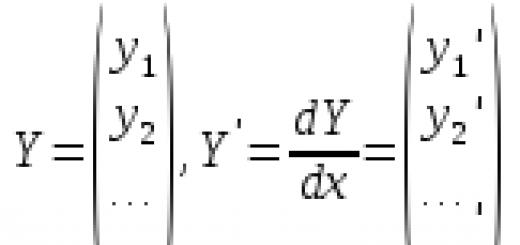Задача.
Вычислить массу соли и воды, необходимые для приготовления 40 г раствора NаСl с массовой долей 5%.
1. Запишите условие задачи с помощью общепринятых обозначений
m р-ра = 40г
1. Рассчитайте массу растворенного вещества по формуле:
m в-ва = ω ∙ m р-ра /100%
m (NаСl) = 5% · 40г/100% = 2г
2. Найдите массу воды по разности между массой раствора и массой растворенного вещества:
m р-ля = m р-ра – m в-ва
m (Н 2 О) = 40г – 2г = 38 г.
3. Запишите ответ.
Ответ: для приготовления раствора необходимо взять 2г соли и 38г воды.
Алгоритм нахождения массовой доли растворенного вещества при разбавлении (упаривании) раствора
Задача
m р-ра1 =80г
m(Н 2 О) = 30г
1. В результате разбавления (упаривания) раствора масса раствора увеличилась (уменьшилась), а вещества в нём осталось столько же.
Рассчитайте массу растворённого вещества, преобразуя формулу:
ω = m в-ва /m р-ра ∙ 100%
m в-ва = ω 1 · m р-ра1 /100%
m в-ва = 15% · 80г = 12г
2. При разбавлении раствора общая масса его увеличивается (при упаривании - уменьшается).
Найдите массу вновь полученного раствора:
m р-ра2 = m р-ра1 + m(H 2 O)
m р-ра2 = 80г + 30г=110г
3. Рассчитайте массовую долю растворённого вещества в новом растворе:
ω 2 = m в-ва / m р-ра2 ∙ 100%
ω 2 = 12г/ 110г· 100% = 10,9%
4. Запишите ответ
Ответ: массовая доля растворенного вещества в растворе при разбавлении равна 10,9%
Алгоритм решения задач по «правилу креста»
Для получения раствора с заданной массовой долей (%) растворенного вещества путем смешивания двух растворов с известной массовой долей растворенного вещества пользуются диагональной схемой ("правило креста").
Сущность этого метода состоит в том, что по диагонали из большей величины массовой доли растворенного вещества вычитают меньшую.
Разности (с-в) и (а-с) показывают, в каких соотношениях нужно взять растворы а и в, чтобы получить раствор с.
Если для разбавления в качестве исходного раствора используют чистый растворитель, например, Н 2 0, то концентрация его принимается за 0 и записывается с левой стороны диагональной схемы.
Задача
Для обработки рук хирурга, ран, послеоперационного поля используется йодная настойка с массовой долей 5%. В каком массовом соотношении нужно смешать растворы с массовыми долями йода 2,5% и 30%, чтобы получить 330 г йодной настойки с массовой долей йода 5%?
1. Запишите условие задачи с помощью общепринятых обозначений.
1. Составьте "диагональную схему". Для этого запишите массовые доли исходных растворов друг под другом, по левую сторону креста, а в центре заданную массовую долю раствора.
2. Вычитают из бóльшей массовой доли меньшую (30–5=25; 5–2,5=2,5) и находят результаты.
Записывают найденные результаты с правой стороны диагональной схемы: при возможности сокращают полученные числа. В данном случае 25 в десять раз больше, чем 2,5, то есть вместо 25 записывают 10, вместо 2,5 пишут 1.
Числа (в данном случае 25 и 2,5 или 10 и 1)называют массовыми числами. Массовые числа показывают, в каком соотношении необходимо взять исходные растворы, чтобы получить раствор с массовой долей йода 5%.
3. Определите массу 30% и 2,5% раствора по формуле:
m р-ра = число частей · m 3 / сумму массовых частей
m 1 (30%) = 1· 330г /1+10 = 30г
m 2 (2,5%) = 10 · 330г/ 1+10 = 300г
4. Запишите ответ.
Ответ: для приготовления 330 г раствора с массовой долей йода 5% необходимо смешать 300 г раствора с массовой долей 2,5% и 30 г с массовой долей 30%.
Задача 3.1. Определите массу воды в 250 г 10%-ного раствора хлорида натрия.
Решение.
Из w = m в-ва / m р-ра
находим массу хлорида натрия:
m в-ва = w m р-ра = 0,1 250 г = 25 г NaCl
Поскольку m р-ра = m в-ва + m р-ля
, то получаем:
m(Н 2 0) = m р-ра — m в-ва = 250 г — 25 г = 225 г Н 2 0
.
Задача 3.2. Определите массу хлороводорода в 400 мл раствора соляной кислоты с массовой долей 0,262 и плотностью 1,13 г/мл.
Решение.
Поскольку w = m в-ва / (V ρ)
, то получаем:
m в-ва = w V ρ = 0,262 400 мл 1,13 г/мл = 118 г
Задача 3.3. К 200 г 14%-ного раствора соли добавили 80 г воды. Определите массовую долю соли в полученном растворе.
Решение.
Находим массу соли в исходном растворе:
m соли = w m р-ра = 0,14 200 г = 28 г.
Эта же масса соли осталась и в новом растворе. Находим массу нового раствора:
m р-ра = 200 г + 80 г = 280 г.
Находим массовую долю соли в полученном растворе:
w = m соли / m р-ра = 28 г / 280 г = 0,100.
Задача 3.4. Какой объем 78%-ного раствора серной кислоты с плотностью 1,70 г/мл надо взять для приготовления 500 мл 12%-ного раствора серной кислоты с плотностью 1,08 г/мл?
Решение.
Для первого раствора имеем:
w 1 = 0,78
и ρ 1 = 1,70 г/мл
.
Для второго раствора имеем:
V 2 = 500 мл, w 2 = 0,12
и ρ 2 = 1,08 г/мл
.
Поскольку второй раствор готовим из первого добавлением воды, то массы вещества в обоих растворах одинаковы. Находим массу вещества во втором растворе. Из w 2 = m 2 / (V 2 ρ 2)
имеем:
m 2 = w 2 V 2 ρ 2 = 0,12 500 мл 1,08 г/мл = 64,8 г.
m 2 = 64,8 г
. Находим
объем первого раствора. Из w 1 = m 1 / (V 1 ρ 1)
имеем:
V 1 = m 1 / (w 1 ρ 1) = 64,8 г / (0,78 1,70 г/мл) = 48,9 мл.
Задача 3.5. Какой объем 4,65%-ного раствора гидроксида натрия с плотностью 1,05 г/мл можно приготовить из 50 мл 30%-ного раствора гидроксида натрия с плотностью 1,33 г/мл?
Решение.
Для первого раствора имеем:
w 1 = 0,0465
и ρ 1 = 1,05 г/мл
.
Для второго раствора имеем:
V 2 = 50 мл
, w 2 = 0,30
и ρ 2 = 1,33 г/мл
.
Поскольку первый раствор готовим из второго добавлением воды, то массы вещества в обоих растворах одинаковы. Находим массу вещества во втором растворе. Из w 2 = m 2 / (V 2 ρ 2)
имеем:
m 2 = w 2 V 2 ρ 2 = 0,30 50 мл 1,33 г/мл = 19,95 г.
Масса вещества в первом растворе также равна m 2 = 19,95 г
.
Находим объем первого раствора. Из w 1 = m 1 / (V 1 ρ 1)
имеем:
V 1 = m 1 / (w 1 ρ 1) = 19,95 г / (0,0465 1,05 г/мл) = 409 мл
.
Коэффициент растворимости (растворимость) - максимальная масса вещества, растворимая в 100 г воды при данной температуре. Насыщенный раствор - это раствор вещества, который находится в равновесии с имеющимся осадком этого вещества.
Задача 3.6. Коэффициент растворимости хлората калия при 25 °С равен 8,6 г. Определите массовую долю этой соли в насыщенном растворе при 25 °С.
Решение.
В 100 г воды растворилось 8,6 г соли.
Масса раствора равна:
m р-ра = m воды + m соли = 100 г + 8,6 г = 108,6 г
,
а массовая доля соли в растворе равна:
w = m соли / m р-ра = 8,6 г / 108,6 г = 0,0792
.
Задача 3.7. Массовая доля соли в насыщенном при 20 °С растворе хлорида калия равна 0,256. Определите растворимость этой соли в 100 г воды.
Решение.
Пусть растворимость соли равна х
г в 100 г воды.
Тогда масса раствора равна:
m р-ра = m воды + m соли = (х + 100) г
,
а массовая доля равна:
w = m соли / m р-ра = х / (100 + х) = 0,256
.
Отсюда
х = 25,6 + 0,256х; 0,744х = 25,6; х = 34,4 г
на 100 г воды.
Молярная концентрация с
- отношение количества растворенного вещества v (моль)
к объему раствора V (в литрах)
, с = v(моль) / V(л)
, с = m в-ва / (М V(л))
.
Молярная концентрация показывает число моль вещества в 1 л раствора: если раствор децимолярный (с = 0,1 М = 0,1 моль/л
) значит, что в 1 л раствора содержится 0,1 моль вещества.
Задача 3.8. Определите массу КОН, необходимую для приготовления 4 л 2 М раствора.
Решение.
Для растворов с молярной концентрацией имеем:
с = m / (М V)
,
где с
- молярная концентрация,
m
- масса вещества,
М
- молярная масса вещества,
V
- объем раствора в литрах.
Отсюда
m = с М V(л) = 2 моль/л 56 г/моль 4 л = 448 г КОН
.
Задача 3.9. Сколько мл 98%-ного раствора Н 2 SO 4 (ρ = 1,84 г/мл) необходимо взять для приготовления 1500 мл 0,25 М раствора?
Решение. Задача на разбавление раствора. Для концентрированного раствора имеем:
w 1 = m 1 / (V 1 (мл) ρ 1)
.
Необходимо найти объем этого раствора V 1 (мл) = m 1 / (w 1 ρ 1)
.
Поскольку разбавленный раствор готовится из концентрированного смешиванием последнего с водой, то масса вещества в этих двух растворах будет одинакова.
Для разбавленного раствора имеем:
с 2 = m 2 / (М V 2 (л))
и m 2 = с 2 М V 2 (л)
.
Найденное значение массы подставляем в выражение для объема концентрированного раствора и проводим необходимые вычисления:
V 1 (мл) = m / (w 1 ρ 1) = (с 2 М V 2) / (w 1 ρ 1) = (0,25 моль/л 98 г/моль 1,5 л) / (0,98 1,84 г/мл) = 20,4 мл
.
Расчеты концентрации
растворенных веществ
в растворах
Решение задач на разбавление растворов особой
сложности не представляет, однако требует
внимательности и некоторого напряжения. Тем не
менее можно упростить решение этих задач,
используя закон разбавления, которым пользуются
в аналитической химии при титровании растворов.
Во всех задачниках по химии показаны решения
задач, представленных как образец решения, и во
всех решениях используется закон разбавления,
принцип которого состоит в том, что количество
растворенного вещества и масса m
в исходном и разбавленном
растворах остаются неизменными. Когда мы решаем
задачу, то это условие держим в уме, а расчет
записываем по частям и постепенно, шаг за шагом,
приближаемся к конечному результату.
Рассмотрим проблему решения задач на
разбавление, исходя из следующих соображений.
Количество растворенного вещества :
= c V ,
где c – молярная концентрация растворенного вещества в моль/л, V – объем раствора в л.
Масса растворенного вещества m (р.в.):
m(р. в.) = m (р-ра) ,
где m
(р-ра) – масса раствора в г, – массовая доля
растворенного вещества.
Обозначим в исходном (или неразбавленном)
растворе величины c
, V
, m
(р-ра), через с
1 , V
1 ,
m
1 (р-ра), 1 ,
а в разбавленном растворе – через с
2 , V
2 ,
m
2 (р-ра), 2 .
Составим уравнения разбавления растворов. Левые
части уравнений отведем для исходных
(неразбавленных) растворов, а правые части – для
разбавленных растворов.
Неизменность количества растворенного вещества
при разбавлении будет иметь вид:
![]()
Сохранение массы m (р. в.):
![]()
Количество растворенного вещества связано с его массой m (р. в.) cоотношением:
= m (р. в.)/M (р. в.),
где M
(р. в.) – молярная масса растворенного
вещества в г/моль.
Уравнения разбавления (1) и (2) связаны между собой
следующим образом:
с 1 V 1 = m 2 (р-ра) 2 /M (р. в.),
m 1 (р-ра) 1 = с 2 V 2 M (р. в.).
Если в задаче известен объем растворенного газа V (газа), то его количество вещества связано с объемом газа (н.у.) отношением:
= V (газа)/22,4.
Уравнения разбавления примут соответственно вид:
V(газа)/22,4 = с 2 V 2 ,
V(газа)/22,4 = m 2 (р-ра) 2 /M (газа).
Если в задаче известны масса вещества или
количество вещества, взятого для приготовления
раствора, то в левой части уравнения разбавления
ставится m
(р. в.) или , в зависимости от условия задачи.
Если по условию задачи требуется объединить
растворы разной концентрации одного и того же
вещества, то в левой части уравнения массы
растворенных веществ суммируются.
Довольно часто в задачах используется плотность
раствора (г/мл). Но
поскольку молярная концентрация с
измеряется в моль/л, то и плотность следует
выражать в г/л, а объем V
– в л.
Приведем примеры решения «образцовых» задач.
Задача 1. Какой объем 1М раствора серной кислоты надо взять, чтобы получить 0,5 л 0,1М H 2 SO 4 ?
Дано:
с 1 = 1 моль/л,
V
2 = 0,5 л,
с
2 = 0,1 моль/л.
Найти:
Решение
V 1 с 1 = V 2 с 2 ,
V 1 1 = 0,5 0,1; V 1 = 0,05 л, или 50 мл.
Ответ. V 1 = 50 мл.
Задача 2
(,
№ 4.23). Определите массу раствора с массовой
долей
(СuSО 4)
10% и массу воды, которые потребуются для
приготовления раствора массой 500 г с массовой
долей
(СuSО 4) 2%.
Дано:
1 = 0,1,
m
2 (р-ра) = 500 г,
2 = 0,02.
Найти:
m
1 (р-ра) = ?
m
(H 2 O) = ?
Решение
m 1 (р-ра) 1 = m 2 (р-ра) 2 ,
m 1 (р-ра) 0,1 = 500 0,02.
Отсюда m 1 (р-ра) = 100 г.
Найдем массу добавляемой воды:
m(H 2 O) = m 2 (р-ра) – m 1 (р-ра),
m(H 2 O) = 500 – 100 = 400 г.
Ответ. m 1 (р-ра) = 100 г, m (H 2 O) = 400 г.
Задача 3
(,
№ 4.37). Какой объем раствора с массовой долей
серной кислоты 9,3%
( = 1,05 г/мл)
потребуется для приготовления 0,35М
раствора
H 2 SO 4
объемом 40 мл?
Дано:
1 = 0,093,
1 = 1050 г/л,
с
2 = 0,35 моль/л,
V
2 = 0,04 л,
М
(H 2 SO 4) = 98 г/моль.
Найти:
Решение
m 1 (р-ра) 1 = V 2 с 2 М (H 2 SO 4),
V 1 1 1 = V 2 с 2 М (H 2 SO 4).
Подставляем значения известных величин:
V 1 1050 0,093 = 0,04 0,35 98.
Отсюда V 1 = 0,01405 л, или 14,05 мл.
Ответ. V 1 = 14,05 мл.
Задача 4
. Какой
объем хлороводорода (н.у.) и воды потребуется,
чтобы приготовить 1 л раствора ( = 1,05 г/см 3), в котором
содержание хлороводорода в массовых долях равно
0,1
(или 10%)?
Дано:
V(р-ра) = 1 л,
(р-ра) = 1050 г/л,
= 0,1,
М
(HCl) = 36,5 г/моль.
Найти:
V
(HCl) = ?
m
(H 2 O) = ?
Решение
V(HCl)/22,4 = m (р-ра) /М (HCl),
V(HCl)/22,4 = V (р-ра) (р-ра) /М (HCl),
V(HCl)/22,4 = 1 1050 0,1/36,5.
Отсюда V
(HCl) = 64,44 л.
Найдем массу добавляемой воды:
m(H 2 O) = m (р-ра) – m (HСl),
m(H 2 O) = V (р-ра) (р-ра) – V (HCl)/22,4 М (HCl),
m(H 2 O) = 1 1050 – 64,44/22,4 36,5 = 945 г.
Ответ. 64,44 л HCl и 945 г воды.
Задача 5 (, № 4.34). Определите молярную концентрацию раствора с массовой долей гидроксида натрия 0,2 и плотностью 1,22 г/мл.
Дано:
0,2,
= 1220 г/л,
М
(NaOH) = 40 г/моль.
Найти:
Решение
m(р-ра) = с V М (NaOH),
m(р-ра) = с m (р-ра) М (NaOH)/.
Разделим обе части уравнения на m (р-ра) и подставим численные значения величин.
0,2 = c 40/1220.
Отсюда c = 6,1 моль/л.
Ответ. c = 6,1 моль/л.
Задача 6 (, № 4.30). Определите молярную концентрацию раствора, полученного при растворении сульфата натрия массой 42,6 г в воде массой 300 г, если плотность полученного раствора равна 1,12 г/мл.
Дано:
m(Na 2 SO 4) = 42,6 г,
m
(H 2 O) = 300 г,
= 1120 г/л,
M
(Na 2 SO 4) = 142 г/моль.
Найти:
Решение
m(Na 2 SO 4) = с V М (Na 2 SO 4).
500 (1 – 4,5/(4,5 + 100)) = m 1 (р-ра) (1 – 4,1/(4,1 + 100)).
Отсюда m 1 (р-ра) = 104,1/104,5 500 = 498,09 г,
m(NaF) = 500 – 498,09 = 1,91 г.
Ответ. m (NaF) = 1,91 г.
ЛИТЕРАТУРА
1. Хомченко Г.П., Хомченко И.Г.
Задачи по химии
для поступающих в вузы. М.: Новая волна, 2002.
2. Фельдман Ф.Г., Рудзитис Г.Е.
Химия-9. М.:
Просвещение, 1990, с. 166.
Задача 3.
5 г поваренной соли (NаС1) растворили в некотором количестве воды. В результате получили 4%-ный раствор NаС1 в воде. Определить массу использованной воды.
Дано:
масса поваренной соли: mNaСl) = 5 г;
массовая доля NаС1 в полученном растворе: NаС1) = 4%.
Найти:
массу использованной воды.
Решение:
Эту задачу можно решить двумя способами: с использованием формулы и пропорции.
I способ:


Подставляем данные из условия в первую формулу и находим массу раствора.

II способ:
Схематично алгоритм решения можно представить следующим образом:

Массовая доля воды в растворе равна: 100% - 4% = 96%.
Так как в растворе содержится 5 г соли, которые составляют 4%, можно составить пропорцию:
5 г составляют 4%
х г составляют 96%
Ответ: mводы = 120г.
Задача 4.
Некоторое количество чистой серной кислоты растворили в 70 г воды. В результате получили 10%-ный раствор Н 2 SO 4 . Определить массу использованной серной кислоты.
Дано:
масса воды: m(Н 2 О) = 70 г;
массовая доля Н 2 SО 4 в полученном растворе: Н 2 SО 4) = 10%.
Найти:
массу использованной серной кислоты.
Решение:
Здесь также возможно использование и соотношения, и пропорции.
I способ:

Подставим последнее выражение в соотношение для массовой доли:
![]()
Подставляем данные из условия в полученную формулу:
![]()
Получили одно уравнение с одним неизвестным Решая его, находим массу использованной серной кислоты:

II способ:
Схематично алгоритм решения можно представить следующим образом:

Применим предложенный алгоритм.
m(Н 2 О) = 100% – (Н 2 SО 4) = 100% – 10% = 90%
Составляем пропорцию:
70 г составляют 90%
х г составляют 10%
Ответ: m(H 2 SO 4) = 7,8 г.
Задача 5.
Некоторое количество сахара растворили в воде. В результате получили 2 л 30%-ного раствора (р = 1,127 г/мл). Определить массу растворенного сахара и объем использованной воды.
Дано:
объем раствора: V р-ра = 2 л;
массовая доля сахара в растворе: (сахара) = 30%;
плотность раствора: р
р-ра =1,127 г/мл
Найти:
массу растворенного сахара; объем использованной воды.
Решение:
Схематично алгоритм решения можно представить следующим образом.
Вычисление массы раствора определенной концентрации по массе растворенного вещества или растворителя.
Вычисление массы растворенного вещества или растворителя по массе раствора и его концентрации.
Вычисление массовой доли (в процентах) растворенного вещества.
Примеры типовых задач по расчету массовой доли (в процентах) растворенного вещества.
Процентная концентрация.
Массовая доля (в процентах) или процентная концентрация (ω) – показывает число грамм растворенного вещества, содержащееся в 100 граммах раствора.
Процентная концентрация или массовая доля есть отношение массы растворенного вещества к массе раствора.
ω = mраств. в-ва ·100% (1),
m р-ра
где ω – процентная концентрация (%),
m раств. в-ва – масса растворенного вещества (г),
m р-ра – масса раствора (г).
Массовая доля измеряется в долях единицы и используется в промежуточных расчетах. Если массовую долю умножить на 100 % получится процентная концентрация, которая используется, когда выдается конечный результат.
Масса раствора складывается из массы растворенного вещества и массы растворителя:
m р-ра = m р-ля + m раств. в-ва (2),
где m р-ра – масса раствора (г),
m р-ля – масса растворителя (г),
m раств. в-ва – масса растворенного вещества (г).
Например, если массовая доля растворенного вещества – серной кислоты в воде равна 0,05, то процентная концентрация составляет 5%. Это означает, что в растворе серной кислоты массой 100 г содержится серная кислота массой 5 г, а масса растворителя составляет 95г.
ПРИМЕР 1 . Вычислить процентное содержание кристаллогидрата и безводной соли, если в 450 г воды растворили 50 г CuSO 4 ·5H 2 O.
РЕШЕНИЕ :
1)Общая масса раствора составляет 450 + 50 = 500 г.
2)Процентное содержание кристаллогидрата находим по формуле (1):
Х = 50 100 / 500 = 10 %
3)Рассчитаем массу безводной соли CuSO 4 , содержащуюся в 50 г кристаллогидрата:
4)Рассчитаем молярную массу CuSO 4 ·5H 2 O и безводной CuSO 4
M CuSO4 · 5H2O = M Cu + M s +4M o + 5M H2O = 64 + 32 + 4·16 + 5·18 = 250 г/моль
М CuSO4 = M Cu + M s + 4M o = 64 + 32 + 4·16 = 160 г/моль
5)В 250 г CuSO 4 ·5H 2 O содержится 160 г CuSO 4
А в 50 г CuSO 4 ·5Н 2 О - Х г СuSO 4
Х = 50·160 / 250 = 32 г.
6)Процентное содержание безводной соли сульфата меди составит:
ω = 32·100 / 500 = 6,4 %
ОТВЕТ : ω СuSO4 · 5H2O = 10 %, ω CuSO4 = 6,4 %.
ПРИМЕР 2 . Сколько грамм соли и воды содержится в 800 г 12 %-ного раствора NaNO 3 ?
РЕШЕНИЕ:
1)Найдем массу растворенного вещества в 800 г 12 %-ного раствора NaNO 3:
800·12 /100 = 96 г
2)Масса растворителя составит: 800 –96 = 704 г.
ОТВЕТ: Масса HNO 3 = 96 г, масса H 2 O = 704 г.
ПРИМЕР 3 . Сколько грамм 3 %-ного раствора MgSO 4 можно приготовить из 100 г MgSO 4 7H 2 O?
РЕШЕНИЕ :
1)Рассчитаем молярную массу MgSO 4 ·7H 2 O иMgSO 4
M MgSO4 · 7H2O = 24 + 32 + 4·16 + 7·18 = 246 г/моль
M MgSO4 = 24 + 32 + 4·16 = 120 г/моль
2)В 246 г MgSO 4 ·7H 2 O содержится 120 г MgSO 4
В 100 г MgSO 4 ·7H 2 O содержится Х г MgSO 4
Х = 100·120 / 246 = 48,78 г
3)По условию задачи масса безводной соли составляет 3 %. Отсюда:
3 % массы раствора составляют 48,78 г
100 % массы раствора составляют Х г
Х = 100·48,78 / 3 = 1626 г
ОТВЕТ : масса приготовленного раствора будет составлять 1626 грамм.
ПРИМЕР 4. Сколько грамм НС1 следует растворить в 250 г воды для получения 10 %-ного раствора НС1?
РЕШЕНИЕ: 250 г воды составляют 100 – 10 =90 % массы раствора, тогда масса НС1 составляет 250·10 / 90 = 27,7 г НС1.
ОТВЕТ : Масса HCl составляет 27,7 г.