Хлорати натрію, кальцію і магнію все ще застосовують як неселективні гербіциди - для очищення залізничного полотна, проммайданчиків та ін; як дефоліанти при збиранні бавовни. Кислотне розкладання хлоратів використовують при отриманні двоокису хлору "на місці" (on-site) для відбілювання високоміцної целюлози.
K2На жаль, серйозним недоліком цього є низька якість побутових дезінфікуючих засобів і відбілювачів. Після пом'якшення політики "обов'язкової стандартизації" виробники засобів типу "білизна" почали використовувати власні технічні умовизнизивши вміст гіпохлориту в продукті зі стандартних 5% мас. до 3% і менше. Тепер для отримання тієї ж кількості хлорату з хорошим виходом потрібно не просто витратити набагато більше "білизни", але й видалити більшу частину води з розчину. Ймовірно, найбільш зручним може бути попереднє концентрування "білизни" частковим виморожуванням.
Професійні рідкі засоби для нейтралізації стоків на суднах містять до 40% натрію гіпохлориту.
K3Диспропорціонування гіпохлориту в хлорид та хлорат протікає з високою швидкістюпри pH
K4Дійсно, високоефективне джерело живлення значної потужності для електролізу – половина успіху справи та тема для особливої розмови.
Тут же хотілося б нагадати про необхідність дотримуватися правил електробезпеки.
Роботи, пов'язані з електролізом у значних масштабах, вважаються особливо небезпечними щодо ураження електричним струмом. Це з тим, що контакт шкіри експериментатора з провідним електролітом практично неминучий. Виділення газів на електродах викликає утворення корозійно-активних аерозолів електроліту, здатних осідати на компонентах електроустаткування, особливо при використанні примусового повітряного охолодження. Наслідки можуть бути дуже сумні - від корозії металевих частин та виходу блоку живлення з ладу до пробою ізоляції з потраплянням напруги на електролізер і всіма наслідками для експериментатора.
У жодному разі не слід встановлювати високовольтні частини установки у безпосередній близькості від електролізера. Усі компоненти джерела живлення слід розташовувати на достатній відстані від електролізера і таким чином, щоб повністю виключити як попадання на них електроліту у разі аварії електролізера, так і осадження струмопровідних аерозолів. При цьому сильноточні дроти від джерела до електролізера повинні мати достатній переріз, що відповідає струму процесу. Усі провідники (і їх з'єднання), безпосередньо пов'язані з електромережею, мають бути герметично ізольовані вологостійкою ізоляцією.
Обов'язковою є гальванічна розв'язка електролізера від електромережі. Звичайний трансформатор забезпечує адекватну ізоляцію, але категорично забороняється живлення електролізера безпосередньо від автотрансформаторів типу ЛАТР і т.п., так як при цьому електролізер може бути прямо з'єднаним із фазним проводом мережі. Однак ЛАТР (або побутовий автотрансформатор) можна використовувати для регулювання напруги на первинній обмотці основного трансформатора. Слід лише подбати про те, щоб потужність ЛАТРа була не меншою за потужність основного трансформатора.
При тривалій роботі установки захист електронних компонентів від перегріву та короткого замикання був би корисним. Для початку цілком можливо обмежитися установкою плавкого запобіжника в первинній обмотці трансформатора на струм, що відповідає його номінальній потужності. Живлення на електролізер також розумно подавати через відповідний плавкий запобіжник (краще регульований електромагнітний розчіплювач), маючи на увазі, що коротке замикання в електролізері цілком можливо.
Питання про необхідність заземлення установки в даному випадку не таке просте. Справа в тому, що у багатьох житлових приміщеннях заземлення спочатку відсутнє і його непросто влаштувати власними силами. У деяких випадках замість заземлення хитрі електрики організують занулення, з'єднуючи шину заземлення і нейтраль мережі безпосередньо у споживача. При цьому "заземлюваний" прилад виявляється безпосередньо підключений до струмоведущого контуру мережі. В наших умовах можна рекомендувати віддати пріоритет якісної ізоляції електролізера від мережі та експериментатора від усієї установки.
Правил безпеки не слід нехтувати ще й з тієї причини, що тривалий експеримент у аматорській лабораторії завжди привертає увагу інших людей, навички та поведінка яких експериментатор не може контролювати. Пам'ятайте про оточуючих та працюйте безпечно.
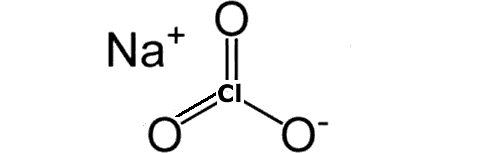
Cl(=O)=O]
Хлорат натрію- неорганічне з'єднання, сіль металу натрію і хлорнуватої кислоти з формулою NaClO 3 безбарвні кристали, добре розчинні у воді.
Отримання
- Хлорат натрію отримують дією хлорнуватої кислоти на карбонат натрію:
texvcне знайдено; Math/README - довідку з налаштування.): \mathsf(Na_2CO_3 + 2\ HClO_3\ \xrightarrow(\ )\ 2\ NaClO_3 + H_2O + CO_2\uparrow )
- або пропускаючи хлор через концентрований розчин гідроксид натрію при нагріванні:
texvcне знайдено; Math/README - довідку з налаштування.): \mathsf(6\ NaOH + 3\ Cl_2\ \xrightarrow(\ )\ NaClO_3 + 5\ NaCl + 3\ H_2O )
- Електроліз водних розчинів хлориду натрію:
texvcне знайдено; math/README - довідку з налаштування.): \mathsf(6\ NaCl + 3\ H_2O \ \xrightarrow(e^-)\ NaClO_3 + 5\ NaCl + 3\ H_2\uparrow )
Фізичні властивості
Хлорат натрію - безбарвні кристали кубічної сингонії. P 2 1 3 , параметри комірки a= 0,6568 нм, Z = 4.
При 230-255°З перетворюється на іншу фазу, при 255-260°З перетворюється на моноклинную фазу.
Хімічні властивості
- Диспропорціонує при нагріванні:
texvcне знайдено; math/README - довідку з налаштування.): \mathsf(10\ NaClO_3 \ \xrightarrow(390-520^oC)\ 6\ NaClO_4 + 4\ NaCl + 3\ O_2\uparrow )
- Хлорат натрію - сильний окислювач, у твердому стані в суміші з вуглецем, сіркою та іншими відновниками детонує при нагріванні чи ударі.
Застосування
- Хлорат натрію знайшов застосування у піротехніці.
Напишіть відгук про статтю "Хлорат натрію"
Література
- Хімічна енциклопедія/Редкол.: Кнунянц І.Л. та ін. – М.: Радянська енциклопедія, 1992. – Т. 3. – 639 с. - ISBN 5-82270-039-8.
- Довідник хіміка / Редкол.: Микільський Б.П. та ін. – 2-ге вид., испр. – М.-Л.: Хімія, 1966. – Т. 1. – 1072 с.
- Довідник хіміка / Редкол.: Микільський Б.П. та ін. - 3-тє вид., Випр. - Л.: Хімія, 1971. - Т. 2. - 1168 с.
- Ріпан Р., Четян І. Неорганічна хімія. Хімія металів – М.: Світ, 1971. – Т. 1. – 561 с.
| Хімічний посуд | Це незавершена стаття про неорганічну речовину. Ви можете допомогти проекту, доповнивши її. |
Уривок, що характеризує хлорат натрію
– Ну і де ж Ви «гуляли», мадонно Ізідоро? – награти милим голосом запитав мій мучитель.- Хотіла відвідати свою дочку, вашу святість. Але не змогла...
Мені було байдуже, що він думав, і чи зробила його моя «вилазка» злим. Душа моя витала далеко, в дивовижному Білому Місті, яке показував мені Істень, а все навколишнє здавалося далеким і убогим. Але Караффа надовго йти в мрії, на жаль, не давав... Тут же відчувши мій настрій, що змінився, «святість» запанікував.
- Чи впустили Вас у Метеору, мадонна Ізідора? - спокійніше спитав Караффа.
Я знала, що в душі він просто «горів», бажаючи швидше отримати відповідь, і вирішила її помучити, поки він мені не повідомить, де зараз мій батько.
– Хіба це має значення, ваша святість? Адже у Вас є мій батько, у якого Ви можете запитати все, на що природно, не відповім я. Чи Ви ще не встигли його достатньо допитати?
- Я не раджу Вам розмовляти зі мною подібним тоном, Ізідоро. Від того, як Ви маєте намір поводитися, багато в чому залежатиме його доля. Тому постарайтеся бути ввічливішими.
- А як би Ви поводилися, якби замість мого, тут опинився Ваш отець, святість?.. - намагаючись поміняти тему, що стала небезпечною, запитала я.
– Якби мій батько був ЄРЕТИКОМ, я спалив би його на багатті! - спокійно відповів Караффа.
Що за душа була у цієї «святої» людини?!.. І чи була вона в нього взагалі?.. Що ж тоді було говорити про чужих, якщо про свого рідного отця він міг відповісти таке?
— Так, я була в Метеорі, ваша святість, і дуже шкодую, що ніколи вже туди не потраплю... — щиро відповіла я.
— Невже Вас теж вигнали звідти, Ізидоро? – здивовано засміявся Караффа.
- Ні, Святість, мене запросили залишитися. Я пішла сама...
– Такого не може бути! Не існує такої людини, яка б не захотіла залишитися там, Ізидоро!
– Ну чому ж? А мій отець, святість?
– Я не вірю, що йому було дозволено. Я думаю, він мав піти. Просто його час, мабуть, закінчився. Або недостатньо сильним виявився Дар.
Мені здавалося, що він намагається, будь-що-будь, переконати себе в тому, у що йому дуже хотілося вірити.
– Не всі люди люблять тільки себе, чи знаєте… – сумно сказала я. – Є щось важливіше, ніж влада чи сила. Є ще на світі Любов...
Караффа відмахнувся від мене, як від настирливої мухи, ніби я щойно вимовила якусь повну нісенітницю...
- Кохання не керує, миром, Ізидоро, ну, а я бажаю ним керувати!
– Людина може все... доки не починає куштувати, ваша святість – не втримавшись, «вкусила» я.
І згадавши щось, про що обов'язково хотіла дізнатися, запитала:
– Скажіть, ваша святість, чи відома вам правда про Ісуса та Магдалина?
- Ви маєте на увазі те, що вони жили в Метеорі? – я кивнула. - Ну звичайно ж! Це було перше, про що я спитав у них!
– Як же таке можливо?!.. – приголомшено спитала я. - А про те, що вони не юдеї, Ви теж знали? - Карафа знову кивнув. - Але ж Ви не говорите ніде про це?.. Ніхто ж про це не знає! А як же ІСТИНА, Ваша святість?!..
— Не смішіть мене, Ізидоро!.. — щиро засміявся Караффа. - Ви справжня дитина! Кому потрібна Ваша «істина»?.. Натовпу, який її ніколи не шукав?! великого значення. Головне, щоб люди підкорялися. А що їм при цьому подається – це вже другорядне. ІСТИНА небезпечна, Ізідоро. Там, де відкривається Істина – з'являються сумніви, ну, а там де виникають сумніви – починається війна... Я веду СВОЮ війну, Ізидоро, і поки вона приносить мені справжнє задоволення! Світ завжди тримався на брехні, чи бачите... Головне, щоб ця брехня була досить цікавою, щоб змогла за собою вести «недалекі» уми... І повірте мені, Ізидоро, якщо при цьому Ви почнете доводити натовпу справжню Істину, яка спростовує їх «віру» невідомо у що, Вас і розірве на частини, той самий натовп...
- Невже ж так розумної людиниЯк ваша святість може влаштовувати таку самозраду?.. Ви ж спалюєте невинних, прикриваючись іменем цього ж оболганого, і такого ж невинного Бога? Як же Ви можете так безсовісно брехати, Ваша святість?!
Хлорати - солі однієї з кисневих кислотхлору, хлорнуватої кислоти - НСЮ3. Хлорновата кислота та її солі при нагріванні легко розкладаються з виділенням кисню, переходячи в солі хлорної кислоти - перхлорати. Всі хлорати більшою чи меншою мірою розчиняються у воді. Розчинність натрію хлорату у воді 50,2% при 20° і 69,7% при 100°. У водних розчинах хлорати надзвичайно стійкі навіть у присутності багатьох речовин, що окислюються.
Хлорат натрію може змінювати органолептичні якості води, надаючи їй гіркувато-солоного присмаку. Для встановлення порогових концентрацій досліджуваної солі у воді за смаком було здійснено за загальноприйнятою методикою кілька серій дослідів з водними розчинами хлорату натрію температури 20 і 60°. Результати дослідів представлені у табл. 1. […]
Хлорат натрію - це білий або жовтуватий кристалічний порошок, який хо-. рошо поглинає воду і розпадається при нагріванні до 300 ° С.
Хлорат натрію - малотоксичний для теплокровних, ЛД50 для щурів 1,2 г на 1 кг, проте за кордоном спостерігалися випадки смертельного отруєння людей при застосуванні хлорату натрію для боротьби з бур'янами. Діє на кров, викликає розпад червоних кров'яних тілець і переводить гемоглобін у метгемоглобін. Клініка отруєння: жовтяниця, блювота жовчю, шлунково-кишкові розлади, висипи на шкірі, лихоманка.
Хлорат натрію кристалічна речовина білого кольору, Ти 248 ° С, щільність 7,49 г / см3, розкладання починається при 265 ° С, добре розчинний у воді, аміаку, спирті, гліцерині, ацетоні, погано - в гексані та толуолі.
ГДК хлорату натрію у повітрі робочої зони 5 мг/м3.
Наші дослідження хлорату натрію включали гострі та підгострі токсикологічні експерименти, а також хронічний санітарно-токсикологічний експеримент.
Для вивчення впливу хлорату натрію на хід мінералізації органічного забруднення було поставлено кілька серій дослідів визначення динаміки БПК під впливом концентрації хлорату натрію 20 і 100 мг/л. Досліди проводилися як із 5-судинною, так і 20-з утковою інкубацією. Результати дослідів представлені у табл. 2. […]
У тварин, які отримували хлорат натрію в дозі 500 мг/кг, з боку морфологічного складукрові (кількість еритроцитів, лейкоцитів, ретикулоцитів) змін, які можна було б пов'язати з впливом хлорату натрію, не було виявлено, не було також відзначено змін у вмісті гемоглобіну, у співвідношенні білкових фракцій сироватки крові. Приріст ваги тварин був однаковим із приростом ваги контрольної групи.
Є також комбінований препарат, що містить хлорат натрію, буру та ТХА.
Гострі досліди щодо вивчення впливу хлорату натрію на організм теплокровних тварин при одноразовому пероральному введенні проводилися на білих, мишах, білих щурах та морських свинках. У дослідах використано 50 мишей, 24 щури та 30 морських свинок. Речовина вводилася тваринам у водному розчині, натще. Клінічна картина отруєння характеризувалася різкою задишкою, ціанозом кінчика носа та лапок, тонічними судомами під час агонії. Зазначені явища особливо різко були виражені у білих мишей, слабше – у щурів і дуже мало – у морських свинок. Тварини, які отримували менші дози, гинули за тих самих явищах, але пізніші терміни. Дані гострих дослідів були піддані статистичної обробкиза методом Міллера та Тейнтераг. Найбільш низька величина середньосмертельної дози спостерігалася у білих мишей (3600±705 мг/кг). У білих щурів і морських свинок вона була приблизно на одному рівні (відповідно 6500±417 мг/кг і 6100±383 мг/кг).
Продукт повинен складатися головним чином з хлорату натрію і являти собою білі або трохи забарвлені кристали, вільні від сторонніх домішок або введених модифікуючих агентів.
Результати гострих дослідів дозволяють віднести хлорат натрію до помірно токсичних речовин і підтверджують літературні дані, що отруєння хлоратами викликає метгемоглобінемію. При цьому виявилося, що найбільше високого рівняметгемоглобінемія досягає через 4-6 годин після отруєння.
У США поширені дефоліанти, що містять хлорат натрію. Для зниження вогненебезпечності хлорату натрію до препаратів додають поліборати або метаборати натрію. Найбільш широко застосовується хлорат-пентаборат натрію, що містить 40% хлорату натрію та 60% пентаборату натрію.
Визначення ґрунтується на реакції взаємодії хлорату натрію з бензидином хлоридом у сірчанокислому середовищі та наступному фотометричному вимірі. оптичної щільностіпофарбованого в жовтий колірпродукту реакції при 430 нм.
Гідразин виходить при взаємодії аміаку з хлоратом натрію.
У США найбільшого поширенняотримали сполуки хлорату натрію з боратами у співвідношеннях 1: 4.
Метод виборний. Супутні при отриманні хлориту натрію речовини (хлорат натрію та ін) не заважають визначенню.
Відсутність загибелі тварин протягом досвіду дозволяє віднести хлорат натрію до некумулятивних речовин.
Підсумовуючи результати підгострого досвіду, можна зробити висновок, що хлорат натрію при систематичному введенні здатний викликати підвищення рівня метгемоглобінемії, проте це підвищення незначне, хоча й є індивідуальні коливання. Підвищення рівня метгемоглобінемії під впливом високих доз (на рівні '/з ОЬбо) не супроводжується реакцією червоного кров'яного паростка або гемолізу. Не зазначено впливу хлорату і загальний стан організму, з його зростання.[ ...]
Здатність до пересування тканин рослини була встановлена у хлорату натрію і сульфамату амонію, хоча ці препарати токсичні і при внесенні їх в грунт.
Дослідження умовно-рефлекторної діяльності щурів під впливом хлорату натрію проводилося за методикою вироблення тимчасових зв'язків на фоні дії хлорату в камері Котляревського з інтегратором Лосєва. Для підбору груп, рівноцінних за особливостями їх нервової діяльності, перед затравкою у всіх щурів був вироблений умовний рефлекспозитивний звуковий сигнал (дзвінок). При цьому враховувалися швидкість появи та зміцнення умовної реакції, величина латентного періоду, величина умовної та безумовної реакції та відсоток випадання рефлексу.
Приклад 3. Вивчали окисну делігніфікацію осинової деревини хлоратом натрію в лабораторних умов. Деревину у вигляді стружки піддавали послідовно,-тельно окислювальної обробки розчином хлорату натрію в присутності соляної кислотита лужної екстракції розчином їдкого натру. Незалежні змінні: Х1 - концентрація натрію хлорату в розчині, г/л (Х!° = 50; = 6); Х2 - концентрація соляної кислоти у розчині, г/л (Х2° = 85; Аг = = 15); Хз - температура окисної обробки, ° С (Хз ° = 70, Аз = 5); Х4 - тривалість окислювальної обробки, хв (Х4 ° = 180; А4 = 30); Х5 - витрата №ОН на екстракцію у відсотках до вихідної деревини (Х5 ° = 2,5; А5 = = 0,5); Ха-температура екстракції, °С (Х6° = 92; Я6=8; Х7 - тривалість екстракції, хв (Х7° = 30; = 10). Як вихідний параметр у прикладі розглянуто вихід твердого залишку у відсотках від вихідної деревини. Змінні Х-, варіювали відповідно до плану ДФЕ ті-іа 27 3 (/а репліка ПФЕ) з генеруючими співвідношеннями: х5=х,хзх4;.х6 = х1х2хз; х7 = х.1х2х3х4.
Експериментальне обґрунтування гранично допустимої концентрації натрію хлорату у воді водойм. В. Т. Мйзаєв Експериментально-токсикологічні матеріали до вивчення комплексної діїхімічних агентів, що забруднюють одночасно воду та повітря. С. М. Павленко Порівняльна оцінка бромсульфалеїнової проби та інших функціональних тестів на печінку в умовах підгострої експериментальної гепатопатії. В. Є. Міклашевський, В. Н. Тугарінова, І. А. Акундинова, А. Н. Новікова, Г. А. Савоничева, Г. Г. Скобцова.
Підбиваючи підсумки санітарно-токсикологічним дослідженням, можна сказати, що хлорат натрію - речовина, що характеризується порівняно малою токсичністю і не має кумулятивних властивостей. Систематичне введення його у високих дозах (до 7з ОЬ50) не спричиняє загибелі тварин, а проявляється лише деяким підвищенням кількості метге-моглобіну. При цьому через добу після чергового введення речовини кількість метгемоглобіну приходить до норми. Останній фактсвідчить про те, що в даному випадку організм справляється з знешкодженням речовини фізіологічним механізмом деметгемоглобінізації (К. С. Косяков, 1939).
Різниця в отриманих величинах практичного значення не має, і концентрація хлорату Натрію 20 мг/л може бути визнана пороговою за впливом на органолептичні властивості води.
Форми застосування. Бура використовується як у чистому вигляді, так і в сумішах, особливо з хлоратом натрію, зменшуючи небезпеку займання останнього (наприклад, 9 частин бури плюс 1 частина хлорату для стерилізації ґрунту) (Grigsby В. H. et al, Mich. ]
Отримані дані говорять про те, що присмак інтенсивністю 1 бал повідомляється воді натрію хлоратом в концентрації 21,9 мг/л при температурі 20° і в концентрації 19 мг/л при температурі 60°.
Як загальновинищувальний гербіцид можна застосовувати солі хлорнуватої кислоти, зокрема хлорат натрію. Він застосовується у дозах 300–500 кг на 1 га при витраті води 1500–2000 л на 1 га. Однак застосування цього гербіциду обмежене через отруйність для людини та тварин, а також через вибухонебезпечність та здатність викликати корозію металів. Сам хлорат натрію безпечний для рослин, але в рослинних тканинах він перетворюється на токсичні сполуки – хлорити та гіпохлорити. Щоб уникнути загрози вибуху, застосовують хлорат кальцію та хлорат магнію - не вибухові речовини.
Деякий інтерес становить утворення двоокису хлору при відновленні соляною кислотою хлорату натрію (№С103), одержуваного електролізом кухонної солі при температурі 60°С.
Для досвіду було взято 20 білих щурів (10 піддослідних, 10 контрольних). Затравка проводилася з розрахунку 7з БЬбо (2200 мг/кг) хлорату натрію щодня протягом 30 днів. Згодом вміст метгемоглобіну визначалося через 4,6 годин і 1 добу після першої затравки, далі на 10-й, 20-й та 30-й дні досвіду. Визначення метгемоглобіну через добу після початку досліду проводилося перед введенням чергової дози хлорату натрію, наступні визначення – через 4-5 годин після чергового введення солі.
При проведенні підгострого токсикологічного експериментунами ставилося завдання, по-перше, вивчити здатність хлорату натрію до кумуляції в організмі, по-друге, з'ясувати особливості впливу цієї речовини при систематичному введенні в організм у порівнянні з гострим отруєнням та на основі цього вибрати тести, які було б доцільно випробувати в умовах хронічного санітарно-токсикологічного експерименту.
Спочатку для хімічної боротьби з бур'янами використовували неорганічні речовини: сульфат міді, сульфат заліза, арсеніт натрію, хлорат натрію, сірчану кислоту та ін.
На рис.5 наведено технологічну схему отримання СЮ2 за способом Метісона. Концентрована сірчана кислотаі розчин натрію хлорату подаються в первинний реактор. Суміш 80г із повітрям закачується в нижню частину реактора. Вміст реактора охолоджується до температури 40 °З допомогою водяної сорочки. Діоксид хлору віддмухується з розчину повітрям і прямує в абсорбер, де поглинається охолодженою водою. Розчин діоксиду хлору, що виходить, збирається в нижній частині абсорбера. Рідина з первинного реактора перетікає у вторинний реактор, де хлорат, що не прореагував, взаємодіє з 80г. Відпрацьована рідина з вторинного реактора продувається чистим повітрямдля відділення розчиненого СЮ2, що залишився, і відкачується в ємність для кислого реакторного залишку.
Форми застосування. Для знищення бур'янів деякі специфікації вимагають вмісту 98% ЫаС103, але у продажу є склади, в яких хлорат натрію з метою зменшення вогненебезпечності, змішаний з іншими солями, наприклад хлоридом натрію.
У цьому способі виключається утворення хлору як побічний продукт і істотно зменшується кількість утворює сульфату натрію в порівнянні з іншими способами, заснованими на використанні хлорату натрію.
Проведені в Приморському краї, Західному Уралі та інших районах країни випробування десикантів у посівах пшениці показали, що найефективнішими є хлорати магнію і кальцію. З великої кількостівипробуваних у Японії десикантів найбільш прийнятним виявився хлорат натрію. У багатьох країнах випробовується з цією метою реглон, який є швидкодіючим ефективним препаратом, проте у деяких випадках у зерні виявлялися невеликі залишки реглону (0,05-0,07 мг/кг). У борошні та висівках препарат не виявлявся.
Патоморфологічно було досліджено печінку, нирку та селезінку піддослідних тварин. При цьому лише у деяких тварин, що піддавалися затравки хлоратом натрію в дозі 500 мг/кг, у селезінці виявлено скупчення макрофагів, заповнених гранулами пігменту, що дає позитивну реакцію на залізо при фарбуванні Пірлсом (гемосидерин). У тварин, які отримували хлорат натрію в дозах 1 та 10 мг/кг, а також у контрольних тварин макрофаги, що містять гемосидерин, зустрічаються одиницями не у всіх полях зору. В інших органах будь-яких морфологічних змін, які можна було б віднести за рахунок впливу хлорату натрію, не було зазначено. Наведені дані дозволяють дійти невтішного висновку, що хлорат натрію при хронічному вплив у дозі 500 мг/кг здатний викликати помірний гемоліз.
Одержання двоокису хлору за способом Полотна, вперше освоєне в нашій країні на Братському ЛПК, відбувається в одному реакторі, який періодично подаються розчин сірчаної кислоти і хлорат натрію з розріджувача. Використання хлорату вбирається у 88- 89%.[ ...]
Електрохімічне одержання білил легше здійснити, застосовуючи ванни з діафрагмами. У таких ваннах в анодному просторі виходить розчин солі свинцю, а в катодному – розчин їдкого натру. В спеціальному апараті аноліт з католітом змішують при пропущенні вуглекислоти. При цьому осаджуються свинцеві білила та регенерується хлорат натрію.
Склади поділяють на категорії відповідно до пожежної небезпеки матеріалів, що знаходяться в них. Так, до категорії А належать: склади ЛЗР, скипидару, одоранту сульфану, розчинників для лаків, спиртових лаків та нітролаків. Склади рідкого хлорату натрію та кисню відносяться до категорії Б. Склади тріски, тростини, соломи, макулатури, ганчір'я та інших горючих матеріалів відносяться до категорії В, а склади негорючих матеріалів – до категорії Д.
Також зареєстрований у:США
Основні відомості:
| Широкий спектр, системний, який переміщає до всіх частин бур'янів. Phytoxic до всіх підприємств. |
| Білий порошок |
Випуск:
натрію хлорат: поведінка у навколишньому середовищі
| Показник | Значення | Пояснення | ||
| Розчинність у воді при 20 o C (мг/л) | 650000 A5 Високий||||
| Розчинність в органічних розчинниках при 20 o C (мг/л) | Insoluble A5 - Most organic Розчинників -||||
| Температура плавлення (C) | 255 A5 -||||
| Температура кипіння (C) | Розкладається до кипіння A4 -||||
| Температура розкладання (C) | 260 A3 -||||
| Температура спалаху (C) | Вогненебезпечність не висока A5 -||||
| Коефіцієнт розподілу у системі октанол/вода при pH 7, 20 o C | P: 1.26 X 10 -03 Розраховується -||||
| Питома густина (г/мл) / Питома вага | 2.499 L3 -||||
| Константа дисоціації (pKa) при 25 o C | -2 A4 -||||
| Примітка: Very Сильна кислота | ||||
| Тиск парів при 25 o C (МПа) | 5.2 X 10-06 A2 Intermediate state||||
| Константа закону Генрі при 25 o C (Па*м3/моль) | 5.2 X 10 -09 A3 - Не летючий||||
| Константа закону Генрі при 20 o C (безрозмірна) | 3.50 X 10 -16 Розраховується Не летюч||||
| Період розпаду у ґрунті (дні) | ДТ50 (типовий) 200 F3 Стійкий||||
| За даними лабораторних дослідженьєвросоюзу ДТ50 складає 46.7-314.6 днів | ||||
| Водний фотоліз ДТ50 (дні) при pH 7 | Значення: Стабільний A5 Стабільний||||
| - | ||||
| Водний гідроліз ДТ50 (дні) при 20 o C та pH 7 | Значення: Стабільний A5 Дуже стійкий||||
| Not senstive to pH | ||||
| Водне осадження ДТ50 (дні) | - - -||||
| Тільки водна фаза ДТ50 (дні) | - - -||||
| Індекс потенційного вимивання GUS | 6.90 Розраховується Висока вилуговуваність||||
| Індекс зростання концентрації у ґрунтових водах SCI (мкг/л) при дозі внесення 1 кг/га (л/га) | Значення: 4.51 X 10 +01 Розраховується -||||
| - | ||||
| Potential for particle bound transport index | - розраховується середній||||
| Koc - коефіцієнт розподілу органічного вуглецю (мл/г) | 10 F3 Very mobile||||
| pH стійкість: | ||||
| Примітка: | ||||
| Ізотерма адсорбції Фрейндліха | Kf: -- | -|||
| - | ||||
| Максимальне УФ-поглинання (л/(моль*см)) | - - -||||
натрію хлорат: екотоксичність
| Показник | Значення | Джерело / Якісні показники / Інша інформація | Пояснення | |
| Коефіцієнт біоконцентрації | BCF: -- | -|||
| Потенціал біоакумуляції | - розраховується Низький||||
| ЛД50 (мг/кг) | > 5000 A5 Пацюк Низький||||
| Ссавці - Короткоперіодний харчовий NOEL | (мг/кг): -- | -|||
| Птахи - Гостра ЛД50 (мг/кг) | 2510 A5 Качка кряква Низький||||
| Птахи - Гостра токсичність (СК50/ЛД50) | - - -||||
| Риби - Гостра 96 годинна СК50 (мг/л) | 10000 G2 Низький||||
| Риби - Хронічна 21 денна NOEC (мг/л) | 500 A5 Даніо Реріо -||||
| Водні безхребетні - Гостра 48 годинна ЕК50 (мг/л) | 919.3 A5 Низький||||
| Водні безхребетні - Хронічна 21 денна NOEC (мг/л) | 500 A5 Дафнія магна (Дафнія велика, Блоха водяна велика) -||||
| Водні ракоподібні - Гостра 96 годинна СК50 (мг/л) | - - -||||
| Донні мікроорганізми - Гостра 96 годинна СК50 (мг/л) | - - -||||
| NOEC, static, Вода (мг/л) | - - -||||
| Донні мікроорганізми - Хронічна 28 денна NOEC, Осадова порода (мг/кг) | - - -||||
| Водні рослини - Гостра 7 денна ЕК50, біомаса (мг/л) | 134 A5 Ряска малаНизький||||
| Водорості - Гостра 72 годинна ЕК50, зріст (мг/л) | 1595 A5 Зелені водорості (Scenedesmus subspicatus)Низький||||
| Водорості - Хронічна 96 годинна NOEC, зростання (мг/л) | - - -||||
| Бджоли - Гостра 48 годинна ЛД50 (мкг/особина) | > 75 A5 Орально Помірно||||
| Грунтові черв'яки - Гостра 14-денна СК50 (мг/кг) | > 750 A5 Помірно||||
| Грунтові черв'яки - Хронічна 14-денна максимально недіюча концентрація речовини, розмноження (мг/кг) | - - -||||
| Інші Членистоногі (1) | LR50 (р/га): 84.4 A5 Хижий кліщПомірно небезпечний at 1 кг/га||||
| Інші Членистоногі (2) | LR50 (р/га): 250.6 A5 НаїзникПомірно небезпечний at 1 кг/га||||
| Ґрунтові мікроорганізми | Мінералізація азоту: -47Дія (%)||||
| Наявні дані щодо мезоміру (мезокосму) | NOEAEC мг/л: - - -||||
натрію хлорат: здоров'я людини
Основні показники:
| Показник | Значення | Джерело / Якісні показники / Інша інформація | Пояснення | |
| Ссавці - Гостра оральна ЛД50 (мг/кг) | > 5000 A5 Пацюк Низький||||
| Ссавці - Шкірна ЛД50 (мг/кг маси тіла) | > 2000 A5 Пацюк -||||
| Ссавці - Інгаляційна СК50 (мг/л) | > 3.9 A5 Пацюк -||||
| ДСД – допустима добова доза (мг/кг маси тіла на день) | Не визначено A5 -||||
| ARfD – середньодобова норма споживання (мг/кг маси тіла на день) | Не визначено A5 -||||
| AOEL – допустимий рівень системного впливу на оператора | 0.35 A5 Пацюк, SF=200 -||||
| Поглинання шкірою (%) | - - -||||
| Директива щодо небезпечних речовин 76/464/ЄС | - - -||||
| Види обмежень | - - -||||
| за категорією | Загальні:||||
| , | ||||
| Приклади Європейських | ||||
Винахід відноситься до галузі виробництва хлорату натрію, що широко використовується в різних областяхпромисловості. Електроліз розчину хлориду натрію здійснюють спочатку у хлорних діафрагмових електролізерах. Хлоридно-лужні розчини, що утворюються, і електролітичний хлор-газ змішують з отриманням хлорид-хлоратного розчину. Отриманий розчин змішують з маточником стадії кристалізації і направляють на бездіафрагмовий електроліз з наступною випаровуванням хлорид-хлоратних розчинів та кристалізацією хлорату натрію. Продукти діафрагмового електролізу можуть частково відводитися для отримання з хлоргазу соляної кислоти для підкислення хлоратного електролізу та використання хлоридно-лужних розчинів для зрошення санітарних колон. Технічний результат- зниження витрати електроенергії та можливість організації автономного виробництва. 1 з.п.ф-ли.
Винахід відноситься до галузі виробництва хлорату натрію, що широко використовується в різних галузях промисловості. Світове виробництво хлорату натрію сягає кількох сотень тисяч тонн на рік. Хлорат натрію застосовується для отримання двоокису хлору (відбілювач), хлорату калію (бертолетова сіль), хлоратів кальцію та магнію (дефоліанти), перхлорату натрію (напівпродукт для виробництва твердого ракетного палива), в металургії при переробці уранової рудиі т.д. Відомий спосіб отримання хлорату натрію хімічним способом, при якому розчини натрію гідроксиду піддаються хлоруванню з отриманням хлорату натрію. За своїми техніко-економічними показниками хімічний спосібне витримує конкуренції з електрохімічним, тому в даний час практично не використовується (Л.М.Якименко "Виробництво хлору, каустичної соди та неорганічних хлорпродуктів", Москва, з-під "Хімія", 1974, с. 366). Відомий спосіб отримання хлорату натрію шляхом електролізу розчину хлориду натрію в каскаді бездіафрагмових електролізерів з отриманням хлорид-хлоратних розчинів, з яких кристалічний хлорат натрію виділяється методом випарювання та кристалізації (K.Wihner, L.Kuchler "Chemische Technologie", Bd. Technologie", s.729, Munchen, 1970; Л.М.Якименко, Т. А.Серишев "Електрохімічний синтез неорганічних сполук, Москва, в " Хімія " , 1984, стор 35-70). Цей спосіб найбільш близький до запропонованого винаходу. Основна технологічна стадія, бездіафрагмовий електроліз розчинів натрію хлориду, протікає з виходом по струму 85-87%. Процес ведуть на окисно-рутенієвих анодах при температурі 70-80 o C, pH 7 при постійному підкисленні електроліту 10%-ним розчином соляної кислоти. Перед подачею на стадію виділення твердого продукту електроліт підлужують до надлишку лугу 1 г/л з додаванням відновника для руйнування корозійно-активного натрію гіпохлориту, завжди присутнього в продуктах електролізу. Побічним анодним процесом при електролізі хлоридних розчинів є виділення Cl 2 що не тільки знижує вихід по струму, але і вимагає очищення електролізних газів у санітарних колонах, зрошуваних розчином лугу. Здійснення процесу тому пов'язане із суттєвою витратою соляної кислоти та лугу: на 1 т хлорату натрію витрачається ~120 кг 31% соляної кислоти та 44 кг 100% NaOH. З цієї ж причини хлоратні виробництва організуються там, де є хлорний електроліз, що постачає каустичну соду і електролітичний хлор і водень для синтезу соляної кислоти, тоді як часто є потреба в автономному виробництві натрію хлорату в точках, віддалених від хлорних виробництв. Але й там, де хлорне виробництво та хлоратний електроліз розташовані поруч, при зупинках та відключеннях хлорного електролізу з тих чи інших причин відбувається і вимушене відключення хлоратного електролізу. Таким чином, відомий спосіб має суттєві недоліки: великі енергетичні витрати (не дуже високий вихід по струму ) та неможливість організації автономного виробництва. Завданням пропонованого винаходу є створення способу отримання хлорату натрію електролізом розчинів натрію хлориду з зниженими енергетичними витратами. Поставлене завдання вирішується запропонованим способом, при якому спочатку хлорид натрію переробляється в хлорних діафрагмових електролізерах з отриманням газоподібного хлоргазу та електролітичних лугів складу 120-140 г/л NaOH і 160-180 г/л NaCl, які потім повних обсягах або частково піддають взаємодії між собою з отриманням хлорид-хлоратного розчину 50-60 г/л NaClO 3 і 250-270 г/л NaCl, що спрямовується на бездіафрагмовий електроліз. Процес хлоратного бездіафрагмового електролізу здійснюють при підкисленні соляною кислотою. Отриманий при цьому хлоратний розчин, що містить хлорид натрію, направляють на стадії випарювання, а потім кристалізації хлорату. Маточник зі стадії кристалізації разом із продуктами взаємодії лугу та хлору від діафрагмового електролізу направляють на бездіафрагмовий хлоратний електроліз. Перед подачею на стадію виділення твердого продукту електроліт підлужують до надлишку лугу 1 г/л з додаванням відновника для руйнування натрію гіпохлориту. При частковому відведенні продуктів електролізу хлорних діафрагмових електролізерів хлор використовується для отримання соляної кислоти, що використовується для підкислення хлоратного електролізу, а луг використовується для зрошення санітарних колон при очищенні електролізних газів. При такій схемі 30-35 г натрію хлориду з 300-310 г, що містяться в кожному літрі вихідного розчину, переробляється в умовах хлорного електролізу. Така схема зумовлює зниження енергетичних витрат, т.к. вихід по струму хлорного електролізу вищий, а напруга на електролізерах нижче, ніж у хлоратному електролізі, і при проведенні частково електрохімічного окислення хлориду натрію в хлорат в умовах хлорного електролізу покращуються показники всього процесу в цілому. Крім того, при використанні описаної схеми знижуються витрати на охолодження електролізу, тому що хлорні електролізери охолодження не потребують. Зауважимо, що більш глибоке спрацьовування хлориду в умовах хлорного електролізу, ніж обумовлено (близько 10%), призводить до неможливості збалансувати технологічну схему за хлоридами, хлоратами та водою і тому не має сенсу. В рамках запропонованої схеми можливе отримання додаткового ефекту при подачі на хлоратний електроліз розчинів зі збільшеною за NaClO 3 концентрацією, одержуваних з більш концентрованих NaOH, ніж діафрагмові лугу, розчинів лугу, для хлорування яких може утилізуватися хлор, що містить інерти. Електролуги хлорного електролізу можуть змішуватися з хлор-газом не повністю, а частково. При цьому частина електролуг діафрагмового електролізу, не спрямована на хлорування, відводиться для використання в санітарних колонах, а еквівалентна частина електролітичного хлору може бути використана для синтезу соляної кислоти. Напрямок електролугів з діафрагмових електролізерів у санітарні колони, а електролітичного хлоргазу на отримання соляної кислоти вирішує проблему автономного хлоратного виробництва, оскільки постачання лугу та кислоти з боку вже не буде потрібно. Частка хлориду натрію, що переробляється в хлорних електролізерах, визначається тим, чи будуть отримані продукти використовуватися тільки для отримання в результаті їх взаємодії хлорид-хлоратних лугів, після змішування з маточником зі стадії кристалізації на бездіафрагмовий електроліз, або електролуга хлорних електролізерів будуть використовуватися тільки для а електролітичний хлор – для синтезу хлорної кислоти для підкислення у схемі хлоратного електролізу, або частина продуктів буде використовуватися в одному напрямку, а частина в іншому. Перевагами запропонованого способу є: 1) зниження енергетичних витрат за рахунок проведення початкової стадії електролізу з великим виходом по струму і при меншій напрузі, ніж у звичайному хлоратному електролізі: вихід по струму 92-94% і напруга 3,2 В хлорному електролізі проти 85 -90% і 3,4 і вище відповідно в хлоратному; 2) можливість отримання одночасно з основним продуктом - хлоратом натрію - лужних розчинів, необхідних технологічної схемидля підлужування та зрошення санітарних колон; 3) можливість використання хлору, одержуваного в хлорних електролізерах, для отримання дома соляної кислоти для підкислення хлоратного електролізу. Приклад У дослідному електролізері ведуть хлорний діафрагмовий електроліз розчину хлориду натрію концентрації 300 г/л на окисно-рутенієвих анодах при щільності струму 1000 А/м 2 і температурі 90 o C. Отримані електролітичні лугу, що містять 140 г/л NaOH NaCl, змішують з анодним хлор-газом і одержують хлорид-хлоратний розчин складу 270 г/л NaCl і 50 г/л NaClO 3 . Цей розчин подають далі на бездіафрагмовий хлоратний електроліз, що проводиться в каскаді з 4 електролізерів з окисно-рутенієвими анодами при щільності струму 1000 А/м 2 і температурі 80 o C з отриманням кінцевого розчину наступного складу: 105 г/л NaCl і 3 NaClO 3 . Таким чином, з одного 1 л вихідного хлоридного розчину напрацьовується з урахуванням 10% зменшення об'єму розчину за рахунок винесення парів води з електролізними газами та випаровування 355 г хлорату натрію, з яких 50 г (14,1%) вийшло після змішування продуктів хлорного діафрагмового електролізу , а 305 (85,9%) напрацьовано у процесі хлоратного електролізу Напруга на хлорному електролізері була 3,3 при виході по струму 93%. Середня напруга на хлоратному електролізері склала 3,4 при виході по струму 85%. Питома витрата електроенергії W (кВтч/т), обчислена за даними експерименту за формулою W = 1000E/mBT, де E - напруга на комірці (B); m – електрохімічний еквівалент (г/Ач); BT - вихід струму в частках одиниці,
становив для хлорного електролізу 2517 кВтг/т, а хлоратного - 5996 кВтг/т, що з урахуванням частки хлорату, виробленого результаті змішування продуктів хлорного електролізу, дає 5404,9 кВтг/т. Витрата електроенергії без застосування хлорного електролізера склала на цій же установці 6150 кВтг/т. Таким чином, зниження енергетичних витрат становило 12,1%.
Формула винаходу
1. Спосіб отримання хлорату натрію шляхом електролізу розчину хлориду натрію з подальшою випаровуванням хлорид-хлоратних і електролітичного хлоргазу, які змішують з отриманням хлорид-хлоратного розчину і направляють після змішування з маточником стадії кристалізації на бездіафрагмовий електроліз. 2. Спосіб за п.1, який відрізняється тим, що продукти діафрагмового електролізу відводять частково для отримання з хлор-газу соляної кислоти для підкислення хлоратного електролізу та використання хлоридно-лужних розчинів для зрошення санітарних колон.