Халогени– Елементи от VII група – флуор, хлор, бром, йод, астат (астатът е малко проучен поради радиоактивността си). Халогените са отделни неметали. Само йодът в редки случаи проявява някои свойства, подобни на металите.
В невъзбудено състояние халогенните атоми имат обща електронна конфигурация: ns2np5. Това означава, че халогените имат 7 валентни електрона, с изключение на флуора.
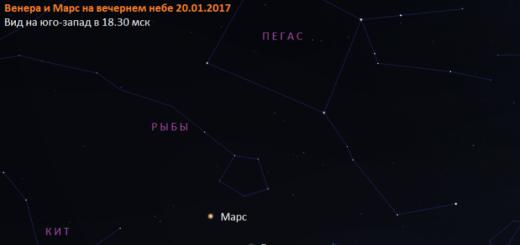
Физични свойства на халогените: F2 – безцветен, трудно втечняващ се газ; Cl2 е жълто-зелен, лесно втечняващ се газ с остър задушлив мирис; Br2 – червено-кафява течност; I2 е виолетово кристално вещество.

Водните разтвори на халогеноводородите образуват киселини. HF – флуороводород (флуорид); HCl – солна (сол); НBr— бромоводород; HI – йодоводород. Силата на киселините намалява отгоре надолу. Флуороводородната киселина е най-слабата в серията халогенирани киселини, а йодоводородната киселина е най-силната. Това се обяснява с факта, че енергията на свързване на Hg намалява отгоре. Силата на NG молекулата намалява в същата посока, което е свързано с увеличаване на междуядреното разстояние. Разтворимостта на слабо разтворимите соли във вода също намалява:
Отляво надясно разтворимостта на халогенидите намалява. AgF е силно разтворим във вода. Всички халогени в свободно състояние са окислители. Силата им като окислители намалява от флуор към йод. В кристално, течно и газообразно състояние всички халогени съществуват под формата на отделни молекули. Атомните радиуси се увеличават в същата посока, което води до повишаване на точките на топене и кипене. Флуорът се разпада на атоми по-добре от йода. Електродните потенциали намаляват при движение надолу по халогенната подгрупа. Флуорът има най-висок електроден потенциал. Флуорът е най-силният окислител. Всеки по-висок свободен халоген ще измести по-ниския, който е в състояние на отрицателен еднократно зареден йон в разтвор.
20. Хлор. Хлороводород и солна киселина
Хлор (Cl) –стои в 3-ти период, в VII група на главната подгрупа на периодичната система, пореден номер 17, атомна маса 35,453; се отнася до халогени.
Физични свойства:жълто-зелен газ с остра миризма. Плътност 3.214 g/l; точка на топене -101 °C; точка на кипене -33,97 °C, при нормална температура лесно се втечнява под налягане от 0,6 MPa. Разтваряйки се във вода, образува жълтеникава хлорна вода. Той е силно разтворим в органични разтворители, особено хексан (C6H14) и въглероден тетрахлорид.
Химични свойства на хлора:електронна конфигурация: 1s22s22p63s22p5. Във външното ниво има 7 електрона. За да завършите нивото, имате нужда от 1 електрон, който хлорът приема, проявявайки степен на окисление -1. Съществуват и положителни степени на окисление на хлора до + 7. Известни са следните хлорни оксиди: Cl2O, ClO2, Cl2O6 и Cl2O7. Всички те са нестабилни. Хлорът е силен окислител. Реагира директно с метали и неметали:
Реагира с водород. При нормални условия реакцията протича бавно, при силно нагряване или запалване - с експлозия, по верижен механизъм:
![]()
Хлорът взаимодейства с алкални разтвори, образувайки соли - хипохлорити и хлориди:
При преминаване на хлор в алкален разтвор се образува смес от хлоридни и хипохлоритни разтвори:
Хлорът е редуциращ агент: Cl2 + 3F2 = 2ClF3.
Взаимодействие с вода:
Хлорът не реагира директно с въглерод, азот и кислород.
Касова бележка: 2NaCl + F2 = 2NaF + Cl2.
Електролиза: 2NaCl + 2H2O = Cl2 + H2 + 2NaOH.
Намиране в природата:съдържа се в следните минерали: халит (каменна сол), силвит, бишофит; морската вода съдържа хлориди на натрий, калий, магнезий и други елементи.
Хлороводород HCl. Физични свойства:безцветен газ, по-тежък от въздуха, силно разтворим във вода, за да се образува на солна киселина.
Касова бележка:в лабораторията:
В промишлеността: водородът се изгаря в поток от хлор. След това хлороводородът се разтваря във вода, за да се образува солна киселина (виж по-горе).
Химични свойства: солната киселина е силна, едноосновна, взаимодейства с метали в серията на напрежение до водород: Zn + 2HCl = ZnCl2 + H2.
Като редуциращ агент реагира с оксиди и хидроксиди на много метали.
ОПРЕДЕЛЕНИЕ
Халогени– елементи от VII А група – флуор (F), хлор (Cl), бром (Br) и йод (I).
Електронна конфигурация на външното енергийно ниво на халогените ns 2 np 5. Тъй като на халогените им липсва само един електрон преди завършване на енергийното ниво, в ORR те най-често проявяват свойствата на окислители. Степени на окисление на халогени: от "-1" до "+7". Единственият елемент от халогенната група, флуорът, показва само една степен на окисление „-1“ и е най-електроотрицателният елемент. Халогенните молекули са двуатомни: F 2, Cl 2, Br 2, I 2.
Химични свойства на халогените
С увеличаване на заряда на ядрото на атом на химичен елемент, т.е. при преминаване от флуор към йод, окислителната способност на халогените намалява, което се потвърждава от способността за изместване на по-ниски халогени с по-високи от халогеноводородни киселини и техните соли:
Br2 + 2HI = I2 + 2HBr;
Cl 2 + 2KBr = Br 2 + 2KCl.
Флуорът има най-голяма химическа активност. Мнозинство химически елементидори при стайна температура взаимодейства с флуор, освобождавайки голям бройтоплина. Дори водата гори във флуор:
2H 2 O + 2F 2 = 4HF + O 2.
Свободният хлор е по-малко реактивен от флуора. Не реагира директно с кислород, азот и благородни газове. Той взаимодейства с всички други вещества като флуор:
2Fe + Cl 2 = 2FeCl 3;
2P + 5Cl 2 = 2PCl 5.
Когато хлорът взаимодейства с водата на студено, възниква обратима реакция:
Cl 2 + H 2 O↔HCl +HClO.
Сместа от реакционни продукти се нарича хлорна вода.
Когато хлорът взаимодейства с алкали на студено, се образуват смеси от хлориди и хипохлорити:
Cl 2 + Ca(OH) 2 = Ca(Cl)OCl + H 2 O.
Когато хлорът се разтвори в горещ алкален разтвор, възниква следната реакция:
3Cl 2 + 6KOH = 5KCl + KClO 3 + 3H 2 O.
Бромът, подобно на хлора, се разтваря във вода и, частично реагирайки с него, образува така наречената „бромна вода“, докато йодът е практически неразтворим във вода.
Йодът се различава значително по химическа активност от другите халогени. Той не реагира с повечето неметали и реагира бавно с металите само при нагряване. Взаимодействието на йод с водород става само при силно нагряване, реакцията е ендотермична и силно обратима:
H 2 + I 2 = 2HI - 53 kJ.
Физични свойства на халогените
На бр. флуорът е светложълт газ с остра миризма. Отровни. Хлорът е светлозелен газ, също като флуора, има остра миризма. Силно отровен. При повишено налягане и стайна температура лесно преминава в течно състояние. Бромът е тежка течност с червено-кафяв цвят с характерна неприятна остра миризма. Течният бром, както и неговите пари, са силно токсични. Бромът е слабо разтворим във вода и добре в неполярни разтворители. Йодът е тъмно сиво твърдо вещество с метален блясък. Йодните пари имат лилаво. Йодът лесно сублимира, т.е. отива в газообразно състояниеот твърдо, заобикаляйки течното състояние.
Производство на халогени
Халогените могат да бъдат получени чрез електролиза на разтвори или стопилки на халогениди:
MgCl 2 = Mg + Cl 2 (топилка).
Най-често халогените се получават чрез реакция на окисление на халогеноводородни киселини:
MnO 2 + 4HCl = MnCl 2 + Cl 2 + 2H 2 O;
K 2 Cr 2 O 7 + 14 HCl \u003d 3Cl 2 + 2KCl + 2CrCl 3 + 7H 2 O;
2KMnO4 +16HCl = 2MnCl2 +5Cl2 +8H2O +2KCl.
Приложение на халогени
Халогените се използват като суровини за производството на различни продукти. По този начин флуорът и хлорът се използват за синтеза на различни полимерни материали; хлорът също е суровина при производството на солна киселина. Намерени са бром и йод широко приложениев медицината бромът се използва и от производството на бои и лакове.
Примери за решаване на проблеми
ПРИМЕР 1
| Упражнение | Изчислете обема на хлора (№), който реагира с калиев йодид, ако се образува йод с тегло 508 g | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Решение | Нека напишем уравнението за реакцията между хлор и калиев йодид: Cl 2 + 2KI = I 2 + 2KCl Моларна маса на йод, изчислена с помощта на таблицата на химичните елементи от D.I. Менделеев, равно на – 254 g/mol. Нека намерим количеството образуван йод: v(I 2) = m(I 2)/M(I 2) В, открит през 1940 г
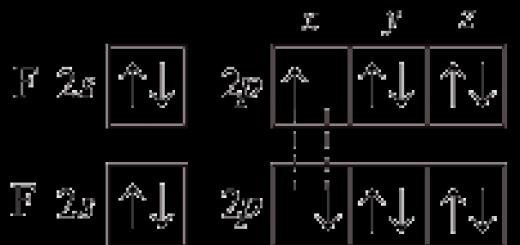
Разпределението на електронните орбитали във външния електронен слой на всички халогени е от един и същи тип
Те имат много общо в структурата на атомите и молекулите. Завършват строителството Р-обвивки на външния слой, така че всички те принадлежат към броя на p-елементите. На външния електронен слой на халогенните атоми му липсва един електрон за завършване, така че електроотрицателността на тези елементи е изразена и в редокс реакциите те се държат главно като окислители. ■ 1. Как се променя атомният радиус в зависимост от увеличаването на заряда на атомното ядро?
Физични свойства на халогенитеВсички свойства на халогените, както физични, така и химични, зависят от структурата на атомите на елемента. Тези свойства на различните халогени са до голяма степен сходни, но в същото време всеки халоген има редица характеристики. ■ 7. Как се променя интензивността на цвета на халогените с увеличаване на ядрените заряди?
10. Съставете и попълнете таблицата „Физични свойства на халогените“ по следния модел:
Физиологичен ефект на халогенитеВсички те са отровни по своите физиологични ефекти. Флуорът е особено токсичен: при вдишване в малки количества причинява белодробен оток, в големи количества причинява разрушаване на белодробната тъкан и смърт. йодНай-малко токсичният от всички халогени. Вдишването на йодни пари, когато се нагрява, може да причини отравяне, но рядко се работи с парообразен йод, например, когато се пречиства чрез сублимация. Кристалният йод не трябва да се взема с ръце, тъй като при контакт с кожата се появяват характерни жълти петна. Всички работи с халогени трябва да се извършват в аспиратор. Запишете в тетрадката си мерките за безопасност при работа с халогени и първа помощ при отравяне. Химични свойства на халогените
По естеството на техните химични свойства, както беше отбелязано по-горе, всички халогени са типични неметали със значителна електроотрицателност. Най-електроотрицателният елемент с най-голяма неметална активност е флуорът, най-малко активният е йодът. Ориз. 21.Изгаряне на водород в хлор. 1- хлор 2- Взаимодействие на халогени с прости вещества. Можете да проследите намаляването на химическата активност от флуор към хлор, като използвате примери за различни реакции. Особено интересно е взаимодействието на различни халогени с водорода. Техните условия на реакция са различни. Флуоридът е най-трайното съединение сред водородните халиди. С водорода бромът образува бромоводород.
Халогените също проявяват окислителни свойства при взаимодействие с метали, което обикновено е много активно. Ориз. 22. Например. Сu + Сl2 = СuСl2 Тук, в реакция с хлор, той проявява степен на окисление, равна на +3 - Fe +3 и равна на +2 - Cu +2. Във всички горепосочени случаи хлорът се държи като. Химия на елементите Неметали от VIIA подгрупа Елементите от VIIA подгрупа са типични неметали с високо електроотрицателност, те имат име на група - „халогени“. Основни въпроси, засегнати в лекцията Обща характеристика на неметалите от VIIA подгрупа. Електронна структура, най-важните характеристики на атомите. Най-характерните сте- наказания за окисление. Характеристики на химията на халогените. Прости вещества. Естествени съединения. Халогенни съединения Халоводородни киселини и техните соли. Сол и флуороводородна киселина слотове, разписка и приложение. Халогенни комплекси. Двоичен кислородни съединенияхалогени. Нестабилност прибл. Редокс свойства на прости вещества и ко- единства. Реакции на диспропорционалност. Диаграми на Латимер.
Химия на елементите от VIIA подгрупа основни характеристики
VIIA-група се образува от р-елементи: флуор F, хлор Cl, бром Br, йод I и астат At. Общата формула за валентните електрони е ns 2 np 5. Всички елементи от група VIIA са типични неметали.
за образуване на стабилна обвивка от осем електрона кутии, затова иматима силна тенденция към добавяне на електрон. Всички елементи лесно се образуват прости еднозарядни ny аниони G – . Под формата на прости аниони елементи от група VIIA се намират в естествена вода и в кристали на естествени соли, например халит NaCl, силвит KCl, флуорит CaF2. Общо групово име на елементи VIIA- група „халогени“, т.е. „раждащи соли“, се дължи на факта, че повечето от техните съединения с металите са пре- съставлява типични соли(CaF2, NaCl, MgBr2, KI), ко- които могат да бъдат получени чрез директно взаимодействие взаимодействие на метал с халоген. Свободните халогени се получават от естествени соли, така че името „халогени“ също се превежда като „родени от соли“.
Минималната степен на окисление (–1) е най-стабилна за всички халогени. Някои характеристики на атомите на елементите от група VIIA са дадени в Най-важните характеристики на атомите на елементи от група VIIA
Халогените имат висок електронен афинитет (максимум при Cl) и много висока йонизационна енергия (максимум при F) и максимум възможна електроотрицателност във всеки период. Флуорът е най-много електроотрицателни на всички химични елементи. Наличието на един несдвоен електрон в халогенните атоми определя представлява обединяването на атомите в простите вещества в двуатомни молекули Г2. За простите вещества най-характерните окислители са халогените свойства, които са най-силни във F2 и отслабват при преминаване към I2. Халогените се характеризират с най-голяма реактивност от всички неметални елементи. Флуорът, дори сред халогените, се откроява има изключително висока активност. Елементът от втория период, флуорът, се различава най-силно от другия други елементи на подгрупата. Това е общ модел за всички неметали.
Флуорът, като най-електроотрицателният елемент, не показва секс резидентни степени на окисление. Във всяка връзка, включително с ки- кислород, флуорът е в степен на окисление (-1). Всички други халогени показват положителни степени на окисление leniya до максимум +7. Най-характерните степени на окисление на халогените: F: -1, 0; Cl, Br, I: -1, 0, +1, +3, +5, +7. Cl има известни оксиди, в които се намира в степени на окисление: +4 и +6. Най-важните халогенни съединения, в положителни състояния, Наказанията за окисляване са кислородсъдържащи киселини и техните соли. Всички халогенни съединения в положителни степени на окисление са са силни окислители. ужасна степен на окисление.Диспропорционалността се насърчава от алкална среда. Практическо приложение на прости вещества и кислородни съединения Редукцията на халогените се дължи главно на техния окислителен ефект. Най-широк практическа употребанамерете прости вещества Cl2 и F2. Най-голямо количествохлор и флуор се консумират в промишлеността органичен синтез: в производството на пластмаси, хладилни агенти, разтворители, пестициди, лекарства. Значителни количества хлор и йод се използват за получаване на метали и за тяхното рафиниране. Използва се и хлор за избелване на целулоза, за дезинфекция пия водаи в производството вода от белина и солна киселина. Солите на оксокиселините се използват при производството на експлозиви.
Киселините - солна и разтопена киселина - намират широко приложение в практиката. Флуорът и хлорът са сред двадесетте най-често срещани елемента там в природата има значително по-малко бром и йод. Всички халогени се срещат в природата в тяхното състояние на окисление(-1). Само йодът се среща под формата на сол KIO3, който е включен като примес в чилийската селитра (KNO3). Астатът е изкуствено произведен радиоактивен елемент (не съществува в природата). Нестабилността на At е отразена в името, което идва от гръцки. "astatos" - "нестабилен". Астатът е удобен излъчвател за лъчетерапия на ракови тумори. Прости вещества Простите вещества на халогените се образуват от двуатомни молекули G2. В прости вещества, по време на прехода от F2 към I2 с увеличаване на броя на електроните тронни слоеве и увеличаване на поляризуемостта на атомите, има увеличение междумолекулно взаимодействие, което води до промяна в агрегатния ко- стои при стандартни условия. Флуорът (при нормални условия) е жълт газ, при –181o C се превръща в течно състояние. Хлорът е жълто-зелен газ, който се превръща в течност при –34o C. С цвят на ха- Името Cl се свързва с него, идва от гръцкото „хлорос” – „жълт- зелено". Рязко повишаване на точката на кипене на Cl2 в сравнение с F2, показва повишено междумолекулно взаимодействие. Бромът е тъмночервена, много летлива течност, кипи при 58,8o C. името на елемента се свързва с острата неприятна миризма на газ и произлиза от "bromos" - "вонящ". Йод – тъмно лилави кристали, със слаб „металик“ бучки, които при нагряване лесно се сублимират, образувайки виолетови пари;
Точката на кипене на йода е 183 ° C. Името му идва от цвета на йодните пари - "йодос" - "пурпурен". Всички прости вещества имат остра миризма и са отровни. Вдишването на техните пари предизвиква дразнене на лигавиците и дихателните органи, а при високи концентрации - задушаване. По време на Първата световна война хлорът е използван като отровно средство. Флуорният газ и течният бром причиняват изгаряния на кожата. Работа с ха- logens, трябва да се вземат предпазни мерки. Тъй като простите вещества на халогените се образуват от неполярни молекули охлаждат, те се разтварят добре в неполярни органични разтворители: алкохол, бензен, тетрахлорид и др. Хлорът, бромът и йодът са слабо разтворими във вода; техните водни разтвори се наричат хлорна, бромна и йодна вода. Br2 се разтваря по-добре от други, концентрация на бром в наситен. Разтворът достига 0,2 mol/l, а хлорът – 0,1 mol/l. Флуоридът разлага водата: 2F2 + 2H2 O = O2 + 4HF Халогените проявяват висока окислителна активност и преход в халогенидни аниони. Г2 + 2e– 2Г– Флуорът има особено висока окислителна активност. Флуорът окислява благородните метали (Au, Pt). Pt + 3F2 = PtF6 Той дори взаимодейства с някои инертни газове (криптон, ксенон и радон), напр. Xe + 2F2 = XeF4 В атмосферата на F2 много много стабилни връзки, Например, вода, кварц (SiO2). SiO2 + 2F2 = SiF4 + O2
В реакции с флуор дори такива силни окислители като азот и сяра нична киселина, действат като редуциращи агенти, докато флуорът окислява входа съдържащи O(–2) в състава си. 2HNO3 + 4F2 = 2NF3 + 2HF + 3O2 H2 SO4 + 4F2 = SF6 + 2HF + 2O2 Високата реактивност на F2 създава трудности при избора на кон- структурни материали за работа с него. Обикновено за тези цели използваме Има никел и мед, които при окисляване образуват плътни защитни филми от флуориди на повърхността си. Името F се дължи на агресивното му действие. ям, идва от гръцки. “fluoros” – “разрушителен”. В серията F2, Cl2, Br2, I2 окислителната способност отслабва поради увеличаване увеличаване на размера на атомите и намаляване на електроотрицателността. IN водни разтвориокислителни и редуктивни свойства на вер- Веществата обикновено се характеризират с помощта на електродни потенциали. Таблицата показва стандартни електродни потенциали (Eo, V) за редукционни полуреакции образуване на халогени. За сравнение, стойността на Eo за ki- въглеродът е най-разпространеният окислител. Стандартни електродни потенциали за прости халогенни вещества
Намалена окислителна активност Както се вижда от таблицата, F2 е много по-силен окислител, отколкото O2, следователно F2 не съществува във водни разтвори , окислява водата, възстановяване до F–. Съдейки по стойността на Eо, окислителната способност на Cl2
също по-висока от тази на O2. Всъщност при дългосрочно съхранение на хлорна вода тя се разлага с отделяне на кислород и образуване на HCl. Но реакцията е бавна (молекулата Cl2 е значително по-силна от молекулата F2 и енергията на активиране за реакции с хлор е по-висока), диспро- порциониране: Cl2 + H2 O HCl + HOCl Във вода не достига края (K = 3,9 . 10–4), следователно Cl2 съществува във водни разтвори. Br2 и I2 се характеризират с още по-голяма стабилност във вода. Диспропорционалността е много характерен окислител редукционна реакция за халогени. Диспропорционалност на усилването излива се в алкална среда. Диспропорционирането на Cl2 в алкали води до образуването на аниони Cl– и ClO–. Константата на диспропорционалност е 7,5. 1015. Cl2 + 2NaOH = NaCl + NaClO + H2O Когато йодът е диспропорциониран в основа, се образуват I– и IO3–. ана- Логично Br2 диспропорционира йода. Промяната на продукта е непропорционална нация се дължи на факта, че анионите GO– и GO2– в Br и I са нестабилни. Реакцията на диспропорциониране на хлор се използва в промишлеността възможност за получаване на силен и бързодействащ хипохлоритен окислител, избелваща вар, бертолетова сол. 3Cl2 + 6 KOH = 5KCl + KClO3 + 3H2 O
Взаимодействие на халогени с метали Халогените реагират енергично с много метали, например: Mg + Cl2 = MgCl2 Ti + 2I2 TiI4 Na + халогениди, в които металът има ниско ниво на окисление (+1, +2), - Това са солеви съединения с преобладаващо йонни връзки. Как да ето, йонните халиди са твърди вещества с висока точка на топене Метални халогениди, в които има метал висока степенокисление са съединения с преобладаващо ковалентни връзки. Много от тях са газове, течности или стопими при нормални условия твърди вещества. Например WF6 е газ, MoF6 е течност, TiCl4 е течен. Взаимодействие на халогени с неметали Халогените взаимодействат директно с много неметали: водород, фосфор, сяра и др. Например: H2 + Cl2 = 2HCl 2P + 3Br2 = 2PBr3 S + 3F2 = SF6 Свързването в неметалните халогениди е предимно ковалентно. Обикновено тези съединения имат ниски точки на топене и кипене. При преминаване от флуор към йод ковалентният характер на халогенидите се увеличава. Ковалентните халогениди на типичните неметали са киселинни съединения; при взаимодействие с вода те се хидролизират и образуват киселини. Например: PBr3 + 3H2O = 3HBr + H3PO3 PI3 + 3H2O = 3HI + H3PO3 PCl5 + 4H2O = 5HCl + H3PO4
Първите две реакции се използват за получаване на бром и йодид. ноева киселина. Интерхалогениди. Халогените, комбинирайки се един с друг, образуват интерг. води. В тези съединения по-лекият и по-електроотрицателен халоген е в степен на окисление (–1), а по-тежкият е в положително състояние. наказания за окисление. Поради директното взаимодействие на халогените при нагряване се получават: ClF, BrF, BrCl, ICl. Има и по-сложни интерхалогениди: ClF3, BrF3, BrF5, IF5, IF7, ICl3. Всички интерхалогениди при нормални условия са течни вещества с ниски температурикипене. Интерхалогенидите имат висока окислителна активност дейност. Например, такива химически стабилни вещества като SiO2, Al2O3, MgO и др. Горят в парите на ClF3. 2Al2 O3 + 4ClF3 = 4 AlF3 + 3O2 + 2Cl2 Флуорът ClF 3 е агресивен флуориращ реагент, който действа бързо двор F2. Използва се в органични синтезии за получаване на защитни филми върху повърхността на никелово оборудване за работа с флуор. Във вода интерхалогенидите се хидролизират, за да образуват киселини. Например, ClF5 + 3H2O = HClO3 + 5HF Халогени в природата. Получаване на прости вещества В промишлеността халогените се получават от техните естествени съединения. всичко процесите за получаване на свободни халогени се основават на окислението на халоген Nid йони. 2Г – Г2 + 2e– Значително количество халогени се намира в естествени водипод формата на аниони: Cl–, F–, Br–, I–. IN морска водаможе да съдържа до 2,5% NaCl. Бромът и йодът се получават от водата нефтени кладенции морска вода.
Строеж и свойства на атомите. Елементи от главната подгрупа на VII група Периодичната таблицаД. И. Менделеев, обединени под общото наименование халогени - флуор F, хлор Cl, бром Br, йод I, астат At (рядко се срещат в природата) - са типични неметали. Това е разбираемо, тъй като техните атоми съдържат на външната енергийно нивоседем електрона и им трябва само един електрон, за да го завършат. Халогенните атоми, когато взаимодействат с метали, приемат електрон от металните атоми. В този случай възниква йонна връзкаи се образуват соли. Ето откъде идва често срещано имеподгрупи "халогени", т.е. "раждащи соли". Халогените са много силни окислители. Флуор в химична реакцияпроявява само окислителни свойства и се характеризира само с -1 степен на окисление в съединенията. Останалите халогени също проявяват редуциращи свойства при взаимодействие с повече електроотрицателни елементи - флуор, кислород, азот. Техните степени на окисление могат да приемат стойности +1, +3, +5, +7. Редукционните свойства на халогените се увеличават от хлор към йод, което е свързано с увеличаване на радиусите на техните атоми: атомите на хлора са приблизително един и половина пъти по-малки от йода. Халогените са прости вещества. Всички халогени съществуват в свободно състояние под формата на двуатомни молекули с ковалентен неполярен химическа връзкамежду атомите. В твърдо състояние F 2, Cl 2, Br 2, I 2 имат молекулярни кристални решетки, което се потвърждава от техните физически свойства(Таблица 7). Таблица 7
Както се вижда, с увеличаване молекулно теглохалогени, техните точки на топене и кипене се повишават (фиг. 88), увеличава се плътността: флуорът и хлорът са газове, бромът е течност, йодът е твърдо вещество.
Ориз. 88. Това се дължи на факта, че с увеличаването на размерите на халогенните атоми и молекули (фиг. 89) се увеличават и силите на междумолекулно взаимодействие между тях.
Ориз. 89. От F 2 до I 2 интензивността на цвета на халогените се увеличава. Йодните кристали имат метален блясък. Химическата активност на халогените, подобно на неметалите, отслабва от флуор до йод. Всеки халоген е най-силният окислител в своя период. Окислителните свойства на халогените се проявяват ясно, когато взаимодействат с метали. В този случай, както вече знаете, се образуват соли. Така флуорът вече реагира при нормални условия с повечето метали, а при нагряване реагира и със златото, среброто и платината, които са известни със своята химическа пасивност. Алуминият и цинкът се запалват във флуорна атмосфера:
Останалите халогени реагират с металите главно при нагряване. И така, в колба, пълна с хлор, кристали от натрошен антимон пламват и горят красиво (фиг. 90), образувайки смес от два антимонови хлорида (III) и (V):
Ориз. 90. Нагретият железен прах също се запалва, когато реагира с хлор. Експериментът може да се проведе и с антимон, но само железните стружки трябва първо да се нагреят в желязна лъжица и след това да се излеят на малки порции в колба с хлор. Тъй като хлорът е силен окислител, реакцията води до образуването на железен (III) хлорид (фиг. 91):
Ориз. 91. Нажежена медна жица гори в бромни пари:
Йодът окислява металите по-бавно, но в присъствието на вода, която е катализатор, реакцията на йод с алуминиев прах протича много бурно:
Реакцията е придружена от отделяне на виолетови йодни пари (защо?). Намаляването на окислителните свойства и увеличаването на редуциращите свойства на халогените от флуор до йод също може да се съди по способността им да се изместват един друг от солни разтвори.
Ориз. 92. Свободният бром измества йода от солите:
Тази реакция не е типична за флуора, тъй като протича в разтвор и флуорът взаимодейства с водата, измествайки кислорода от нея:
Тук кислородът играе необичайната роля на редуциращ агент. Това е може би единственият случай, когато кислородът в реакцията на горене не е едно от изходните вещества, а негов продукт. Отслабването на окислителните свойства на халогените от флуор до йод се проявява ясно, когато те взаимодействат с водород. Уравнението за тази реакция може да бъде написано в общ вид: N 2 + G 2 = 2NG (G - условно химическо обозначениехалогени). Ако флуорът реагира с водород при всякакви условия с експлозия, тогава смес от хлор и водород реагира с експлозия само при запалване или директно облъчване слънчева светлина, бромът реагира с водорода при нагряване и без експлозия. Тези реакции са екзотермични. Реакцията на съединението на кристалния йод с водорода е слабо ендотермична, протича бавно дори при нагряване. В резултат на тези реакции се образуват съответно флуороводород HF, хлороводород HCl, бромоводород HBr и йодоводород HI. Откриване на халогени. Флуорът в свободна форма е получен за първи път през 1886 г. от френския химик А. Моасан, който е награден за това Нобелова награда. Елементът получи името си от гръцкия fluoros - "унищожаващ". Хлорът е открит от шведския химик К. Шееле през 1774 г. Елементът е кръстен на цвета си просто вещество(от гръцки хлорос - жълто-зелен). Бромът е открит през 1826 г. от френския химик А. Балард. Елементът е наречен така заради миризмата на просто вещество (от гръцки bromos - зловонно). Йодът е получен през 1811 г. от френския учен Б. Куртоа и е получил името си за цвета на парите на просто вещество (от гръцките iodes - виолетово). Нови думи и понятия
Задачи за самостоятелна работа
Прочетете също: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||