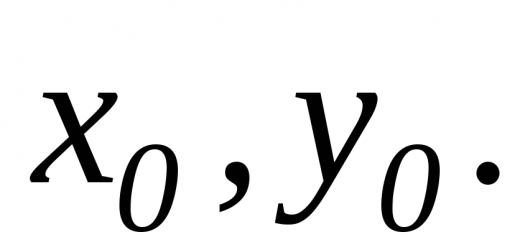... suhbatlashish uchun umumiy mavzu"fizika" va "kimyo" so'zlari.
Ikkala so'z ham bodibilding bilan bog'liqligi ajablanarli emasmi? "Fizika" mushaklar, "kimyo" degan ma'noni anglatadi - yaxshi, buni tushuntirishga hojat yo'q.
Umuman olganda, kimyo fani, asosan, fizika bilan bir xil: u tabiatda sodir bo'ladigan hodisalar haqida. Galiley Piza minorasidan to'p tashlaganida va Nyuton o'z qonunlarini yaratganida, biz insonga mos keladigan o'lchov haqida gapirgan edik - bu fizika edi va shundaydir. Oddiy fizika moddalardan tashkil topgan jismlar bilan shug'ullanadi. Kimyo (alkimyo) moddalarni bir-biriga aylantirish bilan shug'ullangan va shug'ullanadi - bu molekulyar daraja. Ma'lum bo'lishicha, fizika va kimyo o'rtasidagi farq ob'ektlar miqyosida? Hech qisi yo'q! Bu yerga kvant fizikasi atomlar nimadan iboratligi bilan shug'ullanadi - bu submolekulyar daraja. Kvant fizikasi atom ichidagi ob'ektlar bilan shug'ullanadi, bu atom energiyasi ustidan kuch beradi va qo'yadi falsafiy savollar. Ma'lum bo'lishicha, kimyo - bu moddaning atom-molekulyar tuzilishi darajasi bilan aniq chegaralangan bo'lsa-da, fizik miqyosdagi tor chiziq.
Menimcha, yomon tekis (chiziqli) cheksizlik* atrofdagi dunyoga taalluqli emas. Hamma narsa ilmoqli yoki shar shaklida yopilgan. Koinot sharsimondir. Agar biz elementar zarralar (kvarklar va Xiggs bozonlari) tuzilishiga chuqurroq kirib borsak, ertami-kechmi topilgan zarralar maksimal miqyosda - Koinot bilan yopiladi, ya'ni ertami-kechmi biz o'z koinotimizni qush zarralaridan ko'ramiz. mikroskop orqali ko'zni ko'rish.
Keling, bodibilding uchun o'lchov diapazonlari qo'llanilishini ko'rib chiqaylik. Shunday ko'rinadi. "Fizika" (temir bilan va simulyatorlarda mashq qilish) temir buyumlar va mushaklar bilan qattiq ob'ektlar sifatida ishlaydi: odamga mos keladigan o'lchov. "Kimyo" (steroidlar kabi), albatta, molekulyar darajada. Bodibildingda "kvant fizikasi" nima ekanligini aniqlash qoladi? Ko'rinib turibdiki, bu motivatsiya, diqqatni jamlash, iroda kuchi va boshqalar - ya'ni psixika. Psixika esa molekulyar asosga emas, balki aniq asosga asoslanadi elektr maydonlari va davlatlar - ularning miqyosi atomdan past. Shunday qilib, bodibilding to'liq miqyosga yetdi ...
Maqolani o'qish fanlari nomzodi. Elena Goroxovskaya(“Novaya gazeta”, 55-son, 24.05.2013 yil, 12-bet yoki “Postnauka” veb-saytida) biosemiotika asoslari haqida:
yashash nima? (...) Asosiy “suv havzasi” reduksionistik** va antireduksion yondoshuvlar oʻrtasida. Reduksionistlar hayotni barcha o'ziga xosliklari bilan fizik va kimyoviy jarayonlar yordamida tushuntirish mumkinligini ta'kidlaydilar. Antireduksionistik yondashuvlar hamma narsani fizika va kimyoga qisqartirish mumkin emasligini ta'kidlaydi. Eng qiyin narsa tirik organizmning yaxlitligi va maqsadli tuzilishini tushunishdir, bu erda hamma narsa o'zaro bog'liq va hamma narsa uning hayotiy faoliyatini, ko'payishi va rivojlanishini qo'llab-quvvatlashga qaratilgan. Davomida individual rivojlanish, va umuman olganda, har daqiqada tanada nimadir o'zgaradi, bu o'zgarishlarning tabiiy yo'nalishi ta'minlanadi. Ko'pincha tirik organizmlarni ob'ektlar emas, balki jarayonlar deb atash kerakligi aytiladi.* * *...XX asrda kibernetika tirik mavjudotlarning o‘ziga xos xususiyatlarini tushunish uchun muhim ahamiyat kasb etdi, chunki u biologiyada maqsad tushunchasini qayta tikladi. Bundan tashqari, kibernetika tirik organizmlar haqidagi g'oyani juda mashhur qildi axborot tizimlari. Shunday qilib, tirik mavjudotlar haqidagi fanga bevosita moddiy tashkilotga aloqador bo'lmagan gumanitar tushunchalar kiritilgan.
1960-yillarda tirik mavjudotlarning o'ziga xos xususiyatlarini tushunish va o'rganishda yangi yo'nalish paydo bo'ldi. biologik tizimlar- hayot va tirik organizmlarni belgi jarayonlari va munosabatlari deb hisoblaydigan biosemiotika. Aytishimiz mumkinki, tirik organizmlar narsalar dunyosida emas, balki ma'nolar dunyosida yashaydi.
...Molekulyar genetika ko‘p darajada o‘zining kontseptual sxemasiga “genetik axborot” va “genetik kod” kabi tushunchalarning kiritilishi tufayli shakllandi. Ochilish haqida gapirish genetik kod, mashhur biolog Martinas Ichas shunday deb yozgan edi: ““Kod muammosi” haqida eng qiyin narsa kod mavjudligini tushunish edi. Bir asr davom etdi."
Hujayrada oqsil biosintezi turli xil kimyoviy reaksiyalar orqali sodir bo'lsa-da, oqsillarning tuzilishi bilan nuklein kislotalarning tuzilishi o'rtasida bevosita kimyoviy bog'liqlik yo'q. Bu bog'lanish o'z mohiyatiga ko'ra kimyoviy emas, balki informatsion, semiotik xususiyatga ega. DNK va RNK nuklein kislotalaridagi nukleotidlar ketma-ketligi oqsillarning tuzilishi haqida (ulardagi aminokislotalar ketma-ketligi haqida) faqat hujayrada "o'quvchi" (aka "yozuvchi") mavjudligi sababli ma'lumot beradi - bu holda. murakkab tizim"genetik tilda" gapiradigan protein biosintezi. (...) Shunday qilib, hatto haqiqatda ham asosiy daraja tirik aloqa, matn va "nutq" bo'lib chiqadi. Har bir hujayrada va umuman tanada o'qish, yozish, qayta yozish, yangi matnlarni yaratish va doimiy "suhbat" makromolekulyarlarning genetik kodlari tilida va ularning o'zaro ta'siri doimiy ravishda sodir bo'ladi.
Birinchi va oxirgi xatboshilardagi iboralardagi bir nechta so'zlarni almashtiramiz:
Retrogradlarning ta'kidlashicha, bodibilding o'zining barcha xususiyatlarida jismoniy tarbiya va kimyoviy ta'sirlarga qisqartirilishi mumkin. Progressiv yondashuv hamma narsani "fizika" va "kimyo" ga qisqartirish mumkin emasligini ta'kidlaydi. Mushak massasining o'sishi turli jismoniy mashqlar va kimyoviy (hech bo'lmaganda oziq-ovqat) ta'siri orqali amalga oshirilgan bo'lsa-da, mushaklarning o'sishi va jismoniy mashqlar miqdori va "kimyo" miqdori o'rtasida to'g'ridan-to'g'ri bog'liqlik yo'q. Bu bog'lanish o'z mohiyatiga ko'ra fizik yoki kimyoviy emas, balki informatsion, semiotik xususiyatga ega. Shunday qilib, hatto eng asosiy darajada Bodibilding aloqa, matn va "nutq" bo'lib chiqadi(biz, albatta, yondashuvlar orasidagi qo'pol suhbat haqida gapirmayapmiz). Shuning uchun biz buni aytishimiz mumkin bodibildingchilarni ob'ektlar emas, balki axborot jarayonlari deb atash kerak.Mushakni ahmoqona pompalay olmaysiz deb kim bahslasha oladi. Sizga to'g'ri tuzilgan va bajarilgan mashq kerak, sizga kerak to'g'ri ovqatlanish, ya'ni ma'lumot talab qilinadi. Va agar biz ahmoqona kimyo bilan o'zimizni to'ldirsak, biz umuman olganda noaniq natijaga erishamiz. Bizga to'g'ri tuzilgan va bajarilgan kurs kerak, ya'ni yana ma'lumot talab qilinadi. Bunday ma'lumotlar muammosi bilan bog'liq eng qiyin narsa uning haqiqatda mavjudligini tushunishdir. Va buni anglaganimizdan so'ng, biz uni og'ir to'lqinlarda miyamiz qirg'og'iga dumalab tushadigan, vaqti-vaqti bilan uning tubidan marvarid chig'anoqlarini uloqtiradigan loyqa psevdoma'lumot okeanidan ajratishni o'rganishimiz kerak.
To'g'ri, qobiqlarni ochish uchun ustritsa pichog'i kerak ...
------------
* yomon cheksizlik- dunyoning cheksizligi haqidagi metafizik tushuncha, bu bir xil o'ziga xos xususiyatlar, jarayonlar va harakat qonunlarining har qanday makon va vaqtning har qanday miqyosida, hech qanday cheklovsiz, cheksiz, cheksiz takrorlanishini taxmin qilishni nazarda tutadi. Materiyaning tuzilishiga nisbatan u materiyaning cheksiz bo'linuvchanligi haqidagi farazni anglatadi, bunda har bir kichikroq zarracha bir xil xususiyatlarga ega va makroskopik jismlar kabi bir xil o'ziga xos harakat qonunlariga bo'ysunadi. Bu atama Hegel tomonidan kiritilgan, ammo u haqiqiy cheksizlikni materiya emas, balki mutlaq ruhning mulki deb hisoblagan.
** reduksionistik yondashuv– lotincha reductio – qaytish, tiklash; bu holda hayot hodisalarini boshqa narsaga qisqartirish.
Fizik kimyo tarixi
M.V. Lomonosov, qaysi ichida 1752
N.N. Beketov 1865
VA Nernst.
M. S. Vrevskiy.
Molekulalar, ionlar, erkin radikallar.
Elementlarning atomlari kimyoviy jarayonlarda ishtirok etadigan uch turdagi zarrachalarni - molekulalarni, ionlarni va erkin radikallarni hosil qilishi mumkin.
Molekula kimyoviy xossalariga ega bo'lgan va mustaqil yashashga qodir bo'lgan moddaning eng kichik neytral zarrasi. Bir atomli va ko'p atomli molekulalar (diatom, triatomik va boshqalar) mavjud. Oddiy sharoitlarda asil gazlar bir atomli molekulalardan iborat; yuqori molekulyar birikmalar molekulalari, aksincha, minglab atomlarni o'z ichiga oladi.
Va u- elektronlar (anionlar) ko'pligi yoki ularning etishmasligi (kationlari) bo'lgan atom yoki kimyoviy bog'langan atomlar guruhi bo'lgan zaryadlangan zarracha. Moddada har doim musbat ionlar manfiylar bilan birga mavjud. Ionlar o'rtasida ta'sir qiluvchi elektrostatik kuchlar katta bo'lganligi sababli, moddada bir xil belgidagi ionlarning sezilarli darajada ortiqligini hosil qilish mumkin emas.
Erkin radikal to'yinmagan valentli zarracha, ya'ni juftlanmagan elektronli zarracha deyiladi. Bunday zarralar, masalan, ·CH 3 va ·NH 2. Oddiy sharoitlarda erkin radikallar umuman mavjud emas uzoq vaqt, chunki ular o'ta reaktivdir va inert zarrachalarni hosil qilish uchun oson reaksiyaga kirishadi. Shunday qilib, ikkita metil radikali CH3 birlashib, C 2 H 6 (etan) molekulasini hosil qiladi. Ko'p reaktsiyalar erkin radikallar ishtirokisiz mumkin emas. Juda yuqori haroratlarda (masalan, Quyosh atmosferasida) faqat ikki atomli zarrachalar erkin radikallar (·CN, ·OH, ·CH va boshqalar) mavjud bo'lishi mumkin. Olovda ko'plab erkin radikallar mavjud.
Erkin radikallar ko'proq ekanligi ma'lum murakkab tuzilish, ular nisbatan barqaror va oddiy sharoitlarda mavjud bo'lishi mumkin, masalan, trifenilmetil radikali (C 6 H 5) 3 C · (uning ochilishi bilan erkin radikallarni o'rganish boshlandi). Uning barqarorligi sabablaridan biri fazoviy omillar - fenil guruhlarining katta hajmi bo'lib, ular radikallarning geksafeniletan molekulasiga birikmasini oldini oladi.
Kovalent bog'lanish.
Strukturaviy formulalardagi har bir kimyoviy bog'lanish ko'rsatilgan valentlik chizig'i , Masalan:
H-H (ikki vodorod atomi orasidagi bog'lanish)
H 3 N−H + (ammiak molekulasining azot atomi va vodorod kationi orasidagi bog'lanish)
(K +)−(I−) (kaliy kationi va yodid ioni orasidagi bog'lanish).
Kimyoviy bog'lanish tufayli hosil bo'ladi atom yadrolarining bir juft elektronga tortilishi(nuqta ·· bilan ko'rsatilgan), bu murakkab zarrachalarning elektron formulalarida (molekulalar, kompleks ionlar) ifodalanadi. valentlik chizig'i- o'zlaridan farqli o'laroq, yolg'iz elektron juftlari Har bir atom, masalan:
| :::F−F::: | (F 2); | H−Cl::: | (HCl); | .. H−N−H | H | (NH 3) |
Kimyoviy bog'lanish deyiladi kovalent, tomonidan tuzilgan bo'lsa bir juft elektronni almashish ikkala atom.
Molekulyar qutblanish
Xuddi shu elementning atomlari tomonidan hosil bo'lgan molekulalar odatda bo'ladi qutbsiz , bog'lanishlarning o'zi qanchalik qutbsiz. Shunday qilib, H 2, F 2, N 2 molekulalari qutbsizdir.
Turli elementlarning atomlari tomonidan hosil bo'lgan molekulalar bo'lishi mumkin qutbli
Va qutbsiz
. ga bog'liq geometrik shakl
.
Agar shakli simmetrik bo'lsa, u holda molekula qutbsiz(BF 3, CH 4, CO 2, SO 3), agar assimetrik bo'lsa (yolg'iz juftlar yoki juftlanmagan elektronlar mavjudligi sababli), u holda molekula qutbli(NH 3, H 2 O, SO 2, NO 2).
Nosimmetrik molekuladagi yon atomlardan biri boshqa element atomi bilan almashtirilganda, geometrik shakl ham buziladi va qutblanish paydo bo'ladi, masalan, xlorli metan hosilalari CH 3 Cl, CH 2 Cl 2 va CHCl 3 (CH). 4 ta metan molekulasi qutbsiz).
Polarlik dan molekulaning assimetrik shakli kelib chiqadi qutblanish kovalent aloqalar
elementlarning atomlari orasidagi turli elektronegativlik bilan
.
Yuqorida ta'kidlab o'tilganidek, bog'lanish o'qi bo'ylab elektron zichligi ko'proq elektronegativ element atomiga qisman siljishi mavjud, masalan:
| H d+ → Cl d− | B d+ → F d− |
| C d− ← H d+ | N d− ← H d+ |
(bu erda d qisman elektr zaryadi atomlar haqida).
Ko'proq elektromanfiylik farqi elementlar bo'lsa, d zaryadining mutlaq qiymati qanchalik yuqori bo'lsa va shuncha ko'p bo'ladi qutbli kovalent bog'lanish bo'ladi.
Shakli nosimmetrik bo'lgan molekulalarda (masalan, BF 3) manfiy (d-) va musbat (d+) zaryadlarning "og'irlik markazlari" mos keladi, ammo assimetrik molekulalarda (masalan, NH 3) ular mos kelmaydi. mos keladi.
Natijada, assimetrik molekulalarda elektr dipol
- kosmosda, masalan, suv molekulasida ma'lum masofa bilan ajratilgan zaryadlardan farqli o'laroq.
Vodorod aloqasi.
Ko'p moddalarni o'rganayotganda, deb ataladi vodorod aloqalari . Masalan, suyuqlikdagi HF molekulalari vodorod ftorid bir-biriga vodorod bog'i bilan bog'langan, xuddi shunday, suyuq suvdagi yoki muz kristalidagi H 2 O molekulalari, shuningdek NH 3 va H 2 O molekulalari bir-biriga molekulalararo bog'liqlikda bog'langan - ammiak gidrati NH 3 H 2 O.
Vodorod aloqalari beqaror va juda oson yo'q qilinadi (masalan, muz eriganda, suv qaynaganda). Biroq, bu aloqalarni uzish uchun qo'shimcha energiya sarflanadi va shuning uchun moddalarning erish va qaynash nuqtalari vodorod aloqalari molekulalar orasidagi o'xshash moddalarga qaraganda ancha yuqori, ammo vodorod aloqalarisiz:
Valentlik. Donor-akseptor aloqalari. Molekulyar tuzilish nazariyasiga ko'ra, atomlar orbitallarini bitta elektron egallasa, shuncha kovalent bog'lanish hosil qilishi mumkin, ammo bu har doim ham shunday emas. [AO ni to'ldirish uchun qabul qilingan sxemada birinchi navbatda qobiqning raqami, keyin orbitalning turi, so'ngra orbitalda bir nechta elektron bo'lsa, ularning soni (yuqori yozuv) ko'rsatiladi. Shunday qilib, yozib oling (2 s) 2 buni bildiradi s-ikkinchi qobiq orbitallarida ikkita elektron mavjud.] Asosiy holatdagi uglerod atomi (3 R) elektron konfiguratsiyaga ega (1 s) 2 (2s) 2 (2p x)(2 p y), ikkita orbital to'ldirilmagan bo'lsa, ya'ni. har birida bittadan elektron mavjud. Biroq, ikki valentli uglerod birikmalari juda kam uchraydi va yuqori reaktivdir. Odatda, uglerod tetravalentdir va bu uning hayajonlangan 5 ga o'tishi bilan bog'liq. S-davlat (1 s) 2 (2s) (2p x)(2 p y)(2 p z) To'rtta to'ldirilmagan orbital bilan juda kam energiya kerak bo'ladi. O'tish bilan bog'liq energiya xarajatlari 2 s-elektron erkin 2 R-orbital, ikkita qo'shimcha bog'lanish hosil bo'lganda ajralib chiqadigan energiya bilan qoplanadi. To'ldirilmagan AOlarning shakllanishi uchun bu jarayon energiya jihatidan qulay bo'lishi kerak. Elektron konfiguratsiyaga ega azot atomi (1 s) 2 (2s) 2 (2p x)(2 p y)(2 p z) besh valentli birikmalar hosil qilmaydi, chunki 2 ni uzatish uchun energiya talab qilinadi s-3 uchun elektron d-orbital besh valentli konfiguratsiyani hosil qiladi (1 s) 2 (2s)(2p x)(2 p y)(2 p z)(3 d), juda katta. Xuddi shunday, odatdagi konfiguratsiyaga ega bo'lgan bor atomlari (1 s) 2 (2s) 2 (2p) hayajonlangan holatda uch valentli birikmalar hosil qilishi mumkin (1 s) 2 (2s)(2p x)(2 p y), o'tish paytida sodir bo'ladi 2 s-2 uchun elektron R-AO, lekin qo'zg'aluvchan holatga o'tgandan beri besh valentli birikmalar hosil qilmaydi (1 s)(2s)(2p x)(2 p y)(2 p z), 1 dan birining o'tkazilishi tufayli s- elektronlar ko'proq yuqori daraja, juda ko'p energiya talab qiladi. Atomlarning ular orasidagi bog'lanish hosil bo'lishi bilan o'zaro ta'siri faqat yaqin energiyaga ega bo'lgan orbitallar mavjudligida sodir bo'ladi, ya'ni. bosh kvant soni bir xil bo'lgan orbitallar. Davriy jadvalning dastlabki 10 elementi uchun tegishli ma'lumotlar quyida umumlashtiriladi. Atomning valentlik holati - uning kimyoviy bog'lanish holati, masalan, 5-holat S tetravalent uglerod uchun.
| DAVRIY JADEVNING BIRINCHI O'N ELMEENTINING VALENTLIK HOLATLARI VA VALENTLIKLARI | |||
| Element | Tuproq holati | Oddiy valentlik holati | Doimiy valentlik |
| H | (1s) | (1s) | |
| U | (1s) 2 | (1s) 2 | |
| Li | (1s) 2 (2s) | (1s) 2 (2s) | |
| Bo'l | (1s) 2 (2s) 2 | (1s) 2 (2s)(2p) | |
| B | (1s) 2 (2s) 2 (2p) | (1s) 2 (2s)(2p x)(2 p y) | |
| C | (1s) 2 (2s) 2 (2p x)(2 p y) | (1s) 2 (2s)(2p x)(2 p y)(2 p z) | |
| N | (1s) 2 (2s) 2 (2p x)(2 p y)(2 p z) | (1s) 2 (2s) 2 (2p x)(2 p y)(2 p z) | |
| O | (1s) 2 (2s) 2 (2p x) 2 (2 p y)(2 p z) | (1s) 2 (2s) 2 (2p x) 2 (2 p y)(2 p z) | |
| F | (1s) 2 (2s) 2 (2p x) 2 (2 p y) 2 (2 p z) | (1s) 2 (2s) 2 (2p x) 2 (2 p y) 2 (2 p z) | |
| Yo'q | (1s) 2 (2s) 2 (2p x) 2 (2 p y) 2 (2 p z) 2 | (1s) 2 (2s) 2 (2p x) 2 (2 p y) 2 (2 p z) 2 |
Ushbu naqshlar quyidagi misollarda namoyon bo'ladi:

Fizik kimyo tarixi
Fizik kimyo 18-asr oʻrtalarida boshlangan. "Jismoniy kimyo" atamasi tegishli M.V. Lomonosov, qaysi ichida 1752 yili, birinchi marta Sankt-Peterburg universiteti talabalari uchun "Haqiqiy fizik kimyo kursi" ni o'qib chiqdim. Ushbu kursda uning o'zi ushbu fanga quyidagi ta'rifni berdi: "Jismoniy kimyo - bu fizik printsiplar va tajribalar asosida murakkab jismlardagi kimyoviy operatsiyalar orqali nima sodir bo'lishining sababini tushuntirishi kerak bo'lgan fan."
Keyin bir asrdan ko'proq tanaffus bo'ldi va fizik kimyo bo'yicha navbatdagi kursni akademik o'qidi N.N. Beketov Xarkov universitetida 1865 yil. N.N. Beketov Rossiyaning boshqa universitetlarida fizik kimyodan dars bera boshladi. Flavitskiy (Qozon 1874), V. Ostvald (Tartu universiteti 18807), I.A. Kablukov (Moskva universiteti 1886).
Fizik kimyoning mustaqil fan sifatida tan olinishi va akademik intizom, 1887 yilda Leyptsig universitetida (Germaniya) ifodalangan. Birinchi fizik kimyo kafedrasi V. Ostvald rahbarlik qilgan va birinchi tashkil etilganda ilmiy jurnal fizik kimyoda. 19-asrning oxirida Leyptsig universiteti fizik kimyoni rivojlantirish markazi bo'lib, etakchi fizik kimyogarlar: V. Ostvald, J. van't Xoff, Arrenius Va Nernst.
Rossiyada birinchi fizik kimyo kafedrasi 1914 yilda Sankt-Peterburg universitetining fizika-matematika fakultetida ochildi, u erda kuzda majburiy kursni o'qita boshladi va amaliy mashg'ulotlar fizik kimyoda M. S. Vrevskiy.
Fizik kimyo va kimyoviy fizika o'rtasidagi farq
Bu fanlarning ikkalasi ham kimyo va fizika o'rtasidagi chorrahada joylashgan; ba'zan kimyoviy fizika fizik kimyoga kiritilgan. Bu fanlar o'rtasida aniq chegarani belgilash har doim ham mumkin emas. Biroq, o'rtacha darajada aniqlik bilan bu farqni quyidagicha aniqlash mumkin:
fizik kimyo bir vaqtning o'zida ishtirok etish bilan sodir bo'ladigan jarayonlarni jami ko'rib chiqadi to'plamlar zarralar;
· kimyoviy fizika bo'yicha sharhlar alohida zarralar va ular o'rtasidagi o'zaro ta'sir, ya'ni o'ziga xos atomlar va molekulalar (shuning uchun unda "kontseptsiya uchun joy yo'q" ideal gaz", bu fizik kimyoda keng qo'llaniladi).
2-ma'ruza Molekulalarning tuzilishi va kimyoviy bog'lanish tabiati. Kimyoviy bog'lanish turlari. Elementning elektromanfiyligi haqida tushuncha. Polarizatsiya. Dipol momenti. Molekulalarning hosil bo'lishining atom energiyasi. Usullari eksperimental tadqiqot molekulyar tuzilish.
Molekulyar tuzilish(molekulyar tuzilish), o'zaro tartibga solish molekulalardagi atomlar. Kimyoviy reaksiyalar jarayonida reaksiyaga kirishuvchi moddalar molekulalaridagi atomlar qayta joylashadi va yangi birikmalar hosil bo'ladi. Shuning uchun asosiy kimyoviy muammolardan biri atomlarning dastlabki birikmalardagi joylashishini va ulardan boshqa birikmalar hosil bo'lishi paytidagi o'zgarishlarning tabiatini aniqlashdir.
Molekulalarning tuzilishi haqidagi dastlabki fikrlar tahlilga asoslangan edi kimyoviy xatti-harakatlar moddalar. Bu g'oyalar haqida bilim sifatida murakkablashdi kimyoviy xossalari moddalar. Kimyoning asosiy qonunlarini qo'llash ma'lum birikma molekulasini tashkil etuvchi atomlarning soni va turini aniqlash imkonini berdi; bu ma'lumot kimyoviy formulada mavjud. Vaqt o'tishi bilan kimyogarlar molekulani aniq tavsiflash uchun bitta kimyoviy formula etarli emasligini tushunishdi, chunki bir xil izomer molekulalari mavjud. kimyoviy formulalar, lekin har xil xususiyatlar. Bu fakt olimlarni molekuladagi atomlar ular orasidagi bog'lanishlar bilan barqarorlashgan ma'lum bir topologiyaga ega bo'lishi kerak degan fikrga olib keldi. Bu fikrni birinchi marta 1858 yilda nemis kimyogari F.Kekule bildirgan. Uning g'oyalariga ko'ra, molekulani strukturaviy formuladan foydalanib tasvirlash mumkin, bu nafaqat atomlarning o'zini, balki ular orasidagi bog'lanishni ham ko'rsatadi. Atomlararo aloqalar ham mos kelishi kerak fazoviy tartibga solish atomlar. Metan molekulasining tuzilishi haqidagi g'oyalarning rivojlanish bosqichlari rasmda ko'rsatilgan. 1. Tuzilishi zamonaviy ma'lumotlarga mos keladi G : molekula muntazam tetraedr shakliga ega, markazda uglerod atomi va uchlarida vodorod atomlari joylashgan.
Biroq, bunday tadqiqotlar molekulalarning kattaligi haqida hech narsa aytmadi. Ushbu ma'lumot faqat tegishli ma'lumotlarni ishlab chiqish bilan mavjud bo'ldi jismoniy usullar. Ulardan eng muhimi rentgen nurlari diffraksiyasi bo'lib chiqdi. Kristallardagi rentgen nurlarining tarqalishi naqshlaridan kristalldagi atomlarning aniq o'rnini aniqlash, molekulyar kristallar uchun esa alohida molekulada atomlarni lokalizatsiya qilish mumkin bo'ldi. Boshqa usullar gazlar yoki bug'lar orqali o'tayotganda elektronlarning diffraktsiyasini va molekulalarning aylanish spektrlarini tahlil qilishni o'z ichiga oladi.
Bu ma'lumotlarning barchasi faqat beradi umumiy fikr molekulaning tuzilishi haqida. Kimyoviy bog'lanishlarning tabiati bizga zamonaviyni o'rganishga imkon beradi kvant nazariyasi. Va molekulyar strukturani etarlicha yuqori aniqlik bilan hisoblash hali imkoni bo'lmasa-da, ma'lum bo'lgan barcha ma'lumotlar kimyoviy bog'lanishlar tushuntirish mumkin. Yangi turdagi kimyoviy bog'lanishlar mavjudligi hatto bashorat qilingan.
Ko'pincha ma'lum bir jarayonni muhokama qiladigan ko'plab odamlardan: "Bu fizika!" degan so'zlarni eshitishingiz mumkin. yoki "Bu kimyo!" Darhaqiqat, inson hayoti davomida duch keladigan tabiatdagi, kundalik hayotda va kosmosdagi deyarli barcha hodisalarni ushbu fanlardan biriga bog'lash mumkin. Nima ekanligini aniqlash qiziq jismoniy hodisalar kimyoviylardan farq qiladi.
Ilmiy fizika
Fizik hodisalar kimyoviy hodisalardan qanday farq qiladi, degan savolga javob berishdan oldin, ushbu fanlarning har biri qanday ob'ektlar va jarayonlarni o'rganishini tushunish kerak. Keling, fizikadan boshlaylik.
Sizni qiziqtirishi mumkin:
Qadimgi yunon tilidan "fisis" so'zi "tabiat" deb tarjima qilingan. Ya'ni, fizika - bu ob'ektlarning xususiyatlarini, ularning xatti-harakatlarini o'rganadigan tabiat haqidagi fan turli sharoitlar, ularning davlatlari o'rtasidagi o'zgarishlar. Fizikaning maqsadi tabiiy jarayonlarni boshqaradigan qonuniyatlarni aniqlashdir. Bu fan uchun o'rganilayotgan ob'ektning nimadan iboratligi va nimadan iboratligi muhim emas Kimyoviy tarkibi, uning uchun faqat ob'ekt issiqlik ta'sirida o'zini qanday tutishi muhim, mexanik kuch, bosim va boshqalar.
Fizika hodisalarning ma'lum tor doirasini o'rganadigan bir qancha bo'limlarga bo'linadi, masalan, optika, mexanika, termodinamika, atom fizikasi va boshqalar. Bundan tashqari, ko'plab mustaqil fanlar butunlay fizikaga, masalan, astronomiya yoki geologiyaga bog'liq.
Ilmiy kimyo

Fizikadan farqli oʻlaroq, kimyo moddalarning tuzilishi, tarkibi va xossalarini, shuningdek, kimyoviy reaksiyalar natijasida oʻzgarishini oʻrganuvchi fandir. Ya'ni, kimyoni o'rganish ob'ekti kimyoviy tarkib va uning ma'lum bir jarayon davomida o'zgarishi hisoblanadi.
Kimyo, fizika kabi, ko'plab bo'limlarga ega, ularning har biri ma'lum bir sinfni o'rganadi kimyoviy moddalar, masalan, organik va noorganik, bio- va elektrokimyo. Tibbiyot, biologiya, geologiya va hatto astronomiya sohasidagi tadqiqotlar shu fan yutuqlariga asoslanadi.
Qizig'i shundaki, kimyo fan sifatida qadimgi yunon faylasuflari tomonidan uning eksperimental yo'nalishi, shuningdek, uni o'rab olgan soxta ilmiy bilimlar tufayli tan olinmagan (esda tutingki, zamonaviy kimyo alkimyodan "tug'ilgan"). Faqat Uyg'onish davridan boshlab va asosan ingliz kimyogari, fizigi va faylasufi Robert Boylning ishi tufayli kimyo to'liq fan sifatida qabul qilina boshladi.
Jismoniy hodisalarga misollar

Jismoniy qonunlarga bo'ysunadigan juda ko'p misollar keltira olasiz. Misol uchun, har bir maktab o'quvchisi 5-sinfda allaqachon jismoniy hodisani - yo'lda avtomobilning harakatini biladi. Bunday holda, bu mashina nimadan iboratligi, harakat qilish uchun energiyani qayerdan olishi muhim emas, faqat muhimi, u fazoda (yo'l bo'ylab) ma'lum bir tezlikda ma'lum bir traektoriya bo'ylab harakatlanadi. Bundan tashqari, avtomobilni tezlashtirish va tormozlash jarayonlari ham jismoniy. Avtomobilning harakatlanishi va boshqalar qattiq moddalar fizikaning "Mexanika" bo'limi bilan shug'ullanadi.
I. ...VA UMUMAN II. FAN HAQIDA III. KIMYO HAQIDA Kimyo yomonmi? Tibbiyot kimyoning onasimi? Bir dunyo analitik kimyo. Apokalipsismi? Qanchadan-qancha jinoyatlarsiz ochilmaydi sud kimyosi? Agrokimyoviy moddalarsiz qayerga boramiz? Astrokimyo hayot sirini ochib beradimi? Nima uchun biokimyo kerak? Kimyodan galurgiyada nima bor? Haqiqatan ham geokimyo xom ashyoning "giyohvandligi" ning asosidirmi? Gidrokimyo bizga yangi "oltin" beradimi? Nima uchun inson to'qimalari bo'yalgan? Gistokimyo va sitokimyo. Saraton, OITS, gripp... Qaysi fan bunga qarshi? Immunokimyo Kimyoni hisoblash mumkinmi? Kvant kimyosi. Jelli go'sht qanday qilib odamga o'xshaydi? Kolloid kimyo. Katoliklik ajralishni qachon qabul qiladi? Kosmetik kimyo haqida. Nega yerliklar kosmokimyoga muhtoj? Kristal kimyosiz zamonaviy axborot maydoni mumkinmi? Santa Klaus kimyogarlar va shifokorlarga qanday yordam beradi? Kriokimyo va kriyoterapiya. Lazer kimyosi - u nima bilan iste'mol qilinadi? O'rmonsiz kurashish mumkinmi? Yog'och kimyosi. Magnit ichida hayot bo'lishi mumkinmi? Magnetokimyo. Dori kimyosi va patokimyo o'rtasida qanday bog'liqlik bor? Metallurgiyadagi kimyodan nimasi bilan farq qiladi? Nega bizga mexanokimyo kerak? Mikroto'lqinli kimyoni qayerda uchratamiz? Nanokimyo - kimyoning o'lcham chegarasi? Bizni kim boshqaradi? Neyrokimyo. Yo'q organik kimyo: eski yoki yangi fan? Neft yoki uning qayta ishlangan mahsulotlarini sotasizmi? Neft kimyosi. Siz, men, u, u - birga... organik kimyo? Ehtimol, biz qachondir ruhni sintez qilamiz? Organik sintez. Erkin bo'lmagan moddalardagi erkin zarrachaning uzoq umr ko'rishi mumkinmi? Fizikaviy organik kimyo. "Pegniokimyo" nima? Masihning shogirdining neft kimyosi bilan qanday umumiyligi bor? Biz tosh davriga qaytamizmi? Peturgiya. Biz tosh davriga qaytamizmi? Peturgiya. Oshxonada kimyoviy moddalarni qanchalik tez-tez ishlatamiz? Oziq-ovqat kimyosi. Plazma kimyosi odamlar uchunmi yoki Xudo uchunmi? Urush yoki tinchlik uchun amaliy kimyo? Elektron qanday rangda? Radiatsion kimyo. Radioaktivlik hodisasini kim kashf etgan? Radioaktivlik qanchalik xavfli? Kuchli energiya mavjudmi? Radiokimyo. Stereokimyo nima? Qaysi biri yaxshiroq: suv toshqini yoki metan halokati? Supramolekulyar kimyo. D.I. nima haqida gapirdi? Mendeleyev doktorlik dissertatsiyasida? Termokimyo. Texnik kimyo - ajratish oqlanadimi? Topokimyo sirt kimyosimi? Balki biz ko‘mir yoqmasligimiz kerakdir? Ko'mir kimyosi. Bizning davolanishimiz qanday? Farmakokimyo. Femtokimyo yangi narsami? Boshga zarba berish jinoyatmi yoki... fizik kimyomi? Birinchi fitokimyogarlar kimlar edi? Kislorod Yerdan qayerdan keladi va ko'rish tabiati qanday? Fotokimyo. Yuqori energiyali kimyo an'anaviy kimyodan qanday farq qiladi? Tezlashmasdan yashash mumkinmi? Kimyoviy kinetika va kataliz. Kimyoviy fizika fizik kimyodan nimasi bilan farq qiladi? O'rtacha odamning o'yinchisi nima? Kimyoviy texnologiya. Urushlarda kimyoning roli qanday? Kimyoviy qurollar. Xarid qilish paketlari, shinalar va irsiyat agentlari nimadan yasalgan? Makromolekulyar birikmalar kimyosi. Choyni sintez qilish mumkinmi? Tabiiy birikmalar kimyosi. Nima uchun bizga silikat kimyosi kerak? Qattiq jismlar kimyosi savolga qanday javob beradi: hetero normalmi? Organoelement birikmalarining kimyosi nima? Elektrokimyo, nima uchun bizga kerak? Chegaralarni nima itaradi Davriy jadval? Yadro kimyosi. Universitetsiz kimyoga qanday kirish mumkin? Qaysi kimyoviy element Rossiya nomi bilan atalgan? Kimyoviy elementlarning nomlari haqida.
Shrift hajmi: - +
Kimyoviy fizika fizik kimyodan nimasi bilan farq qiladi?
Kimyoviy fizika molekulalar va qattiq jismlarning elektron tuzilishini o'rganadi; molekulyar spektrlar, kimyoviy reaktsiyalarning elementar aktlari, yonish va portlash jarayonlari, ya'ni kimyoviy hodisalarning fizik tomonlari. Bu atama 1930 yilda nemis kimyogari A. Eyken tomonidan kiritilgan.
1920-yillarda tashkil topgan. rivojlanishi bilan bog'liq kvant mexanikasi va uning tushunchalaridan kimyoda foydalanish. Kimyoviy fizika va fizik kimyo o'rtasidagi chegara ixtiyoriydir. Element fizik kimyo aksincha: jismoniy ta'sirning kimyoviy natijasi (masalan, odamning boshiga g'isht bilan urish natijasida o'limi). Kimyoviy fizikaning yutuqlaridan biri nazariyani hisobga olish kerak tarmoqlangan zanjirli reaksiyalar.
Rossiya Fanlar akademiyasining Kimyoviy fizika instituti asoschisi N.N. Semyonov chuqur tadqiqotlar olib bordi zanjir reaktsiyalari. Ular kimyoviy reaktsiyaning o'z-o'zidan boshlanadigan bir qator bosqichlari bo'lib, ular boshlanganidan keyin oxirgi bosqich tugaguniga qadar davom etadi. Nemis kimyogari M.Bodenshteyn bunday reaksiyalar bo‘lishi mumkinligini birinchi marta 1913-yilda ilgari surganiga qaramay, zanjir reaksiya bosqichlarini tushuntiruvchi va uning tezligini ko‘rsatuvchi nazariya yo‘q edi. Zanjir reaktsiyasining kaliti shakllanishning dastlabki bosqichidir erkin radikal- juftlanmagan elektronga ega bo'lgan va shuning uchun kimyoviy jihatdan juda faol bo'lgan atom yoki atomlar guruhi. Bir marta hosil bo'lgach, u molekula bilan shunday o'zaro ta'sir qiladiki, reaksiya mahsulotlaridan biri sifatida yangi erkin radikal hosil bo'ladi. Keyin yangi hosil bo'lgan erkin radikal boshqa molekula bilan reaksiyaga kirishishi mumkin va reaktsiya erkin radikallarning o'xshashlarini hosil qilishiga biror narsa to'sqinlik qilmaguncha davom etadi, ya'ni. zanjir uzilib qolguncha.
Ayniqsa muhim zanjirli reaksiya 1923 yilda fiziklar G.A. tomonidan kashf etilgan tarmoqlangan zanjir reaksiyasidir. Kramers va I.A. Kristiansen. Bu reaksiyada erkin radikallar nafaqat faol maydonlarni hosil qiladi, balki ko'payib, yangi zanjirlar hosil qiladi va reaksiyani tezlashtiradi. Reaksiyaning haqiqiy rivojlanishi bir qator tashqi cheklovlarga bog'liq, masalan, u sodir bo'lgan tomir hajmi. Agar erkin radikallar soni tez ortib ketsa, reaksiya portlashga olib kelishi mumkin. 1926 yilda ikki talaba N.N. Semenov bu hodisani birinchi marta fosfor bug'ining suv bug'i bilan oksidlanishini o'rganayotganda kuzatgan. Bu reaksiya o'sha davrning kimyoviy kinetika qonunlariga ko'ra, xuddi shunday davom etmadi. Semenov bu nomuvofiqlikning sababini ular tarmoqlangan zanjir reaktsiyasi natijasi bilan shug'ullanishlarida ko'rdi. Ammo bunday tushuntirish o'sha paytda tan olingan vakolatli M. Bodenshteyn tomonidan rad etilgan kimyoviy kinetika . N.N. yana ikki yil davomida ushbu hodisani intensiv o'rganishni davom ettirdi. Semenov va S.N. Angliyada mustaqil ravishda tadqiqot olib borgan Hinshelvud va bu davrdan keyin Semenovning haqligi ma'lum bo'ldi.
N.N. Semenov monografiyasini (Zanjirli reaksiyalar. Leningrad, ONTI., 1934) nashr ettirib, unda koʻpgina kimyoviy reaksiyalar, jumladan polimerlanish reaksiyasi zanjir yoki tarmoqlangan zanjirli reaksiya mexanizmi yordamida amalga oshirilishini isbotladi. Keyinchalik bu aniqlandi uran-235 yadrolarining neytronlar tomonidan boʻlinish reaksiyasi ham tarmoqlangan zanjirli reaksiya xarakteriga ega.
1956 yilda Semenov Xinshelvud bilan birgalikda mukofotlangan Nobel mukofoti kimyo fanidan "kimyoviy reaksiyalar mexanizmi sohasidagi tadqiqotlar uchun". Semenov o'zining Nobel ma'ruzasida shunday dedi: "Zanjir reaktsiyasi nazariyasi asosiy muammoni hal qilishga yaqinlashish imkoniyatini ochadi. nazariy kimyo- reaksiyaga kirishuvchi zarrachalarning reaktivligi va tuzilishi o‘rtasidagi bog‘liqlik... Bu bilimlarsiz kimyoviy texnologiyani har qanday darajada boyitish yoki biologiyada hal qiluvchi muvaffaqiyatlarga erishish qiyin...”.
Rossiya Fanlar akademiyasining Kimyoviy fizika instituti (Moskva) va Rossiya Fanlar akademiyasining Kimyoviy fizika muammolari instituti (Chernogolovka) faoliyat yuritadi. “Kimyoviy fizika” jurnali bor. Siz o'qishingiz mumkin: Buchachenko A.L. Zamonaviy kimyoviy fizika: maqsadlar va taraqqiyot yo'llari // Kimyodagi yutuqlar. - 1987. - T. 56. - 11-son.
Fizika va kimyo 21-asrda texnologik taraqqiyotga bevosita hissa qo'shadigan fanlardir. Ikkala fan ham atrofdagi dunyoning ishlash qonuniyatlarini, uning tarkibidagi eng kichik zarrachalardagi o'zgarishlarni o'rganadi. Barcha tabiat hodisalari kimyoviy yoki jismoniy asos, bu hamma narsaga tegishli: porlash, yonish, qaynatish, erish, biror narsaning biror narsa bilan har qanday o'zaro ta'siri.
Maktabda hamma kimyo va fizika, biologiya va tabiatshunoslik asoslarini o'rgandi, lekin hamma ham o'z hayotini bu fanlar bilan bog'lamadi, hozir hamma ham ular orasidagi chegarani aniqlay olmaydi.
Fizika fani va kimyo fani o'rtasidagi asosiy farqlar nimada ekanligini tushunish uchun avvalo ularni diqqat bilan ko'rib chiqish va ushbu fanlarning asosiy tamoyillari bilan tanishish kerak.
Fizika haqida: harakat va uning qonunlari
Fizika shartnomalari to'g'ridan-to'g'ri o'rganish umumiy xususiyatlar atrofdagi dunyo, materiya harakatining oddiy va murakkab shakllari, tabiiy hodisalar, bu barcha jarayonlarning asosini tashkil qiladi. Fan turli moddiy ob'ektlarning sifatlarini va ular o'rtasidagi o'zaro ta'sirlarning namoyon bo'lishini o'rganadi. Fiziklar umumiy naqshlarni ham ko'rib chiqmoqdalar turli xil turlari materiya; bu birlashtiruvchi tamoyillar jismoniy qonunlar deb ataladi.

Fizika ko'p jihatdan asosiy fandir, chunki u ko'rib chiqadi moddiy tizimlar turli miqyosda eng keng tarqalgan. U hamma bilan juda yaqin aloqada tabiiy fanlar, fizika qonunlari biologik va geologik hodisalarni bir xil darajada belgilaydi. Hamma narsa kabi matematika bilan ham kuchli aloqa bor fizik nazariyalar raqamlar bilan tuzilgan va matematik ifodalar. Taxminan aytganda, intizom fizika qonunlariga asoslanib, atrofdagi dunyoning mutlaqo barcha hodisalarini va ularning paydo bo'lish qonuniyatlarini keng o'rganadi.

Kimyo: hamma narsa nimadan iborat?
Kimyo, birinchi navbatda, xossalar va moddalarni turli xil o'zgarishlar bilan birgalikda o'rganish bilan shug'ullanadi. Kimyoviy reaksiyalar- bu aralashtirish natijalari toza moddalar va yangi elementlarni yaratish.
Fan biologiya va astronomiya kabi boshqa tabiiy fanlar bilan chambarchas aloqada. Kimyo har xil turdagi moddalarning ichki tarkibini, moddaning tarkibiy qismlarining o'zaro ta'siri va o'zgarishini o'rganadi. Kimyo ham o'ziga xos qonun va nazariyalardan, qonuniyatlardan va ilmiy farazlardan foydalanadi.

Fizika va kimyo o'rtasidagi asosiy farqlar nimada?
Tabiatshunoslikka mansublik bu fanlarni ko'p jihatdan birlashtiradi, ammo ular o'rtasida umumiylikdan ko'ra ko'proq farqlar mavjud:
- Ikki tabiiy fan o'rtasidagi asosiy farq fizikani o'rganadi elementar zarralar(mikrodunyo, bu atom va nuklon darajalarini o'z ichiga oladi) va ma'lum bir joyda joylashgan moddalarning turli xususiyatlari agregatsiya holati. Kimyo atomlardan molekulalarning "yig'ilishi" jarayonlarini, moddaning boshqa turdagi moddalar bilan ma'lum reaktsiyalarga kirishish qobiliyatini o'rganish bilan shug'ullanadi.
- Biologiya va astronomiya singari, zamonaviy fizika ham o'zining uslubiy vositalarida ko'plab noratsional tushunchalarga imkon beradi, bu asosan Yerdagi hayotning paydo bo'lishi, koinotning paydo bo'lishi va falsafa bilan bog'liqlik haqidagi nazariyalarga taalluqlidir. "ideal" va "material". Kimyo juda yaqinroq bo'lib qoldi ratsional tamoyillar aniq fanlar, ham qadimgi alkimyodan, ham umuman falsafadan uzoqlashish.
- Jismlarning kimyoviy tarkibi jismoniy hodisalarda, ularning xossalari kabi o'zgarishsiz qoladi. Kimyoviy hodisalar moddaning yangi xossalari paydo bo'lishi bilan boshqasiga aylanishini o'z ichiga oladi; Bu fanlar o'rganadigan fanlar o'rtasidagi farqdir.
- Fizika tomonidan tasvirlangan hodisalarning keng sinfi. Kimyo ko'proq yuqori ixtisoslashtirilgan intizom, u fizikadan (makrodunyo va mikrodunyo) farqli o'laroq, faqat mikrodunyoni (molekulyar daraja) o'rganishga qaratilgan.
- Fizika fani moddiy jismlarni sifat va xossalari bilan, kimyo esa bu jismlarning tarkibi, ular tarkibidagi eng kichik zarrachalari va bir-biri bilan o‘zaro ta’sir qiladigan tarkibi bilan shug‘ullanadi.