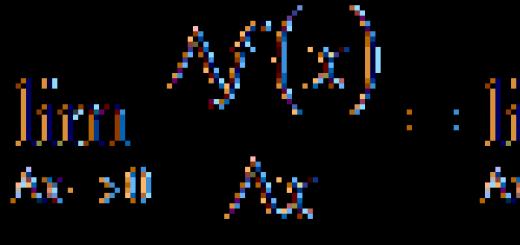Oksidlarning kimyoviy xossalari: asosiy, amfoter, kislotali
Oksidlar ikki kimyoviy elementdan tashkil topgan murakkab moddalar bo'lib, ulardan biri oksidlanish darajasiga ega bo'lgan kisloroddir ($-2$).
Oksidlarning umumiy formulasi: $E_(m)O_n$, bu yerda $m$ — $E$ element atomlari soni, $n$ — kislorod atomlari soni. Oksidlar bo'lishi mumkin qiyin(qum $SiO_2$, kvarts navlari), suyuqlik(vodorod oksidi $H_2O$), gazsimon(uglerod oksidlari: karbonat angidrid $CO_2$ va karbonat angidrid $CO$ gazlari). Kimyoviy xossalariga ko'ra oksidlar tuz hosil qiluvchi va tuz hosil qilmaydiganlarga bo'linadi.
Tuz hosil qilmaydi Bular gidroksidi yoki kislotalar bilan reaksiyaga kirishmaydigan va tuz hosil qilmaydigan oksidlardir. Ulardan bir nechtasi bor, ular tarkibida metall bo'lmaganlar mavjud.
Tuz hosil qiluvchi Bular kislotalar yoki asoslar bilan reaksiyaga kirishib, tuz va suv hosil qiluvchi oksidlardir.
Tuz hosil qiluvchi oksidlar orasida oksidlar mavjud asosiy, kislotali, amfoter.
Asosiy oksidlar- bular asoslarga mos keladigan oksidlardir. Masalan: $CaO$ $Ca(OH)_2 ga, Na_2O ga NaOH$ mos keladi.
Asosiy oksidlarning tipik reaktsiyalari:
1. Asosiy oksid + kislota → tuz + suv (almashinuv reaktsiyasi):
$CaO+2HNO_3=Ca(NO_3)_2+H_2O$.
2. Asosiy oksid + kislotali oksid → tuz (birikma reaktsiya):
$MgO+SiO_2(→)↖(t)MgSiO_3$.
3. Asosiy oksid + suv → ishqor (birikma reaksiya):
$K_2O+H_2O=2KOH$.
Kislotali oksidlar- bu kislotalarga mos keladigan oksidlar. Bu metall bo'lmagan oksidlar:
N2O5 $HNO_3, SO_3 - H_2SO_4, CO_2 - H_2CO_3, P_2O_5 - H_3PO_4$ ga, shuningdek yuqori oksidlanish darajasiga ega boʻlgan metall oksidlariga toʻgʻri keladi: $(Cr)↖(+6)O_3$ $H_2CrO_4, (MN) ga toʻgʻri keladi. +7 )O_7 — HMnO_4$.
Odatda kislota oksidi reaktsiyalari:
1. Kislota oksidi + asos → tuz + suv (almashinuv reaktsiyasi):
$SO_2+2NaOH=Na_2SO_3+H_2O$.
2. Kislota oksidi + asosli oksid → tuz (birikma reaksiya):
$CaO+CO_2=CaCO_3$.
3. Kislota oksidi + suv → kislota (birikma reaktsiyasi):
$N_2O_5+H_2O=2HNO_3$.
Bu reaktsiya faqat kislota oksidi suvda eriydigan bo'lsa mumkin.
Amfoterik sharoitga qarab asosiy yoki kislotali xossalarni namoyon qiluvchi oksidlar deyiladi. Bular $ZnO, Al_2O_3, Cr_2O_3, V_2O_5$. Amfoter oksidlar bevosita suv bilan birikmaydi.
Amfoter oksidlarning tipik reaksiyalari:
1. Amfoter oksid + kislota → tuz + suv (almashinuv reaktsiyasi):
$ZnO+2HCl=ZnCl_2+H_2O$.
2. Amfoter oksid + asos → tuz + suv yoki kompleks birikma:
$Al_2O_3+2NaOH+3H_2O(=2Na,)↙(\text"natriy tetragidroksoalyuminat")$
$Al_2O_3+2NaOH=(2NaAlO_2)↙(\text"natriy aluminat")+H_2O$.
Kimyo bo'yicha OGE ning 18-topshirida biz indikatorlar va pH, shuningdek eritmadagi ionlarga sifatli reaktsiyalar haqidagi bilimlarni namoyish qilamiz.
Kimyo fanidan 18-sonli OGE topshirig'i uchun nazariya
Ko'rsatkichlar
Indikator - bu atrof-muhitning pH darajasiga qarab rangini o'zgartiradigan kimyoviy moddadir.
Eng mashhur ko'rsatkichlar - fenolftalein, metil apelsin, lakmus va universal indikator. Quyidagi rasmdagi muhitga qarab ularning ranglari:
Va bu erda ko'rsatkichlarning ranglari hayotiy misollar bilan batafsilroq:

Biz indikatorlarni ko'rib chiqdik, keling, ionlarga sifatli reaktsiyalarga o'tamiz.
Ionlarga sifatli reaksiyalar
Kationlar va anionlarga sifatli reaksiyalar quyidagi jadvalda keltirilgan.

Kimyo bo'yicha OGE testida 18-topshiriqni qanday to'g'ri bajarish kerak?
Buning uchun taqdim etilgan variantlardan biriga sifatli reaktsiyani tanlashingiz va bu reaktiv ikkinchi modda bilan reaksiyaga kirishmasligiga ishonch hosil qilishingiz kerak.
Kimyodan 18-sonli OGE topshirig'ining tipik variantlarini tahlil qilish
Vazifaning birinchi versiyasi
Ikki modda va bu moddalarni farqlash uchun ishlatilishi mumkin bo'lgan reaktiv o'rtasidagi yozishmalarni o'rnating.
Moddalar:
A) Na2CO3 va Na2SiO3
B) K2CO3 va Li2CO3
B) Na2SO4 va NaOH
Reaktiv:
1) CuCl2
4) K3PO4
Keling, har bir ishni ko'rib chiqaylik.
Na2CO3 va Na2SiO3
- mis xlorid bilan reaksiya ikkala holatda ham sodir bo'lmaydi, chunki mis karbonat va silikat suvli eritmada parchalanadi.
- xlorid kislotasi bilan, natriy karbonat bo'lsa, gaz chiqariladi, silikat bo'lsa, cho'kma hosil bo'ladi - bu silikatlarga sifatli reaksiya
- fosfat bilan natriyga sifatli reaktsiyalar ham mavjud emas
K2CO3 va Li2CO3
- Ushbu moddalar mis xlorid bilan reaksiyaga kirishmaydi (aslida mis gidroksid cho'kmasi cho'kadi, ammo bu reaktsiya ikkita reagentni ajrata olmaydi)
- Ikkalasi ham karbonat angidridni chiqarish uchun xlorid kislotasi bilan reaksiyaga kirishadi.
- Bu moddalar magniy oksidi bilan reaksiyaga kirishmaydi, magniy oksidi esa ion almashish reaksiyalariga kirmaydi.
- fosfat bilan litiy fosfat holida cho'kadi , lekin kaliy yo'q
Bizda oxirgi variant qoldi - mis xlorid. Haqiqatan ham, mis gidroksidi natriy gidroksidi bilan cho'kadi, ammo sulfat bilan reaksiya sodir bo'lmaydi.
Dars mavzusi: GIA variantlarida ijodiy topshiriqlar
Dars o'tkaziladigan joy: 9-sinfda umumiy dars (Kimyo fanidan Davlat imtihoniga tayyorgarlik ko'rishda).
Dars davomiyligi: (60 min.).
Dars mazmuni:
Dars tizimli ravishda GIA variantlaridagi savollarga mos keladigan 3 qismga bo'lingan.
Gazsimon moddalarni olish. Gazsimon moddalarga (kislorod, vodorod, karbonat angidrid, ammiak) sifatli reaksiyalar (A 14).
Indikatorlar yordamida kislotalar va ishqorlarning eritma muhitining xarakterini aniqlash. Eritmadagi ionlarga (xlorid, sulfat, karbonat ionlari, ammoniy ionlari) sifatli reaksiyalar (A 14).
Oddiy moddalarning kimyoviy xossalari. Murakkab moddalarning kimyoviy xossalari. Eritmadagi ionlarga (xlorid, sulfat, karbonat ionlari, ammoniy ionlari) sifatli reaksiyalar. Gazsimon moddalarni olish. Gazsimon moddalarga (kislorod, vodorod, karbonat angidrid) sifatli reaktsiyalar (C 3).
Dars davomida o‘qituvchi multimediali taqdimotdan foydalanadi: “GIA variantlarida ijodiy topshiriqlar”, “Kimyo darslarida xavfsizlik choralari”, “GIA variantlarida ijodiy topshiriqlar” darsning 3-qismi uchun.
Darsning maqsadi: 9-sinf o‘quvchilarini kimyo fanidan Davlat imtihoniga aniq masalalar bo‘yicha tayyorlash.Ishning maqsadi: turli sinfdagi noorganik birikmalarning xossalari, ionlarga sifatli reaksiyalar haqidagi bilimlarni mustahkamlash.O‘quvchilarning kimyo fanidan olgan bilimlarini chuqurlashtirish, fanga qiziqishlarini rivojlantirish.
Dars maqsadlari :
- Chuqurlashtirish, tizimlashtirish va mustahkamlash,talabalarning turli gazlarni olish, yig`ish usullari va xossalari haqidagi bilimlari;
Tahlil qilish, taqqoslash, umumlashtirish va sabab-oqibat munosabatlarini o'rnatish qobiliyatini rivojlantirish;
Sizni ushbu mavzu bo'yicha GIA variantlari vazifalarini bajarish metodologiyasi bilan tanishtiring;
Kimyoviy reagentlar va kimyoviy asbob-uskunalar bilan ishlash ko'nikma va malakalarini shakllantirish;
Muayyan vaziyatlarda bilimlarni qo'llash ko'nikmalarini rivojlantirishga ko'maklashish;
Talabalarning dunyoqarashini kengaytirish, o'rganish motivatsiyasini oshirish, mustaqil faoliyat orqali talabalarni ijtimoiylashtirish;
Talabalarga nostandart vazifalarni hal qilishda haqiqiy tajriba orttirishga yordam berish;
Ta'lim va muloqot qobiliyatlarini rivojlantirish;
Bolalarda o'z-o'zini hurmat qilish va ularning faoliyatini nazorat qilish ko'nikmalarini rivojlantirishga ko'maklashish;
Talabalarni o'rta ta'limga kirishga tayyorlashga yordam bering.
Talabalar uchun maqsadlar:
GIA variantlarida (A-14, C3) ijodiy topshiriqlarni bajarish bilan tanishish;
Nostandart ijodiy muammolarni hal qilishni o'rganing;
Faoliyatingizni nazorat qiling va o'zingizni nazorat qiling.
(Talabalar o'qiydilar).
Dars turi:
Bilim, ko'nikma va ko'nikmalarni takomillashtirish darsi (ko'nikma va ko'nikmalarni shakllantirish, GIA variantlarida o'rganilganlarni maqsadli qo'llash bo'yicha dars)
bilimlarni umumlashtirish va tizimlashtirish darsi;
birlashtirilgan.
Ish shakllari:
Frontal, guruh, individual, jamoaviy.
O'qitish usullari va vositalari:Talabalarning uyda, darsda bajargan mustaqil ishi;individual ish, guruh ishi, laboratoriya tajribasi, doskada ishlash, AKTdan foydalanish, tarqatma materiallar va mavhum dunyo ob'ektlari.
Dars samaradorligi:
Dars davomida o'qituvchi o'quvchilarning faol faoliyati, jumladan, ijodiy faoliyat uchun sharoit yaratdi.
Uskunalar: sharlar, sovun pufakchalari, individual kartochkalar, topshiriq kartalari, amaliy ish topshiriqlari, uyga vazifa kartalari, fikrlash varag'i, “Men materialni qanday o'rgandim?” testi,kompyuter, proyektor, ekran,taqdimotlar. Jadvallar: eruvchanlik, indikatorlarning rangi, ionlarni aniqlash. Doskadagi jadvallar.
Reaktivlar: natriy karbonat, natriy xlorid va natriy sulfat, xlorid kislotasi, kumush nitrat, bariy xlorid, kaltsiy karbonat, suv, ammoniy xlorid. Ko'rsatkichlar: metil apelsin, fenolftalein, lakmus).
"Bizning kayfiyatimiz" testi
( Darsdan oldin talabalarga bolalar olishni istagan har qanday rangdagi kvadratlarni olish taklif etiladi:
Qizil - baquvvat (ishlashga tayyor).
Sariq - quvonch va yaxshi kayfiyatning rangi.
Moviy - tinchlik va muvozanat rangi.
Yashil zerikdi, lekin umid qilamanki, bu kayfiyat o'zgaradi.
Jigarrang - izolyatsiya.
Qora ma'yus.
Dars shiori: Gyote so'zlari: "Bilishning o'zi etarli emas, siz ham murojaat qilishingiz kerak.
Buni xohlashning o'zi etarli emas, buni qilish kerak."
Darslar davomida:
Qizdirish; isitish:
Elektrolitik dissotsilanish nazariyasi asoschisi (Arrhenius).
Elektrolitlarning ionlarga parchalanish jarayoni deyiladi? (ED).
Qanday moddalar elektrolitlar deb ataladi? (Suvli eritmalari yoki eritmalari elektr tokini o'tkazadigan moddalar).
Musbat zaryadlangan ionlar (kationlar) deyiladi.
Manfiy zaryadlangan ionlar (anionlar) deyiladi.
Ishqorlar dissotsilanganda ionlar hosil bo'ladi (gidroksid ionlari).
Ion almashinish reaksiyalarining vujudga kelish sharoitlarini sanab bering (ion almashish reaksiyalari uch holatda tugaydi: 1. Reaksiya natijasida cho’kma hosil bo’ladi; 2. ozgina ajraladigan modda yoki suv; 3. gazsimon modda. shakllantirildi) (talaba javoblari).
Kislotalar dissotsilanganda ionlar (vodorod ionlari) hosil bo'ladi.
Darsning birinchi qismi.
Gazsimon moddalarni olish. Gazsimon moddalarga (kislorod, vodorod, karbonat angidrid, ammiak) sifatli reaktsiyalar
Bilish kerak:
Gazlarning fizik va kimyoviy xossalari (vodorod, kislorod, karbonat angidrid, ammiak).
Gazni yig'ish usullari.
Gazlarni ishlab chiqarish uchun qurilmalarning nomi va ishlashi
Sanoat va laboratoriyalarda gazlarni olishning asosiy usullari
Gazni aniqlash ( sifatli reaktsiyalar) .
1. Gazlarning xilma-xilligi. O‘zingiz bilgan gazlarni guruhlarga taqsimlang (individual ish – o‘quvchilar topshiriqni alohida varaqlarda bajaradilar, javoblar ekranga yoziladi, o‘zaro test tashkil etiladi, o‘quvchilar baholanadi).
Gazsimon moddalarning formulalari qog'oz varaqlariga bosiladi va oldindan doskaga joylashtiriladi:
O 2 , CO, H 2 ,YO'Q 2 , CO 2 , N 2 , N.H. 3 , H 2 S, CI 2 , HCI.
1) gazlar - oddiy moddalar;
2) gazlar - oksidlar;
3) rangli gazlar;
4) xarakterli hidli gazlar;
Javob: 1) Oddiy moddalar: N 2 , O 2 , H 2 ,Cl 2 .
2) Oksidlar: CO, CO 2 ,YO'Q 2 .
3) Rangli gazlar: Cl 2 ,YO'Q 2 .
4) Xarakterli hidli gazlar: Cl 2 ,YO'Q 2 , N.H. 3 , H 2 S, HCl.
2. To'pni qanday gaz bilan to'ldirishini aniqlang. Buning uchun: Sizga berilgan gazlarning havo zichligini hisoblang.
Turli xil rangdagi sharlar turli balandliklarda joylashgan taxtaga osilgan. 5 daqiqa ichida talabalar formulalari quyida keltirilgan gazlardan qaysi gaz har bir to'pni to'ldirishini aniqlashlari kerak: NH 3 , CO 2 , N 2 , HAQIDA 2 .
Biz guruhlar yaratamiz. Har bir guruh o‘z gazini oladi (suyultirilgan gaz tashiladigan ballonlarning rangiga mos keladigan boshqa rangdagi sharcha. Masalan, kislorod: shar ko‘k rangda), uning xossalarini guruh aniqlaydi.1-guruh. - N 2 , 2-guruh - O 2 , 3-guruh - CO 2 , 4-guruh - NH 3 . Talabalar ham javob berishadi: nega to'plar turli balandliklarda joylashgan?
3. Tajriba : Nima uchun havo pufakchalari pastga uchadi? (Suv quroli). Bolalar javob beradilar.
Guruhlarda ishlash:
4. Sizga berilgan gazlarning fizik xossalarini ayting. Qisqacha. (Guruhlarda ishlash).
Kislorod -
Vodorod -
Ammiak -
Karbonat angidrid -
5.Savolga javob bering: Gazlarni yig'ishning qanday usullarini bilasiz? Keling, slaydni ko'rib chiqaylik:
Gazlarni yig'ish uchun asboblar.2) Qanday gazlarni to'plash mumkin1 va 2-rasmdagi qurilma?
Qaysilari havodan engilroq 1, og'irroq - 2.
3) 3-rasmdagi qurilma bilan qanday gazlarni yig'ish mumkin?
Suvda erimaydigan gazlar.
4) Qaysi qurilma raqamidan foydalanasiz?
1-guruh - vodorod? 2 - kislorod?
HAQIDA  Biz ushbu masala bo'yicha Davlat inspektsiyasining ko'rsatmalariga muvofiq ishlayapmiz:
Biz ushbu masala bo'yicha Davlat inspektsiyasining ko'rsatmalariga muvofiq ishlayapmiz:
A) ammiak B) kislorod
C) karbonat angidrid D) vodorod sulfidi

Rasmda qaysi gazni ishlab chiqarish ko'rsatilgan?
A) ammiak B) kislorod
C) karbonat angidrid D) vodorod
6 . Biz GIA masalalari bo'yicha gazlarni ishlab chiqarishning laboratoriya va sanoat usullarini ishlab chiqamiz: (tarqatma materialga muvofiq, 1-jadval.)
TO  ular qanday gaz oladilar?
ular qanday gaz oladilar?
A) ammiak B) kislorod
C) karbonat angidrid D) vodorod
 Siz qanday gaz olasiz?
Siz qanday gaz olasiz?
A) ammiak
B) kislorod
B) karbonat angidrid
D) vodorod

Siz qanday gaz olasiz?
A) ammiak
B) kislorod
B) karbonat angidrid
D) vodorod

Siz qanday gaz olasiz?
A) ammiak B) kislorod C) karbonat angidrid D) vodorod
 Siz qanday gaz olasiz?
Siz qanday gaz olasiz?
A) ammiak B) kislorod
B) karbonat angidrid D) vodorod
7 .Gazlarni bir-biridan qanday ajratish mumkin?

Qanday gaz aniqlanmoqda?
A) ammiak B) kislorod
C) karbonat angidrid D) vodorod

Balonlar qanday gaz bilan to'ldirilgan?
A) vodorod sulfidi B) kislorod
C) karbonat angidrid D) vodorod

Qanday gaz uzatilmoqda?
A) ammiak B) kislorod
C) karbonat angidrid D) vodorod
A14 2012 topshiriqlarining o'ziga xos xususiyati chizmalar bo'yicha savollar edi.
Shunday qilib, GIA topshiriqlarida chizmalar bo'yicha quyidagi savollar mavjud:
Qanday gaz yig'iladi? (Yig'ish usullari)
Siz qanday gaz olasiz? (Olish usullari)
Qanday gaz aniqlanmoqda? (identifikatsiya)
Taqdimot
2.Darsning ikkinchi qismi.
Indikatorlar yordamida kislotalar va ishqorlarning eritma muhitining xarakterini aniqlash.
Eritmadagi ionlarga (xlorid, sulfat, karbonat ionlari, ammoniy ionlari) sifatli reaktsiyalar.
Xavfsizlik qoidalari (taqdimot).
1. Laboratoriya tajribasi.
Kimyo darslarida xavfsizlik choralari (Multimedia taqdimoti)
Guruhlarda sizga berilgan moddalarni aniqlang.
1-guruh
HCI), ishqorlar (NaOH) va suv (H 2 O). Berilgan moddalardan (metil apelsin) foydalanib, qaysi probirkada har bir modda borligini aniqlang.
2-guruh
3-guruh
1.2-ilova (1-3-guruhlar uchun)
Amaliy ish № 1
Dars maqsadlari:
Uskunalar: doska, bo'r, jadval "Kislotalar va ishqorlar eritmalarining tabiatini indikatorlar yordamida aniqlash", "Kislotalar, asoslar, tuzlarning suvda eruvchanligi jadvali", probirkalar solingan stend, spirt lampasi, gugurt, ushlagich sinov naychalari uchun.
Reaktivlar: eritmalar: natriy gidroksid, xlorid kislota, suv, indikator - metil apelsin.
1-guruh
Raqamlar ostidagi uchta probirkada eritmalar mavjud: kislotalar (HCI), ishqorlar (NaOH) va suv (H 2 O). Berilgan indikator moddalardan (metil apelsin, fenolftalein, lakmus) foydalanib, qaysi probirkada har bir modda borligini aniqlang.
Foydalanish bo'yicha ko'rsatmalar.
Topshiriq: uchta raqamlangan probirkada (1, 2, 3) quyidagi moddalar mavjud: kislotalar (HCI), ishqorlar (NaOH) va suv (H 2 O).
Xarakterli reaksiyalardan foydalanib, qaysi probirkada bu moddalar borligini aniqlang.
1, 2, 3 tajribalarni bajaring.
No1 probirkaga 2 - 3 ml eritma quyib, unga 1 - 2 tomchi metiloranj indikator, lakmus, fenolftalein eritmasidan qo`shing, eritmaning rangi qanday o`zgargan?
No2 probirkaga metiloranj indikator, lakmus, fenolftalein eritmasidan quying.
Nimani kuzatyapsiz?
No3 probirkaga metiloranj indikator, lakmus, fenolftalein eritmasidan quying.
Nimani kuzatyapsiz?
3. Jadvalni to'ldiring.
Daftaringizga kerakli eslatmalarni yozing, xulosani ovoz chiqarib ayting (guruhdan bitta talaba gapiradi). Tarqatma materiallar 1.2-ilovaga qarang.
Rang o'zgarishikislotali muhitda
Ishqoriy muhitda rang o'zgarishi
Amaliy ish № 1
Mavzu: Ionlarga sifatli reaksiyalar.
Ishning maqsadi: noorganik moddalarni aniqlash uchun xarakterli reaktsiyalardan foydalanish.
Kimyoviy tajribalarni o'tkazish ko'nikmalarini oshirish;
Amaliy usulda ion almashinish reaksiyalarini o'tkazish shartlarini tasdiqlang.
Dars maqsadlari:
Ta'limiy: kimyoviy tajriba yordamida talabalarning "Elektrolitik dissotsilanish nazariyasi" (noorganik moddalarga xarakterli reaktsiyalar) bo'limidagi bilim, ko'nikma va ko'nikmalarini mustahkamlash.
Rivojlantiruvchi: fikrlashni rivojlantirishga yordam berish (tahlil qilish, taqqoslash, asosiy narsani ta'kidlash, sabab-oqibat munosabatlarini o'rnatish), kognitiv qiziqishlarni rivojlantirish.
Tarbiyaviy: shaxsiy fazilatlarni shakllantirishga yordam berish (mas'uliyat, kollektivizm, tashabbus).
Dars turi: bilim, ko'nikma va malakalarni amaliyotda qo'llash.
Dars turi: amaliy ish.
O`qitish usullari: tahliliy, qiyosiy, umumlashtiruvchi, tasniflash.
2-guruh
Raqamli uchta probirkada eritmalar mavjud: natriy karbonat, natriy xlorid va natriy sulfat. Berilgan moddalardan (xlorid kislota, kumush nitrat, bariy xlorid) foydalanib, qaysi probirkada har bir modda borligini aniqlang.
Foydalanish bo'yicha ko'rsatmalar.
Ushbu tajribani bajarish uchun har bir raqamlangan probirkaning tarkibini uchta namunaga bo'ling.
Jarayon:
Ishning bajarilishini quyidagi shaklda qayd etish uchun jadval:
Nimani kuzatyapsiz?
Nimani kuzatyapsiz?
Nimani kuzatyapsiz?
Reaksiya tenglamasini molekulyar, to‘liq ionli va qaytarilgan ionli shakllarda yozing.
3. Jadvalni to'ldiring.
4. Umumiy xulosa chiqaring. Ishning eksperimental qismi natijalarini hisobot jadvaliga yozing. Hisobotni tayyorlashda §§ 2,3,4 dan foydalaning.
Kerakli eslatmalarni qiling
Amaliy ish № 1
Mavzu: Ionlarga sifatli reaksiyalar.
Ishning maqsadi: noorganik moddalarni aniqlash uchun xarakterli reaktsiyalardan foydalanish.
Kimyoviy tajribalarni o'tkazish ko'nikmalarini oshirish;
Amaliy usulda ion almashinish reaksiyalarini o'tkazish shartlarini tasdiqlang.
Dars maqsadlari:
Tarbiyaviy: kimyoviy eksperiment yordamida talabalarning "Elektrolitik dissotsilanish nazariyasi" (noorganik moddalarga xarakterli reaktsiyalar) bo'limidagi bilim, ko'nikma va ko'nikmalarini mustahkamlash.
Rivojlantiruvchi: fikrlashni rivojlantirishga yordam berish (tahlil qilish, taqqoslash, asosiy narsani ta'kidlash, sabab-oqibat munosabatlarini o'rnatish), kognitiv qiziqishlarni rivojlantirish.
Tarbiyaviy: shaxsiy fazilatlarni shakllantirishga yordam berish (mas'uliyat, kollektivizm, tashabbus).
Dars turi: bilim, ko'nikma va malakalarni amaliyotda qo'llash.
Dars turi: amaliy ish.
O`qitish usullari: tahliliy, qiyosiy, umumlashtiruvchi, tasniflash.
Uskunalar: doska, bo`r, kislotalar, asoslar, tuzlarning suvda eruvchanlik jadvali, probirkalar solingan stend, spirt lampasi, gugurt, probirka ushlagichi.
Reaktivlar: eritmalar: xlorid kislota, suv, indikator - kumush nitrat, kaltsiy karbonat, natriy karbonat va natriy xlorid, xlorid kislota, ammoniy xlorid.
3-guruh
Uchta raqamlangan probirkada qattiq moddalar mavjud: kaltsiy karbonat, ammoniy xlorid va natriy xlorid. Berilgan moddalardan (xlorid kislota, kumush nitrat, natriy gidroksid) foydalanib, qaysi probirkada har bir modda borligini aniqlang.
Foydalanish bo'yicha ko'rsatmalar.
Ushbu tajribani bajarish uchun har bir raqamlangan probirkaning tarkibini uchta namunaga bo'ling.
Jarayon:
1. Ishning bajarilishini quyidagi shaklda qayd etish jadvali:
2. 1, 2, 3-tajribalarni bajaring.No1 probirkaga kumush nitrat eritmasini quying.
Nimani kuzatyapsiz?
Reaksiya tenglamasini molekulyar, to‘liq ionli va qaytarilgan ionli shakllarda yozing.
No2 probirkaga xlorid kislota eritmasini quying.
Nimani kuzatyapsiz?
Reaksiya tenglamasini molekulyar, to‘liq ionli va qaytarilgan ionli shakllarda yozing.
No3 probirkaga natriy gidroksid eritmasini quying.
Nimani kuzatyapsiz?
Reaksiya tenglamasini molekulyar, to‘liq ionli va qaytarilgan ionli shakllarda yozing.
3. Jadvalni to'ldiring.
4. Umumiy xulosa chiqaring. Ishning eksperimental qismi natijalarini hisobot jadvaliga yozing. Hisobotni tayyorlashda §§ 2,3,4 dan foydalaning.
Kerakli eslatmalarni qilingdaftarda xulosa aytiladi. (Guruhdan bitta talaba gapiradi). Tarqatma materiallar 1.2-ilovaga qarang.
3. Darsning uchinchi qismi
Oddiy moddalarning kimyoviy xossalari. Murakkab moddalarning kimyoviy xossalari.
Eritmadagi ionlarga (xlorid, sulfat, karbonat ionlari, ammoniy ionlari) sifatli reaksiyalar.
Gazsimon moddalarni olish.
Gazsimon moddalarga (kislorod, vodorod, karbonat angidrid, ammiak) sifatli reaktsiyalar
Ijodiy topshiriqlar, vazifa C 3, vazifalari qiyin.
3. Har bir guruhga bittadan birlashtirilgan masalani yechish taklif etiladi. Guruh birgalikda qaror qiladi. Yechim doskaga yoziladi.
3.1 : Pavel Bajovning "Mis tog'ining bekasi" ertakida go'zal bezak tosh - malaxit haqida so'z boradi, undan vazalar, qutilar va zargarlik buyumlari tayyorlanadi. Malaxitning kimyoviy formulasi (CuOH) 2 CO 3 . Malaxitning termal parchalanishi paytida uchta murakkab modda hosil bo'ladi: bitta qora qattiq va ikkita gazsimon. Hosil bo'lgan gazsimon moddalardan biri ohak suvidan o'tganda, cho'kindi hosil bo'lishi sababli bulutli bo'ladi.
Hosil bo'lgan cho'kmaning kimyoviy formulasini va nomini yozing. Amalga oshirilgan reaksiyalar uchun ikkita molekulyar tenglamani yozing.
Javob:t 0
(CuOH) 2 CO 3 → 2CuO + CO 2 +H 2 O
Malaxit
CO 2 +Ca(OH) 2 → CaCO 3 ↓+H 2 O
Bu reaktsiya uglerod oksidini aniqlash uchun ishlatiladi (IV).
3.2: X moddasi 1 alyuminiyni sariq kukun bilan reaksiyaga kiritish natijasida olinadi. Suv X ga ta'sir qilganda 1 chirigan tuxum hidli zaharli gaz ajralib chiqadi. Bu gaz yonib, X moddani hosil qiladi 2 o'tkir hid bilan. X ni aniqlang 1 ularning 2. Boradigan reaksiyalar tenglamalarini yozing. X moddaning molyar massasini ko'rsating 2.
Javob:
2Al +3S → Al 2 S 3
Al 2 S 3 + 6 N 2 HAQIDA→ 3H 2 S + 2Al(OH) 3
2 H 2 S + 3 O 2 → 2 SO 2 + 2H 2 HAQIDA
Al 2 S 3 - X 1 , SO 2 - X 2 M (SO 2 ) = 64 g/mol
Vodorod sulfidi bilan barcha tajribalar dudbo'ronda o'tkaziladi!
3.3: Moddaning sifat tarkibini aniqlash uchun o‘quvchilarga 1 kg 1854 yilda kumushdan 270 marta qimmat bo‘lgan, o‘rtada esa metall tuzi berildi.XXasr allaqachon engil metall konstruktsiyalarni ishlab chiqarish uchun keng qo'llanilgan. Berilgan tuzning kristallarini suvda eritib bo‘lgach, o‘quvchilar hosil bo‘lgan tiniq eritmani ikkita probirkaga quydilar.
Ulardan biriga bir necha tomchi natriy gidroksid eritmasi qo'shildi va jelga o'xshash oq cho'kma hosil bo'ldi. Tuz eritmasi bo'lgan boshqa probirkaga bir necha tomchi bariy xlorid eritmasi qo'shildi, bu oq rangli sutga o'xshash cho'kma hosil qildi.
Berilgan tuzning kimyoviy formulasini va nomini yozing. Uni tanib olish jarayonida amalga oshirilgan reaksiyalar uchun ikkita tenglama tuzing.
Javob:
Al 2 (SO 4 ) 3 +6NaOH→3Na 2 SO 4 +2Al(OH) 3 ↓ jelga o'xshashoqcho'kindi
Al 2 ( SO 4 ) 3 + 3 BaCl 2 → 3 BaSO 4 ↓+ 2 AlCl 3
oq, sutli cho'kindi
Darsni yakunlash. Reflektsiya. Baholash.
Baholovchi-reflektiv blok
Ishlaringizni guruhlarda tahlil qilaylik. Har bir guruh sardoriga so‘z beriladi.
Bugun darsda qanday savollar bilan tanishdik?
Ushbu savollarning qaysi biri sizga eng qiyin bo'ldi?
Sinov 3-ilova
Materialni qanday o'rgandim?
Uy vazifasi (topshiriq har bir talaba uchun chop etiladi)
Vazifa № 1.
Tajribalarni o'tkazish uchun tadqiqotchilarga suvda erimaydigan sariq kristallar bo'lgan modda berildi. Ushbu modda gugurt yasashda va kauchukni vulkanizatsiya qilishda qo'llanilishi ma'lum. Chiqarilgan moddaning qizdirilganda konsentrlangan sulfat kislota bilan o'zaro ta'siri natijasida gaz oksidi va suv hosil bo'ladi. Va hosil bo'lgan oksid bariy gidroksid eritmasidan o'tkazilganda, gazning keyingi o'tishi bilan eriydigan oq cho'kma hosil bo'ladi.
Kimyoviy formulani yozing va ikkinchi tajriba natijasida olingan tuzni nomlang. O‘quvchilar tuzni o‘rganishda o‘tkazgan tajribalariga mos keladigan ikkita molekulyar reaksiya tenglamalarini yozing.
t 0
S+2H 2 SO 4 = 3SO 2 + 2H 2 O
SO 2 +Ba(OH) 2 = BaSO 4 ↓ + 2H 2 O
Bariy sulfat
(Dars oxirida kvadratni boshqa rangdagi kvadratga o'zgartirmoqchi bo'lgan o'quvchilarga buni qilish so'raladi. "Bizning kayfiyatimiz" testi).
1-ilova.
Jadval. Ionni aniqlash
Reaktsiya natijasi
H +
Ko'rsatkichlar
Rang o'zgarishi
Ag+
Cl -
Oq cho'kma
BILANu 2+
OH -
S 2-
Moviy cho'kindi
Qora cho'kindi
Olovni ko'k-yashil rangga bo'yash
Fe 2+
OH -
Vaqt o'tishi bilan jigarrang rangga aylangan yashil rangli cho'kindi
Fe 3+
OH -
Jigarrang cho'kindi
Zn 2+
OH -
S 2-
Oq cho'kma, agar ortiqcha bo'lsaOH - eriydi
Oq cho'kma
Al 3+
OH -
Oq, jelega o'xshash cho'kma, ortiqcha bo'lsaOH - eriydi
N.H. 4 +
OH -
Ammiak hidi
Ba 2+
SO 4 2-
Oq cho'kma
Olovni sariq-yashil rangga bo'yash
Ca 2+
CO 3 2-
Oq cho'kma
Olovli g'ishtni qizil rangga bo'yash
Na +
Olov rangi sariq
K +
Olov rangi binafsha (kobalt shishasi orqali)
Cl -
Ag +
Oq cho'kma
H 2 SO 4 *
O'tkir hidli rangsiz gazning chiqishi (HCl)
Br -
Ag +
H 2 SO 4 *
Sarg'ish cho'kindi
TanlashSO 2 VaBr 2 (jigarrang rang)
I -
Ag +
H 2 SO 4 +
Sariq cho'kma
TanlashH 2 SVaI 2 (siyohrang)
SO 3 2-
H +
TanlashSO 2 - fuchsin va binafsha siyoh eritmasini oqartiruvchi o'tkir hidli gaz
CO 3 2-
H +
Ohak suvida loyqalikka olib keladigan hidsiz gazning chiqishi
CH 3 COO -
H 2 SO 4
Sirka kislotasining hidi
YO'Q 3 -
H 2 SO 4 (konk.) vaCu
Jigarrang gazning chiqishi
SO 4 2-
Ba 2+
Oq cho'kma
P.O. 4 3-
Ag +
Sariq cho'kma
OH -
Ko'rsatkichlar
Ko'rsatkichlar rangini o'zgartirish
2-ilova.
Amaliy ish № 1
Mavzu: Ionlarga sifatli reaksiyalar.
Ishning maqsadi: noorganik moddalarni aniqlash uchun xarakterli reaktsiyalardan foydalanish.
Kimyoviy tajribalarni o'tkazish ko'nikmalarini oshirish;
Amaliy usulda ion almashinish reaksiyalarini o'tkazish shartlarini tasdiqlang.
Dars maqsadlari:
Ta'limiy: kimyoviy tajriba yordamida talabalarning "Elektrolitik dissotsilanish nazariyasi" (noorganik moddalarga xarakterli reaktsiyalar) bo'limidagi bilim, ko'nikma va ko'nikmalarini mustahkamlash.
Rivojlantiruvchi: fikrlashni rivojlantirishga yordam berish (tahlil qilish, taqqoslash, asosiy narsani ta'kidlash, sabab-oqibat munosabatlarini o'rnatish), kognitiv qiziqishlarni rivojlantirish.
Tarbiyaviy: shaxsiy fazilatlarni shakllantirishga yordam berish (mas'uliyat, kollektivizm, tashabbus).
Dars turi: bilim, ko'nikma va malakalarni amaliyotda qo'llash.
Dars turi: amaliy ish.
O`qitish usullari: tahliliy, qiyosiy, umumlashtiruvchi, tasniflash.
Uskunalar: doska, bo`r, kislotalar, asoslar, tuzlarning suvda eruvchanlik jadvali, probirkalar solingan stend, spirt lampasi, gugurt, probirka ushlagichi.
Reaktivlar: natriy karbonat, natriy xlorid va natriy sulfat, xlorid kislotasi, kumush nitrat, bariy xlorid.
2-guruh
Raqamli uchta probirkada eritmalar mavjud: natriy karbonat, natriy xlorid va natriy sulfat. Berilgan moddalardan (xlorid kislota, kumush nitrat, bariy xlorid) foydalanib, qaysi probirkada har bir modda borligini aniqlang.
Foydalanish bo'yicha ko'rsatmalar.
Ushbu tajribani bajarish uchun har bir raqamlangan probirkaning tarkibini uchta namunaga bo'ling.
Jarayon:
Ishning bajarilishini quyidagi shaklda qayd etish uchun jadval:
No1 probirkaga bariy xlorid eritmasini quying.
Nimani kuzatyapsiz?
Reaksiya tenglamasini molekulyar, to‘liq ionli va qisqartirilgan ionli shakllarda yozing.
No2 probirkaga xlorid kislota eritmasini quying.
Nimani kuzatyapsiz?
Reaksiya tenglamasini molekulyar, to‘liq ionli va qaytarilgan ionli shakllarda yozing.
No3 probirkaga kumush nitrat eritmasini quying.
Nimani kuzatyapsiz?
Reaksiya tenglamasini molekulyar, to‘liq ionli va qaytarilgan ionli shakllarda yozing.
3. Jadvalni to'ldiring.
4. Umumiy xulosa chiqaring. Ishning eksperimental qismi natijalarini hisobot jadvaliga yozing. Hisobotni tayyorlashda §§ 2,3,4 dan foydalaning.
Kerakli eslatmalarni qiling daftarda xulosa aytiladi. (Guruhdan bitta talaba gapiradi).
3-ilova
Sinov
Materialni qanday o'rgandim?
1. Qattiq bilim oldi, barcha materialni o‘zlashtirdi 9-10 ball
2. Materialni qisman o‘zlashtirgan 7-8 ball
3. Men ko'p narsani tushunmadim, men hali ham 4-6 ball ishlashim kerak
4. Guruhlarda qatnashganingiz uchun o'zingizga qanday baho qo'ygan bo'lardingiz? (Bu erda o'zingizga ushbu reytingni bering).
Arxangelsk viloyati Severodvinsk shahridagi “11-sonli umumta’lim maktabi” munitsipal ta’lim muassasasida “Kimyo” 8-sinf darsligi uchun I.I.Novoshinskiy, N.S.Novoshinskayalar tomonidan amaliy ish daftaridan foydalangan holda, 8-sinfda kimyo o‘qituvchisi O.A.Olkina tomonidan o‘tkazilgan dars (parallel). ).
Darsning maqsadi: I.I.Novoshinskiy, N.S.Novoshinskayaning “Kimyo 8-sinf” darsligi uchun amaliy ish daftaridan foydalanib, turli ko‘rsatkichlar, jumladan, tabiiy ko‘rsatkichlar yordamida eritma muhitining reaksiyasini aniqlash bo‘yicha o‘quvchilarda ko‘nikmalarni shakllantirish, mustahkamlash va nazorat qilish.
Dars maqsadlari:
- Tarbiyaviy. Amaliy ish topshiriqlarini bajarish asosida quyidagi tushunchalarni mustahkamlang: indikatorlar, muhit reaksiyasi (turlari), pH, filtrat, filtrlash. Talabalarning "moddaning eritmasi (formula) - pH qiymati (raqamli qiymat) - muhitning reaktsiyasi" munosabatini aks ettiruvchi bilimlarini sinab ko'ring. Talabalarga Arxangelsk viloyatida tuproqning kislotaliligini kamaytirish yo'llari haqida gapirib bering.
- Rivojlanish. Amaliy ish davomida olingan natijalarni tahlil qilish, ularni umumlashtirish, shuningdek, xulosa chiqarish qobiliyatiga asoslangan talabalarning mantiqiy tafakkurini rivojlantirishga ko'maklashish. Qoidani tasdiqlang: amaliyot nazariyani isbotlaydi yoki rad etadi. Taqdim etilgan turli xil echimlar asosida talabalar shaxsining estetik fazilatlarini shakllantirishni davom ettirish, shuningdek, bolalarning o'rganilayotgan "Kimyo" faniga qiziqishini qo'llab-quvvatlash.
- Tarbiyalash. Talabalarning amaliy ish topshiriqlarini bajarish, mehnatni muhofaza qilish va xavfsizlik qoidalariga rioya qilish, shu jumladan filtrlash va isitish jarayonlarini to'g'ri bajarish ko'nikmalarini rivojlantirishni davom ettirish.
Amaliy ish №6 “Atrof muhitning pH ni aniqlash”.
Talabalar uchun maqsad: Turli ob'ektlar eritmalari (kislotalar, ishqorlar, tuzlar, tuproq eritmasi, ba'zi eritmalar va sharbatlar) muhitining reaktsiyasini aniqlashni o'rganish, shuningdek o'simlik ob'ektlarini tabiiy ko'rsatkichlar sifatida o'rganish.
Uskunalar va reagentlar: probirkalar solingan stend, tiqin, shisha tayoqcha, halqali stend, filtr qog‘oz, qaychi, kimyoviy voronka, stakan, chinni ohak, mayda qirg‘ich, toza qum, universal indikator qog‘oz, sinov eritmasi, tuproq, qaynatilgan suv , mevalar, rezavorlar va boshqa o'simlik materiallari, natriy gidroksid va sulfat kislota eritmasi, natriy xlorid.
Darslar davomida
Yigitlar! Biz allaqachon suvli eritmalar muhitining reaktsiyasi, shuningdek indikatorlar kabi tushunchalar bilan tanishdik.
Suvli eritmalarda qanday reaksiya turlarini bilasiz?
- neytral, ishqoriy va kislotali.
Ko'rsatkichlar nima?
- muhit reaktsiyasini aniqlash uchun ishlatilishi mumkin bo'lgan moddalar.
Qanday ko'rsatkichlarni bilasiz?
- eritmalarda: fenolftalein, lakmus, metil apelsin.
- quruq: universal indikator qog'ozi, lakmus qog'ozi, metil apelsin qog'ozi
Suvli eritmalarning reaksiyasini qanday aniqlash mumkin?
- nam va quruq.
Atrof-muhitning pH darajasi qanday?
- Eritmadagi vodorod ionlarining pH qiymati (pH=– log)
Qaysi olim pH tushunchasini kiritganini eslaylik?
- Daniyalik kimyogari Sorensen.
Juda qoyil!!! Endi 21-betdagi amaliy ish uchun daftarni oching va 1-topshiriqni o'qing.
Vazifa No 1. Universal indikator yordamida eritmaning pH qiymatini aniqlang.
Keling, kislotalar va ishqorlar bilan ishlashda qoidalarni eslaylik!
1-topshiriqdan tajribani yakunlang.
Xulosa chiqaring. Shunday qilib, agar eritma pH = 7 bo'lsa, muhit neytral, pH da< 7 среда кислотная, при pH >7 ishqoriy muhit.
Vazifa No 2. Tuproq eritmasini oling va universal indikator yordamida uning pH ni aniqlang.
21-bet 22-betdagi topshiriqni o'qing, reja bo'yicha topshiriqni bajaring, natijalarni jadvalga kiriting.
Keling, isitish moslamalari (spirtli pechka) bilan ishlashda xavfsizlik qoidalarini eslaylik.
Filtrlash nima?
- aralashmani ajratish jarayoni, bu g'ovakli materialning turli o'tkazuvchanligiga asoslangan - aralashmani tashkil etuvchi zarrachalarga nisbatan filtrat.
filtrat nima?
- filtrlashdan so'ng olingan aniq eritmadir.
Natijalarni jadval shaklida taqdim eting.
Tuproq eritmasi muhitining reaksiyasi qanday?
- Nordon
Mintaqamizda tuproq sifatini yaxshilash uchun nima qilish kerak?
- CaCO 3 + H 2 O + CO 2 = Ca(HCO 3) 2
Ishqoriy reaktsiya muhitiga ega bo'lgan o'g'itlarni qo'llash: maydalangan ohaktosh va boshqa karbonatli minerallar: bo'r, dolomit. Arxangelsk viloyatining Pinejskiy tumanida karst g'orlari yaqinida ohaktosh kabi mineral konlari mavjud, shuning uchun unga kirish mumkin.
Xulosa chiqaring. Olingan tuproq eritmasining reaktsiyasi pH = 4, ozgina kislotali, shuning uchun tuproq sifatini yaxshilash uchun ohaklash kerak.
Vazifa № 3. Universal indikator yordamida ba'zi eritmalar va sharbatlarning pH qiymatini aniqlang.
22-betdagi topshiriqni o‘qing, topshiriqni algoritm bo‘yicha bajaring, natijalarni jadvalga kiriting.
Sharbat manbai |
Sharbat manbai |
||
Kartoshka |
Silikat elim |
||
Yangi karam |
Stol sirkasi |
||
Tuzlangan karam |
Pishirish soda eritmasi |
||
apelsin |
|||
Yangi lavlagi |
|||
Qaynatilgan lavlagi |
Xulosa chiqaring. Shunday qilib, turli xil tabiiy ob'ektlar turli xil pH qiymatlariga ega: pH 1-7 - kislotali muhit (limon, kızılcık, apelsin, pomidor, lavlagi, kivi, olma, banan, choy, kartoshka, tuzlangan karam, qahva, silikat elim).
pH 7-14 ishqoriy muhit (yangi karam, soda eritmasi).
pH = 7 neytral muhit (xurmo, bodring, sut).
Vazifa № 4. O'simliklarni o'rganish ko'rsatkichlari.
Qaysi o'simlik ob'ektlari ko'rsatkich bo'lishi mumkin?
- rezavorlar: sharbatlar, gul barglari: ekstraktlar, sabzavotlar sharbatlari: ildizlar, barglar.
- turli muhitlarda eritma rangini o'zgartira oladigan moddalar.
23-betdagi topshiriqni o‘qing va rejaga muvofiq bajaring.
Natijalarni jadvalda taqdim eting.
O'simlik materiallari (tabiiy ko'rsatkichlar) |
Tabiiy indikator eritma rangi |
||
Kislotali muhit |
Eritmaning tabiiy rangi (neytral muhit) |
Ishqoriy muhit |
|
Kızılcık (sharbat) |
binafsha |
||
Qulupnay (sharbat) |
apelsin |
shaftoli pushti |
|
Blueberry (sharbat) |
qizil-binafsha |
ko'k-binafsha |
|
Qora smorodina (sharbat) |
qizil-binafsha |
ko'k-binafsha |
|
Xulosa chiqaring. Shunday qilib, atrof-muhitning pH darajasiga qarab, tabiiy ko'rsatkichlar: kızılcık (sharbat), qulupnay (sharbat), ko'k (sharbat), qora smorodina (sharbat) quyidagi ranglarga ega bo'ladi: kislotali muhitda - qizil va to'q sariq, neytralda. muhit - qizil, shaftoli - pushti va binafsha ranglar, ishqoriy muhitda pushtidan ko'k-binafsha ranggacha.
Shunday qilib, tabiiy indikator rangining intensivligini ma'lum bir eritma muhitining reaktsiyasi bilan baholash mumkin.
Ishingiz tugagach, ish joyingizni tartibga soling.
Yigitlar! Bugun juda g'ayrioddiy dars bo'ldi! Sizga yoqdimi?! Ushbu darsda olingan ma'lumotlardan kundalik hayotda foydalanish mumkinmi?
Endi mashq daftaringizda berilgan topshiriqni bajaring.
Nazorat vazifasi. Quyida formulalari berilgan moddalarni eritmalarining pH lariga qarab guruhlarga taqsimlang: HCl, H 2 O, H 2 SO 4, Ca (OH) 2, NaCl, NaOH, KNO 3, H 3 PO 4, KOH.
pH 17 - muhit (kislotali), eritmalarga ega (HCl, H 3 PO 4, H 2 SO 4).
pH 714 muhit (ishqoriy), eritmalarga ega (Ca(OH) 2, KOH, NaOH).
pH = 7 muhit (neytral), eritmalarga ega (NaCl, H 2 O, KNO 3).
Ishni baholash ____________________________
Suvli eritmada qaysi H + yoki OH - ionlari ortiqcha bo'lishiga qarab, eritma muhitining quyidagi turlari (belgilari) ajratiladi:
1) nordon
2) ishqoriy
3) neytral
Da muhitning kislotali tabiati eritmada H + vodorod kationlarining ortiqcha miqdori mavjud va gidroksid ionlarining konsentratsiyasi nolga yaqin.
Da ishqoriy muhit eritmada gidroksid ionlarining OH - ortiqcha miqdori mavjud va H + kationlarining konsentratsiyasi nolga yaqin.
Da neytral muhit eritmada, H + va OH - ionlarining konsentrasiyalari bir-biriga teng va amalda nolga teng (0,0000001 mol/l).
Atrof-muhitning tabiatiga qarab rangi o'zgarib turadigan organik moddalar mavjud. Bu hodisa kimyoda keng qo'llaniladi. Eng keng tarqalgan ko'rsatkichlardan ba'zilari lakmus, fenolftalein va metil apelsin (metil apelsin). Atrof-muhitning tabiatiga qarab ushbu moddalarning rangi quyidagi jadvalda keltirilgan:
indikator rangi |
|||
indikator |
neytral muhitda |
kislotali muhitda |
ishqoriy muhitda |
| lakmus | binafsha | qizil
|
ko'k
|
| fenolftalein | rangsiz | rangsiz | qip-qizil
|
| metil apelsin (metil apelsin) |
apelsin
|
pushti
|
sariq
|
Ko'rib turganingizdek, fenolftaleinning o'ziga xos xususiyati shundaki, bu indikator neytral va kislotali muhitni ajratishga imkon bermaydi - har ikkala muhitda ham u hech qanday rangga ega emas. Bu xususiyat, shubhasiz, kamchilikdir, ammo fenolftalein OH - ionlarining ozgina ko'pligiga nisbatan juda sezgirligi tufayli keng qo'llaniladi.
Shubhasiz, ko'rsatkichlar yordamida siz kislotalar, gidroksidi va distillangan suvni bir-biridan ajrata olasiz. Ammo shuni esda tutish kerakki, kislotali, ishqoriy va neytral muhitlar nafaqat kislotalar, ishqorlar va distillangan suv eritmalarida kuzatilishi mumkin. Tuz eritmalarida gidrolizga bo'lgan munosabatiga qarab eritma muhiti ham har xil bo'lishi mumkin.
Masalan, natriy sulfit eritmasini fenolftalein yordamida natriy sulfat eritmasidan ajratish mumkin. Natriy sulfit - kuchli asos va kuchsiz kislotadan hosil bo'lgan tuz, shuning uchun uning eritmalari ishqoriy reaktsiyaga ega bo'ladi. Fenolftalein eritmasida qip-qizil rangga aylanadi. Natriy sulfat kuchli asos va kuchli kislota bilan hosil bo'ladi, ya'ni. gidrolizga uchramaydi va uning suvli eritmalari neytral reaktsiyaga ega bo'ladi. Natriy sulfat eritmasi bo'lsa, fenolftalein rangsiz bo'lib qoladi.