Galogenlar– VII guruh elementlari – ftor, xlor, brom, yod, astatin (astatin radioaktivligi tufayli kam o‘rganilgan). Galogenlar alohida metall bo'lmaganlardir. Faqat yod kamdan-kam hollarda metallarga o'xshash xususiyatlarni namoyon qiladi.
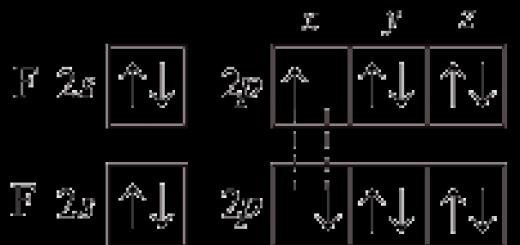
Qo'zg'atmagan holatda, halogen atomlari umumiy elektron konfiguratsiyaga ega: ns2np5. Bu shuni anglatadiki, galogenlar ftordan tashqari 7 ta valent elektronga ega.
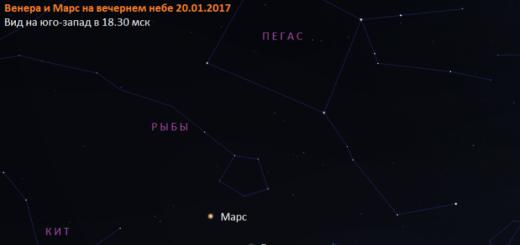
Galogenlarning fizik xususiyatlari: F2 – rangsiz, suyultirilishi qiyin gaz; Cl2 - sariq-yashil, o'tkir bo'g'uvchi hid bilan oson suyultiriladigan gaz; Br2 - qizil-jigarrang suyuqlik; I2 binafsha rangli kristall moddadir.

Vodorod galogenidlarining suvdagi eritmalari kislotalar hosil qiladi. HF – vodorod ftorid (ftorid); HCl - xlorid (tuz); NBr - vodorod bromidi; HI - vodorod yodidi. Kislotalarning kuchi yuqoridan pastgacha kamayadi. Hidroflorik kislota galogenli kislotalar qatorida eng zaif, gidroiyod kislota esa eng kuchli hisoblanadi. Bu Hg ning bog'lanish energiyasi yuqoridan kamayishi bilan izohlanadi. NG molekulasining kuchi xuddi shu yo'nalishda kamayadi, bu yadrolararo masofaning oshishi bilan bog'liq. Suvda ozgina eriydigan tuzlarning eruvchanligi ham kamayadi:
Chapdan o'ngga qarab galogenidlarning eruvchanligi pasayadi. AgF suvda yaxshi eriydi. Erkin holatdagi barcha galogenlar oksidlovchi moddalardir. Ularning oksidlovchi moddalar sifatida kuchi ftordan yodgacha kamayadi. Kristalli, suyuq va gazsimon holatda barcha galogenlar alohida molekulalar shaklida mavjud. Atom radiuslari bir xil yo'nalishda ortadi, bu erish va qaynash nuqtalarining oshishiga olib keladi. Ftor atomlarga yodga qaraganda yaxshiroq ajraladi. Elektrod potentsiallari galogen kichik guruhini pastga siljitishda kamayadi. Ftor eng yuqori elektrod potentsialiga ega. Ftor eng kuchli oksidlovchi moddadir. Har qanday yuqori bo'sh halogen eritmada manfiy bir zaryadlangan ion holatida bo'lgan pastki qismini siqib chiqaradi.
20. Xlor. Vodorod xlorid va xlorid kislotasi
Xlor (Cl) - 3-davrda, davriy tizimning asosiy kichik guruhining VII guruhida, seriya raqami 17, atom massasi 35.453; halogenlarni nazarda tutadi.
Jismoniy xususiyatlar: o'tkir hidli sariq-yashil gaz. Zichlik 3,214 g/l; erish nuqtasi -101 ° C; qaynash nuqtasi -33,97 °C, oddiy haroratda 0,6 MPa bosim ostida osongina suyultiriladi. Suvda erigan sarg'ish xlorli suv hosil qiladi. Organik erituvchilarda, ayniqsa geksanda (C6H14) va uglerod tetrakloridida yaxshi eriydi.
Xlorning kimyoviy xossalari: elektron konfiguratsiya: 1s22s22p63s22p5. Tashqi sathda 7 ta elektron mavjud. Darajani to'ldirish uchun sizga -1 oksidlanish holatini ko'rsatadigan xlor qabul qiladigan 1 ta elektron kerak bo'ladi. Xlorning + 7 gacha bo'lgan ijobiy oksidlanish darajalari ham mavjud. Quyidagi xlor oksidlari ma'lum: Cl2O, ClO2, Cl2O6 va Cl2O7. Ularning barchasi beqaror. Xlor kuchli oksidlovchi moddadir. To'g'ridan-to'g'ri metallar va metall bo'lmaganlar bilan reaksiyaga kirishadi:
Vodorod bilan reaksiyaga kirishadi. Oddiy sharoitlarda reaktsiya sekin, kuchli isitish yoki yorug'lik bilan - zanjir mexanizmiga ko'ra portlash bilan davom etadi:
![]()
Xlor gidroksidi eritmalar bilan o'zaro ta'sir qiladi, tuzlar - gipoxloritlar va xloridlar hosil qiladi:
Xlor gidroksidi eritmasiga o'tkazilganda, xlorid va gipoxlorit eritmalari aralashmasi hosil bo'ladi:
Xlor qaytaruvchi vositadir: Cl2 + 3F2 = 2ClF3.
Suv bilan o'zaro ta'siri:
Xlor uglerod, azot va kislorod bilan bevosita reaksiyaga kirishmaydi.
Kvitansiya: 2NaCl + F2 = 2NaF + Cl2.
Elektroliz: 2NaCl + 2H2O = Cl2 + H2 + 2NaOH.
Tabiatda topish: quyidagi minerallar tarkibida mavjud: galit (tosh tuzi), silvit, bishofit; dengiz suvida natriy, kaliy, magniy va boshqa elementlarning xloridlari mavjud.
Vodorod xlorid HCl. Jismoniy xususiyatlar: rangsiz gaz, havodan og'irroq, hosil bo'lish uchun suvda yaxshi eriydi xlorid kislotasi.
Kvitansiya: laboratoriyada:
Sanoatda: vodorod xlor oqimida yondiriladi. Keyinchalik, vodorod xlorid xlorid kislota hosil qilish uchun suvda eritiladi (yuqoriga qarang).
Kimyoviy xossalari: xlorid kislota kuchli, bir asosli, vodorodgacha kuchlanish qatoridagi metallar bilan o'zaro ta'sir qiladi: Zn + 2HCl = ZnCl2 + H2.
Qaytaruvchi vosita sifatida ko'plab metallarning oksidlari va gidroksidlari bilan reaksiyaga kirishadi.
TA'RIF
Galogenlar– VII A guruh elementlari – ftor (F), xlor (Cl), brom (Br) va yod (I).
Galogenlarning tashqi energiya darajasining elektron konfiguratsiyasi ns 2 np 5. Galogenlar energiya darajasini to'ldirishdan oldin faqat bitta elektronga ega bo'lmaganligi sababli, ORRda ular ko'pincha oksidlovchi moddalarning xususiyatlarini namoyish etadilar. Galogenlarning oksidlanish darajasi: “-1” dan “+7” gacha. Galogen guruhining yagona elementi ftor faqat bitta oksidlanish holatini "-1" ko'rsatadi va eng elektronegativ element hisoblanadi. Galogen molekulalari ikki atomli: F 2, Cl 2, Br 2, I 2.
Galogenlarning kimyoviy xossalari
Kimyoviy element atomi yadrosining zaryadining ortishi bilan, ya'ni. ftordan yodga o'tganda galogenlarning oksidlanish qobiliyati pasayadi, bu quyi halogenlarni gidrogal kislotalar va ularning tuzlaridan yuqoriroqlari bilan siqib chiqarish qobiliyati bilan tasdiqlanadi:
Br 2 + 2HI = I 2 + 2HBr;
Cl 2 + 2KBr = Br 2 + 2KCl.
Ftor eng katta kimyoviy faollikka ega. Ko'pchilik kimyoviy elementlar xona haroratida ham ftor bilan o'zaro ta'sir qiladi, chiqaradi katta miqdorda issiqlik. Hatto suv ftorda yonadi:
2H 2 O + 2F 2 = 4HF + O 2.
Erkin xlor ftorga qaraganda kamroq reaktivdir. Kislorod, azot va asil gazlar bilan bevosita reaksiyaga kirishmaydi. Ftor kabi boshqa barcha moddalar bilan o'zaro ta'sir qiladi:
2Fe + Cl 2 = 2FeCl 3;
2P + 5Cl 2 = 2PCl 5.
Xlor sovuqda suv bilan o'zaro ta'sir qilganda, teskari reaktsiya paydo bo'ladi:
Cl 2 + H 2 O↔HCl +HClO.
Reaksiya mahsulotlari aralashmasi xlorli suv deb ataladi.
Sovuqda xlor ishqorlar bilan o'zaro ta'sirlashganda xloridlar va gipoxloritlar aralashmalari hosil bo'ladi:
Cl 2 + Ca(OH) 2 = Ca(Cl)OCl + H 2 O.
Xlorni issiq gidroksidi eritmasida eritganda quyidagi reaksiya sodir bo'ladi:
3Cl 2 + 6KOH = 5KCl + KClO 3 + 3H 2 O.
Brom, xlor kabi, suvda eriydi va u bilan qisman reaksiyaga kirishib, "bromli suv" deb ataladigan suvni hosil qiladi, yod esa suvda deyarli erimaydi.
Yod kimyoviy faolligi bilan boshqa galogenlardan sezilarli farq qiladi. Koʻpchilik nometallar bilan reaksiyaga kirishmaydi, faqat qizdirilganda metallar bilan sekin reaksiyaga kirishadi. Yodning vodorod bilan o'zaro ta'siri faqat kuchli isitish bilan sodir bo'ladi, bu reaktsiya endotermik va yuqori darajada qaytariladi:
H 2 + I 2 = 2HI - 53 kJ.
Galogenlarning fizik xossalari
No. ftor o'tkir hidli och sariq gazdir. Zaharli. Xlor och yashil gaz, xuddi ftor kabi, o'tkir hidga ega. Yuqori zaharli. Yuqori bosim va xona haroratida u osongina suyuq holatga aylanadi. Brom - xarakterli yoqimsiz o'tkir hidli qizil-jigarrang og'ir suyuqlik. Suyuq brom, shuningdek, uning bug'lari juda zaharli hisoblanadi. Brom suvda yomon, qutbsiz erituvchilarda yaxshi eriydi. Yod to'q kulrang qattiq modda bo'lib, metall yaltiraydi. Yod bug'i bor siyohrang. Yod osongina sublimatsiya qiladi, ya'ni. ichiga kiradi gazsimon holat qattiq holatdan, suyuq holatni chetlab o'tishda.
Galogenlarni ishlab chiqarish
Galogenlarni eritmalar yoki galogenid eritmalarini elektroliz qilish orqali olish mumkin:
MgCl 2 = Mg + Cl 2 (eritma).
Ko'pincha halogenlar gidrogal kislotalarning oksidlanish reaktsiyasi natijasida olinadi:
MnO 2 + 4HCl = MnCl 2 + Cl 2 + 2H 2 O;
K 2 Cr 2 O 7 + 14HCl \u003d 3Cl 2 + 2KCl + 2CrCl 3 + 7H 2 O;
2KMnO 4 +16HCl = 2MnCl 2 +5Cl 2 +8H 2 O +2KCl.
Galogenlarni qo'llash
Galogenlar turli xil mahsulotlarni ishlab chiqarish uchun xom ashyo sifatida ishlatiladi. Shunday qilib, ftor va xlor turli xil polimer materiallarni sintez qilish uchun ishlatiladi, shuningdek, xlorid kislota ishlab chiqarishda xom ashyo hisoblanadi; Brom va yod topilgan keng qo'llanilishi tibbiyotda brom lak-bo'yoq sanoatida ham qo'llaniladi.
Muammoni hal qilishga misollar
MISOL 1
| Mashq qilish | Og'irligi 508 g bo'lgan yod hosil bo'lsa, kaliy yodid bilan reaksiyaga kirishgan xlor hajmini (no) hisoblang. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Yechim | Xlor va kaliy yodid o'rtasidagi reaksiya tenglamasini yozamiz: Cl 2 + 2KI = I 2 + 2KCl D.I. tomonidan kimyoviy elementlar jadvali yordamida hisoblangan yodning molyar massasi. Mendeleyev, teng - 254 g/mol. Hosil bo'lgan yod miqdorini topamiz: v(I 2) = m(I 2)/M(I 2) At, 1940 yilda ochilgan
Barcha galogenlarning tashqi elektron qatlamida elektron orbitallarning taqsimlanishi bir xil turdagi
Ularning atomlar va molekulalarning tuzilishida umumiy jihatlari juda ko'p. Ular qurilishni yakunlamoqda R-tashqi qatlamning qobiqlari, shuning uchun ularning barchasi p-elementlar soniga tegishli. Galogen atomlarining tashqi elektron qatlamida bitta elektron yetishmaydi, shuning uchun bu elementlarning elektron manfiyligi aniq bo'ladi va oksidlanish-qaytarilish reaktsiyalarida ular asosan oksidlovchi moddalar sifatida harakat qiladilar. ■ 1. Atom yadrosi zaryadining oshishiga qarab atom radiusi qanday o'zgaradi?
Galogenlarning fizik xossalariGalogenlarning barcha fizik va kimyoviy xossalari element atomlarining tuzilishiga bog'liq. Turli galogenlarning bu xossalari asosan o'xshashdir, lekin ayni paytda har bir halogen bir qator xususiyatlarga ega. ■ 7. Yadro zaryadlarining ortishi bilan galogenlarning rang intensivligi qanday o'zgaradi?
10. “Galogenlarning fizik xossalari” jadvalini quyidagi model bo‘yicha tuzing va to‘ldiring:
Galogenlarning fiziologik ta'siriUlarning barchasi fiziologik ta'sirida zaharli. Ftor ayniqsa zaharli hisoblanadi: oz miqdorda nafas olganda o'pka shishi, ko'p miqdorda o'pka to'qimalarining vayron bo'lishiga va o'limga olib keladi. Yod Barcha halogenlar orasida eng kam zaharli. Yod bug'ini qizdirilganda nafas olish zaharlanishni keltirib chiqarishi mumkin, ammo bug'li yod bilan ishlash kamdan-kam hollarda, masalan, uni sublimatsiya bilan tozalashda. Kristalli yodni qo'l bilan olmaslik kerak, go'yo u teriga tegsa, xarakterli sariq dog'lar paydo bo'lishiga olib keladi. Galogenlar bilan barcha ishlar tutun qopqog'ida amalga oshirilishi kerak. Galogenlar bilan ishlashda xavfsizlik choralarini va zaharlanishda birinchi yordamni daftaringizga yozing. Galogenlarning kimyoviy xossalari
Yuqorida ta'kidlab o'tilganidek, kimyoviy xossalarining tabiatiga ko'ra, barcha galogenlar sezilarli elektromanfiylikka ega bo'lgan tipik nometalldir. Eng katta metall bo'lmagan faollikka ega bo'lgan eng elektronegativ element ftor, eng kam faoli yoddir. Guruch. 21. Xlorda vodorodning yonishi. 1- xlor 2- Galogenlarning oddiy moddalar bilan o'zaro ta'siri. Turli reaktsiyalar misollari yordamida ftordan xlorgacha bo'lgan kimyoviy faollikning pasayishini kuzatishingiz mumkin. Turli galogenlarning vodorod bilan o'zaro ta'siri ayniqsa qiziq. Ularning reaksiya sharoitlari boshqacha. Ftorid galogen vodorodlar orasida eng mustahkam birikma hisoblanadi. Vodorod bilan brom vodorod bromid hosil qiladi.
Galogenlar, odatda, juda faol bo'lgan metallar bilan o'zaro ta'sirlashganda oksidlovchi xususiyatlarni ham ko'rsatadi. Guruch. 22. Masalan. Su + Sl2 = SuSl2 Bu erda xlor bilan reaksiyaga kirishib, u +3 - Fe +3 va +2 - Cu +2 ga teng oksidlanish darajasini ko'rsatadi. Yuqoridagi barcha holatlarda xlor o'zini tutadi. Elementlar kimyosi VIIA kichik guruhining nometallari VIIA kichik guruhining elementlari yuqori bo'lgan odatiy bo'lmagan metalldir elektronegativlik, ular guruh nomiga ega - "galogenlar". Ma'ruzada yoritiladigan asosiy masalalar VIIA kichik guruhidagi metall bo'lmaganlarning umumiy xususiyatlari. Elektron tuzilma, atomlarning eng muhim xususiyatlari. Eng xarakterli ste- oksidlanish jazolari. Galogenlar kimyosining xususiyatlari. Oddiy moddalar. Tabiiy birikmalar. Galogen birikmalar Gidrogal kislotalar va ularning tuzlari. Tuz va gidroflorik kislota uyalar, kvitansiya va ariza. Halid komplekslari. Ikkilik kislorodli birikmalar halogenlar. Beqarorlik taxminan. Oddiy moddalarning oksidlanish-qaytarilish xossalari va ko- birliklar. Nomutanosiblik reaksiyalari. Latimer diagrammalar.
VIIA kichik guruhi elementlari kimyosi umumiy xususiyatlar
VIIA-guruhni p-elementlar hosil qiladi: ftor F, xlor Cl, brom Br, yod I va astatin At. Valentlik elektronlarining umumiy formulasi ns 2 np 5. VIIA guruhining barcha elementlari odatiy metall bo'lmaganlardir.
barqaror sakkiz elektronli qobiq hosil qilish qutilar, shuning uchun ular bor tomon kuchli moyillik mavjud elektron qo'shilishi. Barcha elementlar osonlikcha oddiy bir zaryadni hosil qiladi ny anionlari G –. Oddiy anionlar shaklida VIIA guruh elementlari tabiiy suvda va tabiiy tuzlarning kristallarida, masalan, galit NaCl, silvit KCl, ftoritda uchraydi. CaF2. Elementlarning umumiy guruhi nomi VIIA- "galogenlar" guruhi, ya'ni "tuzlarni tug'diruvchi" ularning metallar bilan birikmalarining aksariyati tashkil etadi tipik tuzlar(CaF2, NaCl, MgBr2, KI), ko- to'g'ridan-to'g'ri o'zaro ta'sir orqali olinishi mumkin metallning halogen bilan o'zaro ta'siri. Erkin halogenlar tabiiy tuzlardan olinadi, shuning uchun "galogenlar" nomi "tuzlardan tug'ilgan" deb ham tarjima qilinadi.
Minimal oksidlanish darajasi (-1) eng barqaror hisoblanadi barcha halogenlar uchun. VIIA guruh elementlari atomlarining ba'zi xarakteristikalari keltirilgan VIIA guruh elementlari atomlarining eng muhim xarakteristikalari
Galogenlar yuqori elektron yaqinligiga ega (maksimal Cl) va juda yuqori ionlanish energiyasi (F da maksimal) va maksimal har bir davrda mumkin bo'lgan elektronegativlik. Ftor eng ko'p barcha kimyoviy elementlarning elektronegativi. Galogen atomlarida bitta juftlashtirilmagan elektronning mavjudligi aniqlanadi oddiy moddalardagi atomlarning diatomik molekulalarga birlashishini ifodalaydi G2. Oddiy moddalar uchun galogenlar eng xarakterli oksidlovchi moddalardir xususiyatlar, F2 da eng kuchli va I2 ga o'tishda zaiflashadi. Galogenlar barcha metall bo'lmagan elementlarning eng katta reaktivligi bilan tavsiflanadi. Ftor, hatto galogenlar orasida ham ajralib turadi juda yuqori faollikka ega. Ikkinchi davr elementi ftor ikkinchisidan kuchli farq qiladi kichik guruhning boshqa elementlari. Bu barcha metall bo'lmaganlar uchun umumiy namunadir.
Ftor, eng elektronegativ element sifatida, jinsiy aloqani ko'rsatmaydi doimiy oksidlanish darajasi. Har qanday aloqada, shu jumladan ki- kislorod, ftor oksidlanish holatida (-1). Boshqa barcha halogenlar ijobiy oksidlanish darajasini ko'rsatadi leniya maksimal +7 gacha. Galogenlarning eng xarakterli oksidlanish darajalari: F: -1, 0; Cl, Br, I: -1, 0, +1, +3, +5, +7. Cl oksidlanish darajasida bo'lgan ma'lum oksidlarga ega: +4 va +6. Ijobiy holatda eng muhim halogen birikmalar, Oksidlanishning jazosi kislorodli kislotalar va ularning tuzlaridir. Musbat oksidlanish darajasidagi barcha halogen birikmalar kuchli oksidlovchi moddalardir. dahshatli oksidlanish darajasi. Nomutanosiblik ishqoriy muhit tomonidan ta'minlanadi. Oddiy moddalar va kislorod birikmalarini amaliy qo'llash Galogenlarning kamayishi asosan ularning oksidlovchi ta'siriga bog'liq. Eng keng amaliy foydalanish oddiy moddalarni toping Cl2 va F2. Eng katta miqdor xlor va ftor sanoatda iste'mol qilinadi organik sintez: plastmassalar, sovutgichlar, erituvchilar ishlab chiqarishda, pestitsidlar, dorilar. Metalllarni olish va ularni tozalash uchun katta miqdorda xlor va yod ishlatiladi. Xlor ham ishlatiladi tsellyulozani oqartirish uchun, dezinfeksiya qilish uchun ichimlik suvi va ishlab chiqarishda oqartiruvchi suv va xlorid kislotasi. Oksokislotalarning tuzlari portlovchi moddalar ishlab chiqarishda ishlatiladi.
Kislotalar - xlorid va erigan kislotalar amaliyotda keng qo'llaniladi. Ftor va xlor yigirmata eng keng tarqalgan elementlardan biridir u erda tabiatda brom va yod sezilarli darajada kamroq. Barcha galogenlar tabiatda oksidlanish holatida uchraydi(-1). Faqat yod KIO3 tuzi shaklida bo'ladi, Chili selitrasida (KNO3) nopoklik sifatida kiritilgan. Astatin - sun'iy ravishda ishlab chiqarilgan radioaktiv element (u tabiatda mavjud emas). Otning beqarorligi yunon tilidan kelgan nomda aks etadi. "astatos" - "beqaror". Astatin saraton o'smalarining radiatsiya terapiyasi uchun qulay emitent hisoblanadi. Oddiy moddalar Galogenlarning oddiy moddalarini ikki atomli molekulalar G2 hosil qiladi. Oddiy moddalarda, elektronlar sonining ko'payishi bilan F2 dan I2 ga o'tish paytida taxt qatlamlari va atomlarning qutblanishining ortishi, o'sish bor molekulalararo o'zaro ta'sir agregatlarning o'zgarishiga olib keladi. standart sharoitlarda turish. Ftor (normal sharoitda) sariq gaz bo'lib, -181o C da aylanadi suyuqlik holati. Xlor sariq-yashil gaz bo'lib, -34o C da suyuqlikka aylanadi. Cl nomi u bilan bog'liq bo'lib, u yunoncha "xloros" - "sariq-" dan keladi. yashil". F2 ga nisbatan Cl2 ning qaynash nuqtasining keskin oshishi, molekulalararo o'zaro ta'sir kuchayganligini ko'rsatadi. Brom toʻq qizil, juda uchuvchan suyuqlik boʻlib, 58,8o S da qaynaydi. elementning nomi gazning o'tkir yoqimsiz hidi bilan bog'liq va undan olingan "bromos" - "xushbo'y". Yod - quyuq binafsha rangli kristallar, zaif "metall" qizdirilganda osongina sublimatsiyalanadigan, binafsha rangli bug'larni hosil qiluvchi bo'laklar;
Yodning qaynash nuqtasi 183 ° S. Uning nomi yod bug'ining rangidan kelib chiqadi - "yodos" - "binafsha". Barcha oddiy moddalar o'tkir hidga ega va zaharli hisoblanadi. Ularning bug'larini inhalatsiyalash shilliq pardalar va nafas olish organlarining tirnash xususiyati keltirib chiqaradi va yuqori konsentratsiyalarda - bo'g'ilish. Birinchi jahon urushi paytida xlor zaharli vosita sifatida ishlatilgan. Ftor gazi va suyuq brom terining kuyishiga olib keladi. Ha bilan ishlash logens, ehtiyot choralarini ko'rish kerak. Galogenlarning oddiy moddalari qutbsiz molekulalar tomonidan hosil qilinganligi sababli soviydi, ular qutbsiz organik erituvchilarda yaxshi eriydi: spirt, benzol, uglerod tetraklorid va boshqalar.. Xlor, brom va yod suvda kam eriydi, ularning suvdagi eritmalari xlor, brom va yodli suvlar deb ataladi; Br2 boshqalarga qaraganda yaxshiroq eriydi, to'yingandagi brom konsentratsiyasi. Eritma 0,2 mol/l ga, xlor esa 0,1 mol/l ga etadi. Ftorid suvni parchalaydi: 2F2 + 2H2 O = O2 + 4HF Galogenlar yuqori oksidlanish faolligi va o'tish xususiyatini namoyon qiladi galoid anionlariga aylanadi. G2 + 2e– 2G– Ftor ayniqsa yuqori oksidlovchi faollikka ega. Ftor asil metallarni oksidlaydi (Au, Pt). Pt + 3F2 = PtF6 U hatto ba'zi inert gazlar (kripton, ksenon va radon), masalan, Xe + 2F2 = XeF4 F2 atmosferasida juda ko'p barqaror ulanishlar, Masalan, suv, kvarts (SiO2). SiO2 + 2F2 = SiF4 + O2
Ftor bilan reaktsiyalarda, hatto azot va oltingugurt kabi kuchli oksidlovchi moddalar ham nik kislota, qaytaruvchi sifatida harakat qiladi, ftor esa kirishni oksidlaydi tarkibida O(–2) mavjud. 2HNO3 + 4F2 = 2NF3 + 2HF + 3O2 H2 SO4 + 4F2 = SF6 + 2HF + 2O2 F2 ning yuqori reaktivligi konfiguratsiyani tanlashda qiyinchiliklar tug'diradi. u bilan ishlash uchun konstruktiv materiallar. Odatda bu maqsadlar uchun biz foydalanamiz Nikel va mis mavjud bo'lib, ular oksidlanganda ularning yuzasida ftoridlarning zich himoya plyonkalarini hosil qiladi. F nomi uning tajovuzkor harakati bilan bog'liq. Men ovqatlanaman, u yunon tilidan keladi. "Ftorlar" - "buzg'unchi". F2, Cl2, Br2, I2 qatorlarida oksidlanish qobiliyati kuchayishi tufayli zaiflashadi. atomlar hajmini oshirish va elektronegativlikni kamaytirish. IN suvli eritmalar Ver-ning oksidlovchi va qaytaruvchi xususiyatlari Moddalar odatda elektrod potentsiallari yordamida tavsiflanadi. Jadvalda qisqartirish yarim reaktsiyalari uchun standart elektrod potentsiallari (Eo, V) ko'rsatilgan galogenlarning hosil bo'lishi. Taqqoslash uchun, ki- uchun Eo qiymati uglerod eng keng tarqalgan oksidlovchi moddadir. Oddiy halogen moddalar uchun standart elektrod potensiallari
Oksidlanish faolligining pasayishi Jadvaldan ko'rinib turibdiki, F2 - ancha kuchli oksidlovchi, O2 dan ko'ra, shuning uchun F2 suvli eritmalarda mavjud emas , suvni oksidlaydi, F-gacha tiklanish. Eo qiymatiga ko'ra, Cl2 ning oksidlanish qobiliyati
O2 dan ham yuqori. Haqiqatan ham, xlorli suvni uzoq muddatli saqlash vaqtida u kislorodning chiqishi va HCl hosil bo'lishi bilan parchalanadi. Ammo reaktsiya sekin (Cl2 molekulasi F2 molekulasiga qaraganda sezilarli darajada kuchliroq va xlor bilan reaksiyalar uchun aktivlanish energiyasi yuqori), dispro- qismlarga ajratish: Cl2 + H2 O HCl + HOCl Suvda u oxirigacha etib bormaydi (K = 3,9 . 10-4), shuning uchun Cl2 suvli eritmalarda mavjud. Br2 va I2 suvda yanada katta barqarorlik bilan tavsiflanadi. Nomutanosiblik juda xarakterli oksidlanish- halogenlar uchun qaytarilish reaktsiyasi. Kuchaytirishning nomutanosibligi ishqoriy muhitda quyiladi. Ishqorda Cl2 ning nomutanosibligi anionlarning hosil bo'lishiga olib keladi Cl- va ClO-. Disproporsiya konstantasi 7,5 ga teng. 1015. Cl2 + 2NaOH = NaCl + NaClO + H2O Yod ishqorda nomutanosib bo'lsa, I- va IO3- hosil bo'ladi. Ana- Mantiqan, Br2 yodni nomutanosiblashtiradi. Mahsulot o'zgarishi nomutanosibdir millat Br va I dagi GO– va GO2– anionlari beqaror ekanligi bilan bog‘liq. Xlorning nomutanosiblik reaktsiyasi sanoatda qo'llaniladi kuchli va tez ta'sir qiluvchi gipoxlorit oksidlovchini olish qobiliyati, oqartiruvchi ohak, bertolet tuzi. 3Cl2 + 6 KOH = 5KCl + KClO3 + 3H2 O
Galogenlarning metallar bilan o'zaro ta'siri Galogenlar ko'plab metallar bilan kuchli reaksiyaga kirishadi, masalan: Mg + Cl2 = MgCl2 Ti + 2I2 TiI4 Na + galogenidlar, ularda metall past oksidlanish darajasiga ega (+1, +2), - Bular tuzga o'xshash birikmalar bo'lib, ular asosan ionli aloqalarga ega. Qanday lo, ionli galogenidlar erish nuqtasi yuqori bo'lgan qattiq moddalardir Metall halidlari, ular tarkibida metall mavjud yuqori daraja oksidlanish ionlar asosan kovalent bog'lanishga ega bo'lgan birikmalardir. Ularning ko'pchiligi normal sharoitda gazlar, suyuqliklar yoki eriydiganlardir qattiq moddalar. Masalan, WF6 gaz, MoF6 suyuqlik, TiCl4 suyuqlikdir. Galogenlarning metall bo'lmaganlar bilan o'zaro ta'siri Galogenlar ko'plab metall bo'lmaganlar bilan bevosita o'zaro ta'sir qiladi: vodorod, fosfor, oltingugurt va boshqalar. Masalan: H2 + Cl2 = 2HCl 2P + 3Br2 = 2PBr3 S + 3F2 = SF6 Metall bo'lmagan galogenidlardagi bog'lanish asosan kovalentdir. Odatda bu birikmalar past erish va qaynash nuqtalariga ega. Ftordan yodga o'tganda galogenidlarning kovalent tabiati kuchayadi. Odatda nometallarning kovalent galogenidlari kislotali birikmalar; suv bilan o'zaro ta'sirlashganda ular gidrolizlanib, kislotalar hosil qiladi. Masalan: PBr3 + 3H2 O = 3HBr + H3 PO3 PI3 + 3H2 O = 3HI + H3 PO3 PCl5 + 4H2 O = 5HCl + H3 PO4
Dastlabki ikkita reaksiya brom va vodorod yodidi ishlab chiqarish uchun ishlatiladi. noik kislota. Intergalidlar. Galogenlar bir-biri bilan birikib, interg olib boradi. Bu birikmalarda engilroq va ko'proq elektromanfiy galogen (-1) oksidlanish darajasida, og'irroq esa musbat holatda bo'ladi. oksidlanish jazolari. Galogenlarning qizdirilganda to'g'ridan-to'g'ri o'zaro ta'siri tufayli quyidagilar olinadi: ClF, BrF, BrCl, ICl. Bundan tashqari, murakkabroq intergalidlar mavjud: ClF3, BrF3, BrF5, IF5, IF7, ICl3. Oddiy sharoitlarda barcha intergalidlar suyuq moddalardir past haroratlar qaynash. Intergalidlar yuqori oksidlanish faolligiga ega faoliyat. Masalan, SiO2, Al2 O3, MgO va boshqalar kabi kimyoviy barqaror moddalar ClF3 bug'larida yonadi. 2Al2 O3 + 4ClF3 = 4 AlF3 + 3O2 + 2Cl2 Ftorid ClF 3 tez ta'sir qiluvchi agressiv ftorli reagentdir hovli F2. U ishlatiladi organik sintezlar va ftor bilan ishlash uchun nikel uskunalari yuzasida himoya plyonkalar olish. Suvda intergalidlar gidrolizlanib, kislotalar hosil qiladi. Masalan, ClF5 + 3H2 O = HClO3 + 5HF Tabiatdagi halogenlar. Oddiy moddalarni olish Sanoatda galogenlar ularning tabiiy birikmalaridan olinadi. Hammasi erkin galogenlarni olish jarayonlari galogenning oksidlanishiga asoslangan Nid ionlari. 2G – G2 + 2e– Galogenlarning katta miqdori mavjud tabiiy suvlar anionlar shaklida: Cl–, F–, Br–, I–. IN dengiz suvi 2,5% gacha NaCl ni o'z ichiga olishi mumkin. Brom va yod suvdan olinadi neft quduqlari va dengiz suvi.
Atomlarning tuzilishi va xossalari. VII guruhning asosiy kichik guruhining elementlari Davriy jadval D.I.Mendeleyev, umumiy nom ostida birlashgan galogenlar - ftor F, xlor Cl, brom Br, yod I, astatin At (tabiatda kamdan-kam uchraydi) - tipik metall bo'lmaganlar. Bu tushunarli, chunki ularning atomlari tashqi tomondan mavjud energiya darajasi etti elektron va ularni bajarish uchun faqat bitta elektron kerak. Galogen atomlari metallar bilan o'zaro ta'sirlashganda, metall atomlaridan elektronni qabul qiladi. Bunday holda, paydo bo'ladi ionli bog'lanish va tuzlar hosil bo'ladi. Bu qaerdan keladi umumiy ism kichik guruhlar "galogenlar", ya'ni "tuzlarni tug'ish". Galogenlar juda kuchli oksidlovchi moddalardir. Ftorid kimyoviy reaksiyalar faqat oksidlovchi xossalarini namoyon qiladi va birikmalarda faqat -1 oksidlanish darajasi bilan tavsiflanadi. Qolgan galogenlar ko'proq elektron manfiy elementlar - ftor, kislorod, azot bilan o'zaro ta'sirlashganda qaytaruvchi xususiyatni ham namoyon qiladi. Ularning oksidlanish darajasi +1, +3, +5, +7 qiymatlarini olishi mumkin. Galogenlarning qaytaruvchi xossalari xlordan yodgacha oshadi, bu ularning atomlari radiuslarining oshishi bilan bog'liq: xlor atomlari yoddan taxminan bir yarim baravar kichikdir. Galogenlar oddiy moddalardir. Barcha galogenlar kovalent qutbsiz bo'lgan ikki atomli molekulalar shaklida erkin holatda mavjud. kimyoviy bog'lanish atomlar orasida. Qattiq holatda F 2, Cl 2, Br 2, I 2 molekulyarga ega kristall panjaralar, bu ular tomonidan tasdiqlangan jismoniy xususiyatlar(7-jadval). 7-jadval
Ko'rinib turibdiki, ortib borishi bilan molekulyar og'irlik galogenlar, ularning erish va qaynash temperaturalari ortadi (88-rasm), zichligi ortadi: ftor va xlor gazlar, brom suyuqlik, yod qattiq moddadir.
Guruch. 88. Buning sababi shundaki, galogen atomlari va molekulalarining o'lchamlari ortishi bilan (89-rasm), ular orasidagi molekulalararo o'zaro ta'sir kuchlari ham ortadi.
Guruch. 89. F 2 dan I 2 gacha galogenlarning rang intensivligi ortadi. Yod kristallari metall yorqinlikka ega. Galogenlarning kimyoviy faolligi, xuddi metall bo'lmaganlar kabi, ftordan yodgacha zaiflashadi. Har bir halogen o'z davridagi eng kuchli oksidlovchi moddadir. Galogenlarning oksidlovchi xossalari metallar bilan o'zaro ta'sirlashganda aniq namoyon bo'ladi. Bunday holda, siz allaqachon bilganingizdek, tuzlar hosil bo'ladi. Shunday qilib, ftor ko'pchilik metallar bilan normal sharoitda allaqachon reaksiyaga kirishadi va qizdirilganda kimyoviy passivligi bilan mashhur bo'lgan oltin, kumush va platina bilan ham reaksiyaga kirishadi. Alyuminiy va rux ftorli atmosferada yonadi:
Qolgan galogenlar asosan qizdirilganda metallar bilan reaksiyaga kirishadi. Shunday qilib, xlor bilan to'ldirilgan kolbada maydalangan surma kristallari alangalanadi va chiroyli tarzda yonadi (90-rasm), ikkita surma xlorid (III) va (V) aralashmasini hosil qiladi:
Guruch. 90. Isitilgan temir kukuni xlor bilan reaksiyaga kirishganda ham yonadi. Tajriba surma bilan ham o'tkazilishi mumkin, lekin faqat temir qoziqlari avval temir qoshiqda qizdirilishi kerak, so'ngra kichik qismlarga xlorli kolbaga quyiladi. Xlor kuchli oksidlovchi bo'lganligi sababli, reaksiya natijasida temir (III) xlorid hosil bo'ladi (91-rasm):
Guruch. 91. Qizil-issiq mis sim brom bug'ida yonadi:
Yod metallarni sekinroq oksidlaydi, ammo katalizator bo'lgan suv ishtirokida yodning alyuminiy kukuni bilan reaktsiyasi juda shiddatli davom etadi:
Reaktsiya binafsha yod bug'ining chiqishi bilan birga keladi (nima uchun?). Oksidlanish xossalarining kamayishi va galogenlarning ftordan yodgacha qaytarilish xossalarining oshishiga ularning tuz eritmalaridan bir-birini siqib chiqarish qobiliyati bilan ham baho berish mumkin.
Guruch. 92. Erkin brom yodni tuzlardan siqib chiqaradi:
Bu reaktsiya ftor uchun xos emas, chunki u eritmada bo'ladi va ftor suv bilan o'zaro ta'sir qiladi va undan kislorodni siqib chiqaradi:
Bu erda kislorod kamaytiruvchi vositaning g'ayrioddiy rolini o'ynaydi. Bu, ehtimol, yonish reaktsiyasida kislorod boshlang'ich moddalardan biri emas, balki uning mahsuloti bo'lgan yagona holat. Ftordan yodgacha bo'lgan galogenlarning oksidlanish xususiyatlarining zaiflashishi ular vodorod bilan o'zaro ta'sirlashganda aniq namoyon bo'ladi. Ushbu reaksiya tenglamasini umumiy shaklda yozish mumkin: N 2 + G 2 = 2NG (G - shartli kimyoviy belgi halogenlar). Agar ftor har qanday sharoitda vodorod bilan portlash bilan reaksiyaga kirsa, xlor va vodorod aralashmasi faqat alangalanganda yoki to'g'ridan-to'g'ri nurlanganda portlash bilan reaksiyaga kirishadi. quyosh nuri, brom qizdirilganda va portlashsiz vodorod bilan reaksiyaga kirishadi. Bu reaksiyalar ekzotermikdir. Kristalli yod birikmasining vodorod bilan reaksiyasi zaif endotermikdir; u qizdirilganda ham sekin kechadi. Bu reaksiyalar natijasida vodorod ftorid HF, vodorod xlorid HCl, vodorod bromid HBr va vodorod yodid HI hosil bo'ladi. Galogenlarning kashfiyoti. Erkin holatda ftor birinchi marta 1886 yilda frantsuz kimyogari A. Moissan tomonidan olingan bo'lib, u buning uchun mukofotlangan. Nobel mukofoti. Element o'z nomini yunoncha florolardan oldi - "yo'q qilish". Xlor shved kimyogari K. Scheele tomonidan 1774 yilda kashf etilgan. Element rangi uchun shunday nomlangan. oddiy modda(yunoncha chloros - sariq-yashil). Brom 1826 yilda fransuz kimyogari A. Balard tomonidan kashf etilgan. Element oddiy moddaning hidi uchun shunday nomlangan (yunoncha bromos - fetid). Yod 1811 yilda frantsuz olimi B.Kurtua tomonidan olingan va o'z nomini oddiy moddaning bug'larining rangi uchun oldi (yunoncha iyodlardan - binafsha). Yangi so'zlar va tushunchalar
Mustaqil ish uchun topshiriqlar
Shuningdek o'qing: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||