1.1 ALKANLAR (to'yingan uglevodorodlar).
1.2 ALKANLAR ISHLAB CHIQARISH USULLARI.
1.3 ALKANLARNING VAKILLARI.
2.1 ALKENLAR (etilen uglevodorodlari).
2.2 ALKENLAR OLISH USULLARI.
2.3 ALKENLARNING VAKILLARI.
3.1 ALKINLAR (atsetilen uglevodorodlari).
3.2 ALKINLAR ISHLAB CHIQARISH USULLARI.
3.3 ALKINLARNING VAKILLARI.
4. ALKANLAR, ALKENLAR, ALKINLARNING QO'LLANISHI.
1.1 SATURAL uglevodorodlar (alkanlar).
To'yingan uglevodorodlar (alkanlar) - uglerod va vodorod atomlaridan tashkil topgan, bir-biri bilan faqat Q-bog'lar orqali bog'langan va tarkibida halqalar bo'lmagan birikmalar. Alkanlarda uglerod atomlari gibridlanishning sp3 darajasida bo'ladi.
1.2 Alkanlarni olish usullari.
Asosiy tabiiy manba to'yingan uglevodorodlar neft, gomologik qatorning birinchi a'zolari uchun esa - tabiiy gaz. Biroq, neft yoki uning yorilish mahsulotlaridan alohida birikmalarni ajratib olish juda ko'p mehnat talab qiladigan va ko'pincha imkonsiz ishdir, shuning uchun sintetik tayyorlash usullariga murojaat qilish kerak.
1. Alkanlar metall natriyning monogalogen hosilalarga ta'siridan hosil bo'ladi - Vurts reaktsiyasi:
H3C-CH2-Br + Br-CH2-CH3 CH3-CH2-CH2-CH3 + 2NaBr
Agar turli xil galogen hosilalari olinsa, u holda uch xil alkan aralashmasi hosil bo'ladi, chunki reaksiya kompleksida bir xil yoki turli molekulalarni uchratish ehtimoli teng va ularning reaktivligi yaqin:
3C2H5I + 3CH3CH2CH2IC4H10 + C5H12 + C6H14 + 6NaI
2. Alkanlarni alkenlar yoki alkinlarni vodorod bilan katalizatorlar ishtirokida qaytarish orqali olish mumkin:
NZC-CH=CH-CH3 NZC-CH2-CH2-CH3
3. Alkan hosilalarining xilma-xilligi yuqori haroratda gidroiyod kislota bilan qaytarilishi mumkin:
H3C H3C
CHBr +2HI CH2 + HBr + I2
H3C H3C
Biroq, bu hollarda uglerod skeletining qisman izomerlanishi kuzatiladi - ko'proq shoxlangan alkanlar hosil bo'ladi.
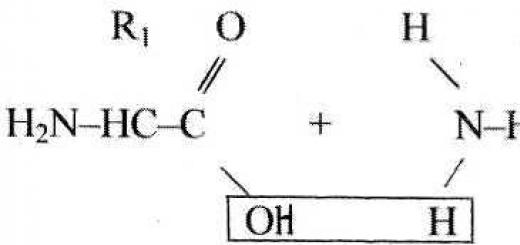
4. Alkanlarni tuzlarni eritish orqali olish mumkin karboksilik kislotalar ishqor bilan. Olingan alkan tarkibida asl karboksilik kislotadan bir uglerod atomi kamroq bo'ladi:
O
CH3-C + NaOH CH4 + Na2C03
ONA
1.3 Alkanlarning vakillari
A.M.Butlerovning tuzilish nazariyasiga ko‘ra, moddalarning fizik xossalari ularning tarkibi va tuzilishiga bog‘liq. Keling, to'yingan uglevodorodlar misolida o'zgarishni ko'rib chiqaylik jismoniy xususiyatlar gomologik qatorda.
Gomologik seriyaning birinchi to'rt a'zosi, metandan boshlab, gazsimon moddalar. Pentandan boshlab oddiy uglevodorodlar suyuqlikdir. Metan suyuqlikka faqat -162 °C da kondensatsiyalanadi. Seriyaning keyingi a'zolarining qaynash nuqtasi ortadi va keyingi gomologga o'tishda u taxminan 25 ° ga oshadi.
Uglevodorodlarning qaynash nuqtasidagi zichligi qatorning quyi a'zolari uchun avval tez, keyin esa tobora sekin ortadi: metan uchun 0,416 dan 0,78 dan biroz kattaroq qiymatgacha.Gomolog qatordagi oddiy uglevodorodlarning erish nuqtasi sekin ortadi. . C16H34 uglevodorodidan boshlab, oddiy haroratlarda yuqori gomologlar qattiq moddalardir.
Barcha tarmoqlangan alkanlarning qaynash harorati oddiy alkanlarnikidan pastroq va bundan tashqari, molekulaning uglerod zanjiri qanchalik shoxlangan bo'lsa, shuncha past bo'ladi. Buni, masalan, uchta izomer pentanning qaynash nuqtalarini taqqoslashdan ko'rish mumkin. Aksincha, eng ko'p tarmoqlangan uglerod zanjiriga ega bo'lgan izomerlar uchun erish nuqtasi eng yuqori bo'ladi. Shunday qilib, barcha izomerik oktanlardan faqat geksa-metil bosqichi (CH3)3C-C (CH3)3 qattiq allaqachon normal haroratda (mp 104 ° C). Bu naqshlar quyidagi sabablar bilan izohlanadi.
Suyuqlikning gazga aylanishi van der Vaalsning alohida molekulalarning atomlari orasidagi o'zaro ta'sir kuchlari tomonidan oldini oladi. Shuning uchun molekulada qancha atom bo'lsa, moddaning qaynash nuqtasi shunchalik yuqori bo'ladi, shuning uchun gomologik qatorda qaynash harorati bir xilda oshishi kerak. Agar n-pentan va neopentan molekulalari o'rtasidagi o'zaro ta'sir kuchlarini solishtirsak, bu kuchlar tarvaqaylab ketganlarga qaraganda oddiy uglerod atomlari zanjiriga ega bo'lgan molekula uchun ko'proq ekanligi aniq bo'ladi, chunki neopentan molekulasida markaziy atom odatda istisno qilinadi. o'zaro ta'sir.
Moddaning erish nuqtasiga ta'sir qiluvchi asosiy omil - bu molekulaning o'rash zichligi. kristall panjara. Molekula qanchalik nosimmetrik bo'lsa, uning kristalda to'planishi shunchalik zichroq va erish nuqtasi shunchalik yuqori bo'ladi (n-pentan uchun -132 ° C, neopentan uchun -20 ° C).
2.1 ALKENLAR (etilen uglevodorodlari, olefinlar)
Uglevodorodlar, ularning molekulasida, bundan tashqari oddiy Q-ulanishlar uglerod - uglerod va uglerod - vodorod uglerod-uglerod mavjud
-bog'lar to'yinmagan deb ataladi. -bog'ning hosil bo'lishi rasmiy ravishda molekula tomonidan ikkita vodorod atomining yo'qolishiga teng bo'lganligi sababli, to'yinmagan uglevodorodlar to'yingan uglevodorodlarga qaraganda 2n kam vodorod atomlarini o'z ichiga oladi, bu erda n - bog'lar soni.
C6H14 C6H12C6H10C6H8C6H6
A'zolari bir-biridan (2H)n ga farq qiladigan qator izologik qator deyiladi. Shunday qilib, yuqoridagi sxemada izologlar geksan, geksen, geksadien, geksin, geksatrien va benzoldir.
Tarkibida bir bogʻ (yaʼni qoʻsh bogʻ) boʻlgan uglevodorodlar alkenlar (olefinlar) yoki qatorning birinchi aʼzosi boʻlgan etilen, etilen uglevodorodlari deb ataladi. Ularning gomologik qatorlarining umumiy formulasi CnH2n
2.2 Alkenlarni olish usullari
Kaustik ishqorlarning spirtli eritmalari galogen hosilalariga ta'sir qilganda, galogen vodorod ajralib chiqadi va qo'sh bog' hosil bo'ladi:
H3C-CH2-CH2BrH3C-CH=CH2+NaBr+H2O
Propil bromid Propilen
Agar galogen bilan bog'langan uglerod atomining a-holatida uchinchi, ikkilamchi va birlamchi vodorod atomlari mavjud bo'lsa, unda uchinchi darajali vodorod atomi asosan ikkilamchi va ayniqsa birlamchi bo'linadi (Zaitsev qoidasi):
H3C-C-CI H3C-C + KCL + H2O
H3C CH3 H3C CH3
2,3-Dimetil-3-xloropentan 2,3-Dimethelpenten-2
Bu hosil bo'lgan alkenlarning termodinamik barqarorligi bilan bog'liq. Alkenning vinil uglerod atomlarida qanchalik ko'p o'rinbosarlari bo'lsa, uning barqarorligi shunchalik yuqori bo'ladi.
2. Suvni ajratuvchi moddalarning spirtlarga ta'siri: a) 300-400° S da alyuminiy oksidi ustidan spirtlarni o'tkazishda.
NzS-SN-SN2.-SNzNzS-SN=SN-SNz
OH Buten-2
Ikkinchi butil spirti
B) engil sharoitda spirtlarga sulfat kislota ta'sirida reaksiya sulfat kislota efirlarining oraliq hosil bo'lishi orqali sodir bo'ladi:
H3C-CH-CH3 H3C-CH=CH2
OH O-SO3H
izopropil spirti
Spirtli ichimliklarni kislotali muhitda og'ir sharoitlarda suvsizlantirishda vodorod atomlarini olishda ham xuddi shunday holat kuzatiladi. turli xil turlari, vodorod halidini yo'q qilishda bo'lgani kabi.
Ushbu jarayonning birinchi bosqichi spirtning protonlanishi bo'lib, undan so'ng suv molekulasi bo'linadi va karbokatiya hosil bo'ladi:
CH3-CH2-CH-CH3 + H CH3-CH2-CH-CH3 CH3-CH-CH-
OH O H
H H
CH3CH3-CH-CH-CH3CH3-CH=CH-CH3
Hosil bo'lgan karbokation qo'shni joydan protonning ajralib chiqishi bilan qo'sh bog'lanish (g-eliminatsiya) hosil bo'lishi bilan barqarorlashadi. Bunda eng shoxlangan alken ham hosil bo'ladi (termodinamik jihatdan barqarorroq). Ushbu jarayon davomida ko'pincha uglerod skeletining izomerizatsiyasi bilan bog'liq bo'lgan karbokatsiyalarning qayta tuzilishi kuzatiladi:
CH3 CH3
CH3 C-CH - CH3 CH3 C-CH-CH3
CH3 OH CH3
CH3 CH3 CH3 CH3
C-CH C=C
CH3 CH3 CH3 CH3
3. Zn yoki Mg ikkita bilan digalogen hosilalariga ta'sir qilganda
Qo'shni uglerod atomlarida halogen atomlari:
H3C – C CH2CIH3C - C - CH2+MgCI2
CH3 CH3
1,2-dikloro-2-metall-izobutilen
propan
4. Asetilen uglevodorodlarini faolligi pasaygan katalizatorlar (Fe yoki "zaharlangan", ya'ni katalitik faollikni kamaytirish uchun oltingugurt o'z ichiga olgan birikmalar bilan ishlov berish, Pt va Pd) ustida gidrogenlash:
HCC-CH(CH3)2H2C=CH-CH(CH3)2
2.3 Alkenlarning vakillari.
Ishqorlar singari, bir qator oddiy alkenlarning quyi gomologlari normal sharoitda gazlar bo'lib, C5 dan boshlab ular past qaynaydigan suyuqliklardir (jadvalga qarang).
T.pl., T. d4
Formula nomi °C qaynatiladi, °C
Ch2=CH2 Etilen -169 -104 0,5660 (-102° S da)
CH3CH=CH3 Propilen -185 -47 0,6090 (-47" C da)
CH3CH3CH=CH2 CH3-CH=CH-CH3 (cis)Buten-1 -130 -5 0,6696 (-5°C da) 0,6352 (O°C da)
-139 +4
(cis)
CH3-CH=CH-CH3 (trans)-Butep-2 -105 +1 0,6361 (0°C da)
(trans)
(CH3)3C=CH2 Ieobutilen -140 -7 0,6407 (0°C da)
Barcha alkenlar, xuddi alkanlar kabi, suvda amalda erimaydi va boshqa organik erituvchilarda yaxshi eriydi, metil spirti bundan mustasno; ularning barchasi suvga qaraganda kamroq zichlikka ega.
3.1 ALKINLAR (atsetilen uglevodorodlari)
Alkinlar uglevodorodlar bo'lib, Q-bog'lardan tashqari ikkitasini ham o'z ichiga oladi
-bir juft uglerod atomidagi bog'lar (uchlik bog'lar). Asetilen uglevodorodlarining gomologik qatorining umumiy formulasi CnH2n-2; bitta bog'ning hosil bo'lishi rasmiy ravishda ikki vodorod atomining yo'qolishiga teng.
Har xil jismoniy usullar bilan Asetilen C2H2 - alkinlarning gomologik qatorining eng oddiy vakili - uglerod-uglerod uch aloqasining uzunligi 1,20 A, uglerod-vodorod bog'larining uzunligi esa 1,06 A bo'lgan chiziqli molekulaga ega ekanligi isbotlangan.
S-N ulanishlari atsetilenda vodorodning s orbitalining uglerodning gibridlangan sp orbitali bilan qoplanishi natijasida hosil boʻlgan Q bogʻlar qatoriga kiradi; molekulada bitta uglerod-uglerod a-bog'i (uglerodning ikkita gibridlangan sp-orbitallarining bir-birining ustiga chiqishi natijasida hosil bo'lgan) va ikkita uglerod-uglerod bog'lari mavjud - bu ikkita o'zaro perpendikulyar juft "sof" p-orbitallarning bir-biriga yopishishi natijasidir ( P va P) qo'shni uglerod atomlari. Bog'lanish burchaklari atsetilenda, bu modelga asoslangan holda, 180 ° ga teng va molekula chiziqli konformatsiyaga ega bo'lib, bu uchlik bog'lanishda cis-trans izomeriyasini imkonsiz qiladi.
3.2 Alkinlarni olish usullari.
Ko'pchilik umumiy tarzda asetilen uglevodorodlarini ishlab chiqarish - ishqorlarning spirtli eritmasining galogen atomlarining vicinal (a) yoki geminal (b) joylashuvi bilan to'yingan uglevodorodlarning digalogen hosilalariga ta'siri.
a) CH2Br –CH2Br -> CHCH + 2HBr
b) SNz-SN2-SNSl2 ->SNz-SN+2ISl
CH3-CH2-CCl2-CH3 -> CH3-C C-CH3 + 2HC1
Vicinal digalogen hosilalari odatda etilen uglevodorodlariga galogenlarni qo'shish yo'li bilan olinganligi sababli (a) reaktsiyasini etilen uglevodorodlarini asetilen uglevodorodlariga aylantirish reaktsiyasi deb hisoblash mumkin.
Geminal digalogen hosilalari (bir uglerod atomidagi ikkala halogen atomi ham) ketonlar yoki aldegidlarning hosilalaridir va shuning uchun (b) reaktsiyalar yordamida karbonil birikmalaridan alkinlarga o'tishni amalga oshirish mumkin. Vodorod galogenidlarini yo'q qilishda allaqachon ma'lum bo'lgan Zaitsev qoidasi qo'llaniladi: vodorod kamroq miqdordagi vodorod atomlarini o'z ichiga olgan uglerod atomidan chiqariladi.
Asetilen to'g'ridan-to'g'ri metan yoki undan murakkab uglevodorodlarning yuqori haroratli (termik yoki elektrotermik) yorilishidan olinishi mumkin:
2SN4N-SS-N + ZN2
3.3 Alkinlarning vakillari.
Alkanlar va alkenlar kabi alkinlarning gomologik qatorining quyi a'zolari normal sharoitda gazsimon moddalardir. Jadval ma'lumotlari 22 ko'rib chiqilayotgan sinflardagi uglevodorodlarning asosiy fizik-kimyoviy xususiyatlari bir-biridan ozgina farq qilishini ko'rsatadi (jadvalga qarang).
Formula nomi Erish nuqtasi, °C Qaynash nuqtasi, °C D4
HCCHCH3CCHHCC- CH2CH3 CH3CCCH3 Asetilen PropinButin-1Butin-2 -82-105-137-33 -84(yuqori, -23) 927 0,6200 (-84°C da) 0,6785 (-27°60 da) ° C) 0,6880 (25 ° C da)
4. ALKANLAR, ALKINLAR, ALKENLARNING QO'LLANISHI
Alkenlar, alkanlar, asetilen va aromatik uglevodorodlar bilan birgalikda og'ir (keng ko'lamli) organik sintez sanoati uchun asosiy xom ashyolardan biridir.
Etilen polietilen va etil spirtini qayta ishlash uchun juda ko'p miqdorda ishlatiladi, etilen glikolga qayta ishlanadi va mevalarning pishishini tezlashtirish uchun issiqxonalarda ishlatiladi.
Propilen polipropilen, aseton va izopropil spirtiga qayta ishlanadi.
Asetilen sanoatda juda muhim rol o'ynaydi. Uning global ishlab chiqarilishi bir necha million tonnaga etadi. Ko'p miqdorda asetilen metallni payvandlashda, u yonganda ishlatiladi
kislorodda harorat 2800 ° S ga etadi. Bu metanning yonishi haqida gapirmasa ham, kislorodda vodorodning yonishidan sezilarli darajada yuqori haroratdir. Buning sababi, alkanlarning yonishi paytida alkinlarga qaraganda ko'proq hosil bo'ladigan H2O ga nisbatan CO2 ning sezilarli darajada past issiqlik sig'imidir:
2SzN6 + 7O2 -> 4SO2 + 6N2O
2S2 N2 + 5O2 -> 4SO2 + ZN2O
Karbiddan olingan asetilenning yoqimsiz hidi PH3 va AsH3 aralashmalari bilan bog'liq; toza asetilen barcha quyi uglevodorodlar (benzin) kabi hidlanadi. Asetilen va uning havo bilan aralashmalari juda portlovchi; asetilen gözenekli materiallarni singdiruvchi aseton eritmalari shaklida silindrlarda saqlanadi va tashiladi.
NEFT VA UNNI QAYTA QILISH
Yog 'tarkibi. To'yingan uglevodorodlarning asosiy tabiiy manbai neftdir. Yog'larning tarkibi sohaga qarab o'zgaradi, lekin oddiy distillashda barcha moylar odatda quyidagi fraktsiyalarga bo'linadi: gaz fraksiyasi, benzin, reaktiv yoqilg'i, kerosin, dizel yoqilg'isi, kerosin, neft smolasi.
Gaz fraktsiyasi (qaynoq harorati 40? C gacha) S gacha bo'lgan normal va tarmoqlangan alkanlarni, asosan propan va butanlarni o'z ichiga oladi. Gaz konlaridan chiqadigan tabiiy gaz asosan metan va etandan iborat.
Aviatsiya benzini (bp 40-180 °C) tarkibida C6 - C10 uglevodorodlar mavjud.Benzinda 100 dan ortiq individual birikmalar, jumladan, normal va tarmoqlangan alkanlar, sikloalkanlar va alkilbenzollar (arenlar) topilgan.
Reaktiv yoqilg'isi (bp 150-280 ° C).
Traktor kerosini (t, qaynash harorati 110-300 ° C) C7-C14 uglevodorodlarini o'z ichiga oladi.
C13 - C18 uglevodorodlarini o'z ichiga olgan dizel yoqilg'isi (qaynoq harorati 200-330 ° C) keng miqyosda yorilib, past molekulyar og'irlikdagi alkanlarga (va alkenlarga) aylanadi (pastga qarang).
Moylash moylari (bp 340-400 ° C) tarkibida C18 - C25 uglevodorodlar mavjud.
Neft parafin (bp 320-500 ° C), uning tarkibi C26-C38 uglevodorodlarini o'z ichiga oladi, ulardan neft jeli olinadi. Distillashdan keyin qoldiq odatda asfalt yoki smola deb ataladi.
Turli toifadagi uglevodorodlardan tashqari neft tarkibida kislorod, oltingugurt va azotli moddalar mavjud; ba'zan ularning umumiy tarkibi bir necha foizga etadi.
Hozirgi vaqtda eng mashhur nazariya - bu o'simlik va hayvon qoldiqlarining o'zgarishi mahsuloti sifatida neftning organik kelib chiqishi. Bu neft namunalarida porfirinlarning qoldiqlari, o'simlik va hayvonot steroidlari, shuningdek, "kimyofosillar" - plankton tarkibidagi turli xil parchalar topilganligi bilan tasdiqlanadi.
Neft kimyoviy xom ashyoning eng qimmatli tabiiy manbai ekanligi umumiy qabul qilingan bo'lsa-da, neft va neft mahsulotlarining asosiy qismi hali ham ichki yonuv dvigatellarida (benzin), dizel dvigatellarida va reaktiv dvigatellarda (kerosin) yondiriladi.
Dvigatel yoqilg'isi. Oktan soni. Turli xil kelib chiqishi benzinlari ichki yonuv dvigatellarida boshqacha harakat qiladi.
Kichik o'lchamlari va og'irligi bilan dvigatel quvvatini maksimal darajada oshirishga intilib, ular silindrdagi yonuvchi aralashmaning siqilish darajasini oshirishga harakat qilishadi. Biroq, majburiy ateşleme bilan ishlaydigan yuqori tezlikda ishlaydigan to'rt zarbali dvigatellarda, ba'zida aralashmaning muddatidan oldin yonishi sodir bo'ladi - portlash. Bu dvigatel quvvatini pasaytiradi va eskirishni tezlashtiradi. Bu hodisa suyuq yoqilg'ining tarkibi bilan bog'liq, chunki turli tuzilishdagi uglevodorodlar motor yoqilg'isi sifatida ishlatilganda o'zini boshqacha tutadi. Oddiy tuzilishdagi parafinlar uchun eng yomon ko'rsatkichlar.
Oddiy geptan yuqori portlash qobiliyatiga ega bo'lgan yonuvchan moddalar uchun standart sifatida olinadi. Parafin uglevodorodining uglerod zanjiri qanchalik tarmoqlangan bo'lsa, uning silindrda yonishi shunchalik yaxshi davom etadi va yonuvchi aralashmaning siqilish darajasiga erishish mumkin. Standart dvigatel yoqilg'isi 2, 2, 4-trimetilpentan (odatda izooktan deb ataladi) bo'lib, u taqillatishga qarshi yaxshi xususiyatlarga ega. Ushbu oktanning n-geptap bilan har xil nisbatdagi aralashmalarini hosil qilish orqali ularning dvigateldagi harakati sinovdan o'tgan benzinning harakati bilan taqqoslanadi. Agar 70% izooktanni o'z ichiga olgan aralashma xuddi o'rganilayotgan benzin kabi harakat qilsa, ikkinchisining oktan soni 70 ga teng deb aytiladi (izooktanning oktan soni 100 ga teng; n-geptanning oktan soni). nolga teng).
Uchqunli dvigatellar uchun yoqilg'ining taqillatishga chidamliligini oshirish usullaridan biri bu taqillatishga qarshi vositalardan foydalanishdir.
Antiknock agentlari - taqillatishga qarshi xususiyatlarini yaxshilash uchun benzinga qo'shiladigan moddalar (0,5% dan ko'p bo'lmagan). Tetraetil qo'rg'oshin (TEP) Pb (C2H5) 4 taqillatishga qarshi juda samarali vositadir.
Biroq, issiqlik elektr stansiyalarining benzini va uning yonish mahsulotlari juda zaharli hisoblanadi. Hozirgi vaqtda siklopC5H5Mn (CO)5 kabi marganets-organik birikmalar asosida yangi zarbaga qarshi vositalar topildi: ular kamroq zaharli va yaxshi taqillatuvchi xususiyatlarga ega. Ushbu anti-taqillatuvchi vositalarni benzinning yaxshi navlariga qo'shish sizga 135 gacha oktanli yoqilg'ini olish imkonini beradi.
Raketa va dizel dvigatellari uchun, aksincha, eng qimmatli yoqilg'i uglerod atomlarining oddiy zanjiriga ega bo'lib, eng past tutashuv haroratiga ega. Bu xususiyat qabul qilinadi
setan sonida baholang. Setan soni 100 uglevodorod n-Sc,Nd4 uchun, setan soni esa 1-metilnaftalin uchun 0 ga teng.
CO+H2 dan uglevodorodlar sintezi. Uglerod oksidi (II) va vodorod aralashmasini 250 ° C da mayda maydalangan nikel ustiga o'tkazib, metan olish mumkin:
CO+3N2CH4+H2O
Agar bu reaktsiya 100-200 atm bosim va 400 ° S gacha bo'lgan haroratda amalga oshirilsa, asosan kislorod o'z ichiga olgan mahsulotlardan iborat aralashma olinadi, ular orasida spirtlar ustunlik qiladi; Bu aralashma schshpol deb nomlangan.
Temir-kobalt katalizatorlari va 200 ° S haroratda ishlatilganda alkanlar aralashmasi - sintin hosil bo'ladi.
nSO + (2n + 1) N2 SnN2n + 2 + H2O
Sintin va sintol keng ko'lamli organik sintez mahsulotlari bo'lib, ko'plab kimyo sanoati uchun xom ashyo sifatida keng qo'llaniladi.
Klatratlar. Neftning sintin va benzinli fraktsiyalari oddiy tuzilishdagi va tarmoqlangan zanjirli uglevodorodlar aralashmalaridan iborat. Yaqinda topilgan samarali usul yilda olingan oddiy zanjirlar va shoxlanganlar bilan organik birikmalarni ajratish umumiy holat klatrat ajratish usulining nomi. Karbamid uglevodorodlarni ajratish uchun ishlatilgan. Karbamid kristallari shunday qurilganki, kristallar ichida tor olti burchakli kanallar mavjud. Bu kanallarning diametri shundayki, ular orqali faqat normal tuzilishga ega uglevodorodlar o'tishi va adsorbsion kuchlar ta'sirida saqlanib qolishi mumkin. Shuning uchun, organik birikmalar aralashmasi karbamid (yoki ba'zi boshqa birikmalar) bilan ishlov berilganda, oddiy uglerod atomlari zanjiriga ega bo'lgan moddalar u bilan birga komplekslar shaklida kristallanadi. Bu usul, albatta, juda katta kelajakka ega - topilganda kattaroq raqam samarali klatrat hosil qiluvchilar.
BUTADYEN-1,3 (DIVINIL) OLISH
Butadien-1,3 CH 2 =CH-CH-CH 2 sintetik kauchuklar ishlab chiqarish uchun asosiy monomerdir.
S.V.Lebedev tomonidan ishlab chiqilgan etanoldan butadien-1,3 sintezi monomer olishning birinchi sanoat usuli bo'lib, uning asosida 1932 yilda dunyoda birinchi marta sintetik kauchuk ishlab chiqaruvchi zavod ishga tushirildi. .
Umumiy reaksiya tenglamasini quyidagicha yozish mumkin
2C 2 H 5 OH ® C 4 H 6 + H 2 + 2H 2 O, DH = 85 kJ
Tenglama shuni ko'rsatadiki, umumiy reaksiya kondensatsiya, suvsizlanish va suvsizlanishning kombinatsiyasidan iborat. Lebedev tomonidan taklif qilingan, gidrogenlashtiruvchi va suvsizlantiruvchi komponentlarni o'z ichiga olgan ikki funktsiyali oksidli katalizator ushbu talablarga javob beradi. Biroq, endi usul amaliy ahamiyatini yo'qotdi. Usulning asosiy kamchiligi uning past selektivligidir (hatto 100% etanoldan divinilning nazariy hosildorligi 58,7% ni tashkil qiladi).
Hozirgi vaqtda divinilni sintez qilishning asosiy usullari dehidrogenatsiya hisoblanadi n-tabiiy gazdan ajratilgan butan va neft mahsulotlarining pirolizidan butan-butilen fraksiyalarini kompleks qayta ishlash, shu jumladan butadien ekstraktsiyasi, izobutilenni ajratish va dehidrogenlash. n-butilenlardan butadiengacha.
Butanni gidrogenlashda termodinamik cheklovlar muhim rol o'ynaydi, buning natijasida 1,3-butadienni bir bosqichda oddiy sharoitlarda texnik jihatdan maqbul rentabellik bilan va faqat maxsus texnikalar yordamida olish deyarli mumkin emas. vakuum, oksidlovchi dehidrogenatsiya) hosildorlikni kerakli darajaga ko'tarish mumkin.
Butandan divinil ishlab chiqarish uchun sanoat inshootlarining ko'pchiligi ikki bosqichli sxema bo'yicha ishlaydi. Butan dehidrogenatsiyasining birinchi bosqichi uni butilenga aylantirish, ikkinchisi esa butilendan divinil olish jarayonidir.
Alyuminiy oksidida qo'llab-quvvatlanadigan xrom oksidi rag'batlantirilgan katalizatorda butanning butilenga dehidrogenatsiyasi reaksiya orqali davom etadi.
C 4 H 10 ® C 4 H 8 + H 2, DH = 131 kJ
Tarkibi......Al 2 O 3 Fe 2 O 3 Cr 2 O 3 SiO 2 KNO 3 CaO H 2 O
Massa ulushi, % 66,10 1,72 15,8 7,9 4,93 0,14 3,34
Butanni gidrogenlash jarayonida katalizator uglerod konlari bilan qoplanadi va uni o'zgartiradi Kimyoviy tarkibi. Bunda katalizatorning faolligi keskin pasayadi. Qayta faollashtirish uchun katalizator doimiy ravishda reaktordan chiqariladi va suyuq qatlamli regeneratorda havo oqimida yondiriladi. Bunda uglerod birikmalari yonib ketadi va quyi xrom oksidlari Cr 2 Oz ga oksidlanadi. Texnologiya tizimi butan dehidrogenatsiya zavodi shaklda ko'rsatilgan. 1.
Butan quritgichga suyuqlik shaklida kiradi. 1 , adsorbent (A1 2 O 3, zeolitlar) bilan to'ldirilgan va keyin bug'latgichga 2. Olingan bug'lar quvurli pechda isitiladi 3 780-820 K haroratgacha va reaktor taqsimlash tarmog'i ostiga kiradi 4 dehidrogenlash uchun. Reaktsiya davom etishi uchun zarur bo'lgan issiqlik miqdori regenerator 5 dan qizdirilgan regeneratsiyalangan katalizator oqimi bilan ta'minlanadi. Regeneratordagi harorat 890-920 K. Regeneratsiya qilingan katalizator yuqori taqsimlash tarmog'iga va shuning uchun katalizatorga beriladi. va reaksiya gazlari teskari oqim bilan harakatlanadi. Yuqori qismida reaksiya gazlarini o'chirish uchun lasan mavjud. Buning yordamida gazlarning harorati tezda 720-750 K gacha pasayadi va ularning keyingi parchalanishining oldi olinadi.
| |
Katalizator regeneratorga havo oqimi bilan, reaktorga esa asl uglevodorod yoki azot bug'i bilan etkaziladi. Reaktordan kontakt gazi qayta tiklash qozoniga yuboriladi 6 ikkilamchi bug 'ishlab chiqarish, so'ngra katalizator changini ushlash va keyingi sovutish uchun - suv bilan sug'orilgan 7-srubberga. Regeneratordan chiqadigan tutun gazlari elektr cho'ktirgichda katalizator changidan tozalanadi. 8, keyin skrubberdan o'tadi va atmosferaga chiqariladi.
Yo'qotishlarni qoplash va faollikni saqlash uchun tizimda aylanib yuradigan katalizatorga har kuni yangi katalizator qo'shiladi. Tozalangan aloqa gazi turbokompressorga kiradi 9, tushirish bosimi taxminan 0,5 MPa, keyin esa kondensatsiya tizimiga 10, Bu erda sovutgich sifatida suv va qaynayotgan propan ketma-ket ishlatiladi. Kondensatsiyalanmagan mahsulot absorberga yuboriladi 11 . Absorbtsiya C 6 -C 12 uglevodorodlar aralashmasi bilan amalga oshiriladi. Eritilgan butilen tozalagichda distillanadi 12 va kondensatordan suyultirilgan mahsulot bilan aralashmalar 10 distillash ustuni tizimiga kiradi 13 Va 14. Ustunlarda past va yuqori qaynaydigan aralashmalar dehidrogenatsiya mahsulotidan distillanadi (ikkinchisi yo'qotishlarni qoplash uchun aylanma changni yutish vositasiga qo'shiladi). Butan dehidrogenlash mahsulotlari ekstraktiv rektifikatsiya qurilmasiga yuboriladi 15 butilen fraktsiyasini ajratib olish uchun.
Butilenning divinilga degidrogenlanishi da sodir bo'ladi
reaktsiya uchun kaltsiy xrom fosfat katalizatori
C 4 H 8 ® C 4 H 8 + H 2, DH = 119 kJ.
Butilenni gidrogenatsiyalashning texnologik sxemasi 2-rasmda ko'rsatilgan.
| |
 Boshlang'ich butilen fraktsiyasi va suv bug'lari quvurli pechlarda qizdiriladi 1
Va 2
mos ravishda 770 va 990 K gacha, in'ektsiya mikserida reaktordan oldin darhol aralashtiriladi. 3
va reaktor blokiga yuboriladi 4.
Reaktorning chiqishidagi gaz-bug 'aralashmasi suv kondensati bilan "so'ndiriladi", darhol 810 K ga sovutiladi. Har bir reaktor chiqindi issiqlik qozoni 5 bilan jihozlangan, shundan so'ng aloqa gazi qo'shimcha ravishda sovutiladi va tozalanadi. ikkita tozalagich 6
va 7, birinchisi dizel yoqilg'isi, ikkinchisi esa suv bilan sug'oriladi. Skrubberlarda suv bug'lari to'liq kondensatsiyalanadi. Skrubberdan 7 chiqqandan keyin gaz kompressorda siqiladi 8
va kondensatsiya tizimida kondensatsiyalanadi 9.
Kondensatsiyalanmagan uglevodorodlar qo'shimcha ravishda absorber-desorber qurilmasida olinadi 10
Va 11
. Absorbent qo'shimcha mahsulot sifatida hosil bo'lgan C 6 -C 12 uglevodorodlardir. Umumiy suyultirilgan oqim ustunlarga yo'naltiriladi 12
Va 13
past va yuqori qaynaydigan aralashmalarni oldindan ajratish va undan keyin ekstraktiv rektifikatsiya qilish uchun 14.
Butilen konvertatsiyasi o'rtacha 40-45% ni, divinil uchun selektivlik taxminan 85% ni tashkil qiladi.
Boshlang'ich butilen fraktsiyasi va suv bug'lari quvurli pechlarda qizdiriladi 1
Va 2
mos ravishda 770 va 990 K gacha, in'ektsiya mikserida reaktordan oldin darhol aralashtiriladi. 3
va reaktor blokiga yuboriladi 4.
Reaktorning chiqishidagi gaz-bug 'aralashmasi suv kondensati bilan "so'ndiriladi", darhol 810 K ga sovutiladi. Har bir reaktor chiqindi issiqlik qozoni 5 bilan jihozlangan, shundan so'ng aloqa gazi qo'shimcha ravishda sovutiladi va tozalanadi. ikkita tozalagich 6
va 7, birinchisi dizel yoqilg'isi, ikkinchisi esa suv bilan sug'oriladi. Skrubberlarda suv bug'lari to'liq kondensatsiyalanadi. Skrubberdan 7 chiqqandan keyin gaz kompressorda siqiladi 8
va kondensatsiya tizimida kondensatsiyalanadi 9.
Kondensatsiyalanmagan uglevodorodlar qo'shimcha ravishda absorber-desorber qurilmasida olinadi 10
Va 11
. Absorbent qo'shimcha mahsulot sifatida hosil bo'lgan C 6 -C 12 uglevodorodlardir. Umumiy suyultirilgan oqim ustunlarga yo'naltiriladi 12
Va 13
past va yuqori qaynaydigan aralashmalarni oldindan ajratish va undan keyin ekstraktiv rektifikatsiya qilish uchun 14.
Butilen konvertatsiyasi o'rtacha 40-45% ni, divinil uchun selektivlik taxminan 85% ni tashkil qiladi. PARAFINLAR VA ULARNING GALOGEN HOSILALARINI XLORLASH
Sanoatda termal xlorlash gaz fazasida xlor molekulalarini faollashtirish uchun zarur bo'lgan haroratda amalga oshiriladi, bu radikal zanjir reaktsiyasini keltirib chiqaradi: C1 2 ® C1 × + C1 ×
RH + S1× ® R + HCl
R + Cl 2 ® RCl + C1× va boshqalar.
Vodorod atomlarini xlor atomlari bilan almashtirish reaktsiyasi olib keladi
mono-, di- va polixlorli mahsulotlar aralashmasi hosil bo'lishiga va vodorod xloridning chiqarilishiga.
U yoki bu mahsulotning ustun shakllanishi reaksiya sharoitlari bilan belgilanadi; harorat rejimi va uglevodorod va xlorning molekulyar nisbati (3-rasm).

Metanni xlorlash xloratorda (4-rasm) amalga oshiriladi, u ichki tomondan shamotli g'isht bilan qoplangan po'lat silindrsimon korpusdir. 2, uning yuqori qismida chinni halqalardan yasalgan nozul mavjud 3, yagona reaktsiyani rag'batlantirish. Xloratorning ichki qismi balandligining yarmini ochiq keramik vertikal silindr egallaydi. 4 pastki qismida teshiklari bo'lgan, uning ichiga xom ashyoni etkazib beradigan keramik quvur toraygan halqa bilan tushiriladi. Jarayon xloratorning ichki qismini oldindan qizdirish bilan boshlanadi (reaksiyani boshlash uchun). Isitish havo bilan aralashtirilgan metanning bir qismini yoqish, so'ngra havoni xlor bilan almashtirish orqali amalga oshiriladi. Keyinchalik reaksiya avtotermik tarzda davom etadi. Xlorlash mahsulotlari apparatning yuqori qismidan chiqariladi, so'ngra vodorod xlorid kislota absorberlarida gaz aralashmasidan suv bilan olinadi (xlorid kislotasi olinadi), gaz aralashmasi ishqor bilan neytrallanadi, muzlatib quritiladi, siqiladi va suyultiriladi. chuqur sovutish. Alohida mahsulotlar metilxlorid 28-32%, metilenxlorid 50-53%, xloroform 12-14% va uglerod tetraklorid 3-5% ni o'z ichiga olgan suyuqlik aralashmasidan rektifikatsiya yordamida ajratib olinadi.
Barcha xlorli metan birikmalari topilgan keng qo'llanilishi. Shunday qilib, metilxlorid CH 3 C1 butil kauchuk ishlab chiqarishda erituvchi sifatida, organik sintezda metillashtiruvchi vosita sifatida, silikonorganik polimerlar - silikonlarni ishlab chiqarishda boshlang'ich material bo'lib xizmat qiladigan metilxlorosilanlarni olish uchun ishlatiladi. Metilenxlorid CH 2 C1 2 tsellyuloza asetat, yog'lar, yog'lar, kerosin, kauchuklar uchun qimmatli sanoat erituvchidir; u yonuvchan emas va havo bilan portlovchi aralashmalar hosil qilmaydi.
BENZOLNI XLORLASH
Benzolni xlorlash orqali xlorlash sharoitiga qarab monoxlorbenzol yoki boshqa xlorli hosilalar olinadi. Shunday qilib, 310-330 K va benzol va xlorning molyar nisbati 1:0,6 da temir katalizatorida monoxlorbenzol hosil bo'ladi; nisbati pastroq va A1C1 3 katalizatori bilan asosan o-diklorbenzol olinadi (bo'yoqlar va zararkunandalarga qarshi vositalar sintezida ishlatiladi); ultrabinafsha nurlanish ostida bir xil haroratda geksaxlorotsiklogeksan olinadi. Shaklda. 5-rasmda ortiqcha benzolning bug'lanishi hisobiga ekzotermik reaksiyaning issiqligini olib tashlash bilan xlorbenzolni olish sxemasi ko'rsatilgan.
 Xlorlash po'lat silindrsimon apparatda amalga oshiriladi,
Xlorlash po'lat silindrsimon apparatda amalga oshiriladi,
| |
uglevodorodlarni xlorlash jarayonlarida hosil bo'lgan vodorod xloriddan foydalanish muammosi.
Vodorod xlorid - neftni qayta ishlashdan olingan kerosin va aromatik uglevodorodlarni xlorlashdan olingan chiqindi mahsulot bo'lib, sanoatda keng qo'llaniladi. organik sintez. Qayta ishlash xlorlash mahsulotlarining tannarxini pasaytirish, sanitariya sharoitlarini yaxshilash va metall korroziyasiga qarshi kurashish bilan bog'liq dolzarb vazifadir.
Vodorod xloridning bir qismi ishlab chiqarish uchun ishlatiladi xlorid kislotasi HC1 ning suv bilan qarama-qarshi yutilishi bilan. Biroq, xlorid kislotaga bo'lgan mahalliy ehtiyojlar, odatda, uni vodorod xloriddan ishlab chiqarish imkoniyatlaridan ancha past. Xlorid kislotani uzoq masofalarga tashish uning yuqori korroziv qobiliyati tufayli qiyin.
HC1 dan foydalanishning istiqbolli usuli oksidlovchi xlorlash usuli hisoblanadi. Zamonaviy sanoatda bu usul yordamida etilendan vinilxlorid sintez qilinadi: oksidlovchi xlorlash reaktorida etilen 1,2-dikloroetanga aylanadi, uning katalitik parchalanishi vinilxloridni hosil qiladi; Bu holda hosil bo'lgan HC1 yana reaktorga yuboriladi:
2CH 2 = CH 2 + 4HC1 + O 2 ® 2CH 2 C1-CH 2 C1 + 2H 2 O, DH = –238 kJ/mol CH 2 C1-CH 2 C1 ® CH 2 = CHCI + HC1.
Oksidlanish xlorlash jarayoni katalizator (inert tashuvchida mis xlorid) ishtirokida 530-570 K da sodir bo'ladi; dikloroetanning pirolizi 770 K da g'ovak katalizatorda (pomza) amalga oshiriladi.
| |

Shaklda. 6-rasmda vinilxloridni etilendan sintez qilishning soddalashtirilgan sxemasi keltirilgan. Mikserda 1 etilen, qayta ishlanadigan gaz va vodorod xlorid kislorod bilan aralashtiriladi va reaktorga beriladi. 2 suyuq katalizator bilan; hosil bo'lgan dikloroetan va reaksiyaga kirmagan etilen, kislorod va HC1 bug'lari to'g'ridan-to'g'ri aralashtiriladigan muzlatgichda sovutiladi. 3 muzlatgichdan keladigan suv va dikloroetan aralashmasi 4. Keyin gaz-bug 'aralashmasi issiq ishqoriy tozalash moslamasidan 5 o'tadi, unda HCl va CO 2 dan tozalanadi, muzlatgichda sovutiladi va gaz ajratgichdan o'tadi. 6, gazlardan ajratiladi - etilen va kislorod aralashmasi, ular reaktorga qaytariladi (gazni qayta ishlash). 7-separatordagi dikloroetan suvdan ajraladi va quritish ustuniga kiradi 8, bu erda azeotrop distillashdan foydalanib, u nihoyat suvsizlanadi va distillash ustuniga beriladi. 9; dikloroetan kollektorda yig'iladi 10. Vinilxlorid hosil qilish uchun dikloroetanning keyingi pirolizlanishi quvurli pechda sodir bo'ladi. 11 ; o'choqdan olingan reaktsiya aralashmasi to'g'ridan-to'g'ri aralashtirish muzlatgichiga kiradi, sovutilgan dikloroetanni aylanma orqali sovutiladi va muzlatgichdan o'tgandan keyin 4, distillash ustuniga kiradi 12, Bu erda HC1 ajratiladi, u oksidlovchi xlorlash reaktoriga qaytariladi va vinilxlorid va konvertatsiya qilinmagan dikloroetan distillash kolonnasida ajratiladi. 13; dikloroetan ustunga qaytariladi 9, va vinilxlorid polimerizatsiya uchun yuboriladi.
Neftni qayta ishlash gazlariga asoslangan korxonalarni birlashtirish, xususan, etilen va asetilen va vinilxloridni birgalikda qayta ishlashni qayta ishlash uchun katta qiziqish uyg'otadi; Etilendan vinilxlorid ishlab chiqarishda hosil bo'lgan vodorod xlorid asetilenni gidroxlorlash uchun ishlatiladi:
CH 2 = CH 2 + C1 2 ® CH 2 C1-CH 2 C1 (piroliz) ® CH 2 = CH 1 + HCI
SNºSN + HC1 ® SN 2 = SNS1
Vodorod xloriddan foydalanishning iqtisodiy usuli bu xlor bilan almashtirilgan metanni olish uchun metan xlorlash bilan oksidlovchi xlorlanishni birlashtirishdir:
CH 4 + 4S1 2 ® CCI 4 + 4HCI
CH 4 + 4HC1 + O 2 ® SS! 4 + 2H 2 O
Bu jarayonda uglerod tetrakloriddan tashqari metilenxlorid va xloroform hosil bo‘ladi. Tetraxlorid uglerod erituvchi sifatida, qishloq xoʻjaligida (fumigant), yongʻinlarni oʻchirishda va boshqalarda ishlatiladi.Xloroform fenollar, ftoroplastlar va boshqalar sintezida qimmatli oraliq mahsulotdir.
Xlorbenzol, shuningdek, aralash katalizatorda (A1 2 O 3 - CuC1 2 - FeCl 3) benzol, vodorod xlorid va havo (kislorod) bug'-gaz aralashmasidan 500 K da oksidlovchi xlorlash orqali olinadi:
C 6 H 6 + HC1 + 1/ 2 O 2 ® C 6 H 5 C1 + H 2 O
Vodorod xloriddan foydalanish uchun siz uning elektrokimyoviy oksidlanishini xlorga aylantirishingiz mumkin.
Xrom seziy katalizatori va uni vodorod xloridni xlorga oksidlash, ya'ni organik birikmalarni xlorlash natijasida chiqindi gazlardan xlorni qayta tiklash uchun foydalanish usuli taklif qilingan.
ASETILEN ISHLAB CHIQARISH VA UNNI KAYTALASH
Kaltsiy karbidini parchalash orqali asetilen ishlab chiqarish atsetilen generatorlarida nam va quruq usullar bilan reaksiya tenglamasiga muvofiq amalga oshiriladi:
CaC 2 + 2H 2 O ® C 2 H 2 + Ca (OH) 2 DH = -127 kJ.
"Suvga karbid" printsipi bo'yicha ishlaydigan generatorlarda nam usulda ezilgan kaltsiy karbid ko'p miqdorda suv bo'lgan generatorga bir xilda beriladi, uning isishi tufayli jarayon davomida chiqarilgan issiqlik chiqariladi. Ushbu sxemada ishlatiladigan asbob-uskunalar va ayniqsa, hosil bo'lgan loyni va suv aylanishini olib tashlash uchun kommunikatsiyalar juda og'ir. Bundan tashqari, 70% gacha suv o'z ichiga olgan suyuq ohak sutini tashish va ishlatish katta qiyinchiliklarni keltirib chiqaradi.
Uglevodorodlardan atsetilen olishning samarali sanoat usullari ham ishlab chiqilgan. Parafinlardan asetilen quyidagi qaytariladigan endotermik reaktsiyalar natijasida hosil bo'ladi:
2CH 4 D C 2 H 2 + H 2 DH = 376 kJ
C 2 H 6 D C 2 H 2 + 2H 2 DH = 311 kJ
C 3 H 8 D C 2 H 2 + CH 4 + H 2 DH = 255 kJ
CH 4 D C + 2H 2 DH = 88 kJ
Reaksiya (d) yon reaksiya hisoblanadi.
Haroratning oshishi bilan reaksiyalar muvozanati asetilen hosil bo'lishi tomon siljiydi. Metan uchun yuqori darajadagi muvozanat konvertatsiyasi T>1670 K, etan uchun - 1170 K. Lekin >1680 K haroratda asetilen va uglevodorodlar beqaror bo'lib, kuyik va uglerodga parchalanadi.
Ishlab chiqarishda qabul qilingan 1670-1770 K haroratlarda metanni asetilenga aylantirish reaktsiyasi asetilenning elementlarga parchalanishi reaktsiyasiga qaraganda tezroq ketadi, shuning uchun reaktsiya mahsulotlari tezda soviydi, bu asetilenning parchalanishini oldini olishga yordam beradi; xuddi shu maqsadda yuqori hajmli gaz tezligidan foydalaniladi, bunda xom ashyo faqat soniyaning mingdan bir qismi reaktsiya zonasida bo'lishi kerak.
Asetilen hosil bo'lishining ekzotermik reaksiyasini amalga oshirish uchun issiqlik berish usuliga ko'ra, jarayonni o'tkazishning quyidagi usullari ajratiladi: 1) gazsimon uglevodorodlarni yoki suyuq mahsulotlarni elektrokreking; 2) bir hil piroliz; 3) termik-oksidlovchi piroliz.
Elektrokraking to'g'ridan-to'g'ri oqim elektr kamon pechlarida voltaik yoy yordamida amalga oshiriladi.
Bir hil piroliz taxminan 2200 K haroratda issiq tutun gazlari oqimida xom ashyoning parchalanishidan iborat.
Termooksidlovchi pirolizda zarur issiqlik metanning bir qismini yoqish orqali olinadi.
Asetilen ishlab chiqarish uchun karbid usulining asosiy kamchiliklari kaltsiy karbidini ishlab chiqarishda yuqori energiya sarfi va bir necha bosqichda qayta ishlanadigan ko'p miqdorda iste'mol qilinadigan xom ashyo (ohaktosh va koks) hisoblanadi. Shu bilan birga, karbid usuli konsentrlangan asetilenni ishlab chiqaradi, uni kichik aralashmalardan tozalash qiyinchilik tug'dirmaydi.
Termal uglevodorodlarni bo'lish usullari bir bosqichda asetilenga aylanadigan kamroq miqdordagi xom ashyoni ishlatadi, ammo asetilen suyultiriladi va uni talab qiladi. murakkab tizim uning tozalanishi va kontsentratsiyasi. Shuni ta'kidlash kerakki, karbid usuli dunyoda ishlab chiqarilgan asetilenning taxminan 70% ni ishlab chiqaradi.
Asetilenni birlamchi qayta ishlashning quyidagi asosiy usullari mavjud.
Hidratsiya:
a) atsetaldegid va sirka kislotasini (katalizator (HgSO 4) hosil qilish uchun):
b) aseton ishlab chiqarish (faollashtirilgan uglerodda ZnO katalizatori)
2CH = CH + 3H 2 O ® CH 3 COCH 3 + CO 2 + 2H 2
Polimerizatsiya sintetik kauchuk monomerlari va tolalarini olish uchun chiziqli va siklik moddalarga.
Xlorlash erituvchilar va monomerlarni olish.
Asetilen bilan vinillash monomerlarni hosil qilish uchun turli moddalar:
ROH ® ROCH=CH 2
RCOOH ® RCOOCH=CH 2
Rossiya Federatsiyasi Ta'lim vazirligi
Kursk davlat qishloq xo'jaligi
nomidagi akademiyasi Prof. I. I. Ivanova
ANTRACT ON
Organik kimyo
ALKANLAR, ALKENLAR, ALKINLARNI OLISH.
MUHIM VAKILLAR.
SANOAT ISHLAB CHIQISH.
Bajarildi:
KURSK-2001
Reja.
1.1 ALKANLAR (to'yingan uglevodorodlar).
1.2 ALKANLAR ISHLAB CHIQARISH USULLARI.
1.3 ALKANLARNING VAKILLARI.
2.1 ALKENLAR (etilen uglevodorodlari).
2.2 ALKENLAR OLISH USULLARI.
2.3 ALKENLARNING VAKILLARI.
3.1 ALKINLAR (atsetilen uglevodorodlari).
3.2 ALKINLAR ISHLAB CHIQARISH USULLARI.
3.3 ALKINLARNING VAKILLARI.
4. ALKANLAR, ALKENLAR, ALKINLARNING QO'LLANISHI.
1.1 SATURAL uglevodorodlar (alkanlar).
Toʻyingan uglevodorodlar (alkanlar) atomlardan tashkil topgan birikmalardir
uglerod va vodorod, bir-biriga faqat Q-bog'lar orqali bog'langan va o'z ichiga olmaydi
sikllar. Alkanlarda uglerod atomlari gibridlanish darajasida bo'ladi sp3.
1.2 Alkanlarni olish usullari.
To'yingan uglevodorodlarning asosiy tabiiy manbai neft va uchun
gomologik qatorning birinchi a'zolari tabiiy gazdir. Biroq, ajratish
neft yoki uning kreking mahsulotlaridan individual birikmalar juda
mehnat talab qiladigan va ko'pincha imkonsiz vazifa, shuning uchun siz murojaat qilishingiz kerak
sintetik ishlab chiqarish usullari.
1. Alkanlar hosil bo'ladi metall natriyning ta'sirida
monogalogen hosilalari - Wurtz reaktsiyasi:
H3C-CH2-Br + Br-CH2-CH3 CH3-CH2-CH2-CH3 + 2NaBr
Agar turli xil halogen hosilalari olinadigan bo'lsa, uch xil aralashmasi
alkanlar, chunki reaksiya kompleksida molekulalarning uchrashish ehtimoli
bir xil yoki turli xillar teng va ularning reaktivligi yaqin:
3C2H5I + 3CH3CH2CH2IC4H10 + C5H12 + C6H14 + 6NaI
2. Alkanlarni ishlab chiqarish mumkin alkenlar yoki alkinlarning qaytarilishida
vodorod katalizatorlar ishtirokida:
NZC-CH=CH-CH3 NZC-CH2-CH2-CH3
3. Alkan hosilalari xilma-xil bo'lishi mumkin da qayta tiklandi
yuqori haroratli gidroiod kislotasi:
CHBr +2HI CH2 + HBr + I2
Biroq, bu holatlarda uglerodning qisman izomerizatsiyasi
skelet - ko'proq shoxlangan alkanlar hosil bo'ladi.
4. Alkanlarni ishlab chiqarish mumkin bilan karboksilik kislotalarning tuzlarini eritganda
gidroksidi. Olingan alkanda bitta kam uglerod atomi mavjud,
asl karboksilik kislotaga qaraganda:
CH3-C + NaOH CH4 + Na2C03
1.3 Alkanlarning vakillari
A. M. Butlerovning tuzilish nazariyasiga ko'ra, moddalarning fizik xususiyatlari bog'liq
ularning tarkibi va tuzilishi haqida. Keling, to'yingan uglevodorodlar misolini ko'rib chiqaylik
homolog qatordagi fizik xususiyatlarning o'zgarishi.
Metandan boshlangan gomologik qatorning dastlabki to'rt a'zosi gazsimon
moddalar. Pentan va undan yuqorisidan boshlab, oddiy uglevodorodlar
suyuqlikdir. Metan suyuqlikka faqat -162 °C da kondensatsiyalanadi. Keyingi
qator a'zolari, qaynoq nuqtasi ortadi, va keyingi harakat qachon
homolog u taxminan 25 ° ga oshadi.
Seriyaning quyi a'zolari uchun uglevodorodlarning qaynash nuqtasidagi zichligi
avval tez, keyin esa tobora sekin ortadi: metan uchun 0,416 dan
qiymatlar 0,78 dan biroz kattaroq.Erish nuqtasi normal
gomologik qatordagi uglevodorodlar sekin ortadi. bilan boshlanadi
uglevodorod C16H34, oddiy haroratda yuqori gomologlar - moddalar
Barcha shoxlangan alkanlarning qaynash harorati oddiy alkanlarnikidan past.
alkanlar va bundan tashqari, molekulaning uglerod zanjiri qanchalik past bo'lsa, shuncha ko'p tarmoqlanadi.
Buni, masalan, uchta izomer pentanning qaynash nuqtalarini taqqoslashdan ko'rish mumkin.
Aksincha, erish nuqtasi bilan izomerlar uchun eng yuqori
maksimal tarvaqaylab ketgan uglerod zanjiri. Shunday qilib, barcha izomerik oktanlar
faqat geksa-metil bosqichi (CH3)3C-C (CH3)3 allaqachon qattiq moddadir.
normal harorat (mp 104 ° C). Bu naqshlar tushuntiriladi
quyidagi sabablarga ko'ra.
Suyuqlikning gazga aylanishi van der Vaals o'zaro ta'sir kuchlari tomonidan oldini oladi
alohida molekulalarning atomlari orasidagi. Shuning uchun molekulada qancha atom bo'lsa, shuncha ko'p bo'ladi
moddaning qaynash nuqtasi, shuning uchun gomologik qatorda harorat
Qaynoq bir tekis ko'tarilishi kerak. Agar molekulalar orasidagi o'zaro ta'sir kuchlarini solishtirsak
n-pentan va neopentan bo'lsa, bu kuchlar molekula uchun kattaroq ekanligi aniq.
uglerod atomlarining oddiy zanjiri tarvaqaylab ketganlarga qaraganda, chunki molekulada
neopentanning markaziy atomi odatda o'zaro ta'sirdan chiqariladi.
Moddaning erish nuqtasiga ta'sir qiluvchi asosiy omil zichlikdir
molekulalarning kristall panjaraga o'ralishi. Molekula qanchalik nosimmetrik bo'lsa, shunchalik nosimmetrik bo'ladi
uning kristall ichida qadoqlanishi qanchalik zich bo'lsa va erish nuqtasi shunchalik yuqori bo'ladi (da n
Pentan -132 ° C, neopentan -20 ° C)
2.1 ALKENLAR (etilen uglevodorodlari, olefinlar)
Uglevodorodlar, ularning molekulasida oddiy Q-bog'lardan tashqari uglerod - uglerod va
uglerod - vodorod uglerod-uglerod mavjud
Ulanishlar chaqiriladi
cheksiz. Chunki ta'lim
bog'lanish rasmiy ravishda molekula tomonidan ikkita vodorod atomining yo'qolishiga tengdir
to'yinmagan uglevodorodlar mavjud 2p nisbatan kamroq vodorod atomlari mavjud
chegara, bu erda n - son
C6H14 C6H12C6H10C6H8C6H6
A'zolari bir-biridan (2H)n ga farq qiladigan qator deyiladi
izologik qator. Shunday qilib, yuqoridagi diagrammada izologlar
geksan, geksen, geksadien, geksin, geksatrien va benzol.
Bittasini o'z ichiga olgan uglevodorodlar
Bog'lanish (ya'ni qo'sh bog'lanish) deyiladi alkenlar (olefinlar) yoki, tomonidan
seriyaning birinchi a'zosi - etilen, etilen uglevodorodlari. Umumiy formula
ularning gomologik qatorlari - CnH2n
2.2 Alkenlarni olish usullari
Kaustik ishqorlarning spirtli eritmalari halogen hosilalariga ta'sir qilganda:
Vodorod galoidi chiqariladi va qo'sh bog' hosil bo'ladi:
H3C-CH2-CH2BrH3C-CH=CH2+NaBr+H2O
Propil bromid Propilen
Agar galogen bilan bog'langan uglerod atomining a-pozitsiyasi bo'lsa
keyin uchinchi darajali, ikkilamchi va birlamchi vodorod atomlari afzallik bilan yo'q qilinadi
uchinchi darajali vodorod atomi, kamroq darajada ikkilamchi va hatto birlamchi
(Zaytsev qoidasi):
H3C-C-CI H3C-C + KCL + H2O
2,3-Dimetil-3-xloropentan 2,3-Dimethelpenten-2
Bu hosil bo'lgan alkenlarning termodinamik barqarorligi bilan bog'liq. Qanaqasiga
Alkenning vinil uglerod atomlarida qanchalik ko'p o'rnini bosuvchi moddalar bo'lsa, u shunchalik yuqori bo'ladi
barqarorlik.
2. Suvni olib tashlaydigan moddalarning spirtlarga ta'siri: a) o'tayotganda
300-400 ° S da alyuminiy oksidi ustidan spirtlar.
NzS-SN-SN2.-SNzNzS-SN=SN-SNz
Deut.- Butil spirti
b) sulfat kislota yumshoq sharoitda spirtlarga ta'sir qilganda reaksiya sodir bo'ladi
sulfat kislota efirlarini oraliq hosil qilish orqali:
H3C-CH-CH3 H3C-CH=CH2
izopropil spirti
Spirtli ichimliklarni kislotali muhitda og'ir sharoitlarda suvsizlantirishda xuddi shunday ta'sir kuzatiladi.
kabi har xil turdagi vodorod atomlarining ajralishida muntazamlik
vodorod galogenidini yo'q qilish.
Ushbu jarayonning birinchi bosqichi spirtning protonatsiyasi bo'lib, undan keyin
suv molekulasi ajraladi va karbokation hosil bo'ladi:
CH3-CH2-CH-CH3 + H CH3-CH2-CH-CH3 CH3-CH-CH-
CH3CH3-CH-CH-CH3CH3-CH=CH-CH3
Olingan karbokatsiya qo'shni protonning chiqishi bilan barqarorlashadi
qo'sh bog'lanish (b-eliminatsiya) hosil qilish uchun pozitsiyalar. Unda
holda eng shoxlangan alken ham hosil bo'ladi (termodinamik jihatdan ko'proq
barqaror). Bu jarayonda ko'pincha karbokatsiyalarning qayta tashkil etilishi kuzatiladi.
uglerod skeletining izomerizatsiyasi bilan bog'liq:
CH3 C-CH - CH3 CH3 C-CH-CH3
CH3 CH3 CH3 CH3
3. Zn yoki Mg ikkita bilan digalogen hosilalariga ta'sir qilganda
Qo'shni uglerod atomlarida halogen atomlari:
H3C – C CH2CIH3C - C - CH2+MgCI2
1,2-dikloro-2-metall-izobutilen
4. Asetilen uglevodorodlarini katalizatorlar orqali gidrogenlash Bilan
faoliyatning pasayishi (Fe yoki "zaharlangan", ya'ni qayta ishlangan
HCC-CH(CH3)2H2C=CH-CH(CH3)2
2.3 Alkenlarning vakillari.
Ishqorlar singari, oddiy sharoitda bir qator oddiy alkenlarning pastki gomologlari -
gazlar va C5 dan boshlab - past qaynaydigan suyuqliklar (jadvalga qarang).
| m.p., | T. | d4 | ||
| Formula | Ism | °S | Qaynatish, ° C | |
| Ch2=CH2 | Etilen | -169 | -104 | 0,5660 (-102°C da) |
| CH3CH=CH3 | Propilen | -185 | -47 | 0,6090 (-47"C da) |
| CH3CHZCH=CH2 CH3-CH=CH-CHZ | (cis) Buten-1 | -130 | -5 | 0,6696 (-5°C da) 0,6352 (O°C da) |
| -139 | +4 | |||
(cis) | ||||
| SNz-SN=SN-SNz | (trans)-Butep-2 | -105 | +1 | 0,6361 (0°C da) |
(trans) | ||||
| (CH3)3C=CH2 | Ieobutilen | -140 | -7 | 0,6407 (0 ° C da) |
Barcha alkenlar, xuddi alkanlar kabi, suvda deyarli erimaydi va yaxshi eriydi
boshqa organik erituvchilarda, metil spirti bundan mustasno; Hammasi
ularning zichligi suvga qaraganda pastroq.
3.1 ALKINLAR (atsetilen uglevodorodlari)
Alkinlar uglevodorodlar bo'lib, Q-bog'lardan tashqari ikkitasini ham o'z ichiga oladi
Ulanishlar (uchlik
bog'lanish) bir juft uglerod atomida. Gomologik qatorning umumiy formulasi
asetilen uglevodorodlari SnN2n-2 birining hosil bo'lishi
Bog'lanish rasmiy ravishda ikkita vodorod atomining yo'qolishiga tengdir.
Asetilen C2H2 - I eng oddiy ekanligi turli fizik usullar bilan isbotlangan
alkinlarning gomologik qatorining vakili - chiziqli molekulaga ega,
bunda uglerod-uglerod uchli bog'lanish uzunligi 1,20 A, bog'lanish uzunligi esa
uglerod-vodorod 1,06 A.
Asetilendagi C-H bog'lari hosil bo'lgan Q-bog'lar qatoriga kiradi
vodorod orbitalining gibridlangan orbital bilan qoplanishi sp- orbital
uglerod; molekulada bitta uglerod-uglerod a-bog'i mavjud (hosil bo'ladi
ikkita duragayning bir-birining ustiga chiqishi sp-orbi- uglerodli ko'targichlar) va ikkita
uglerod-uglerod
Bog'lanishlar ikkita o'zaro perpendikulyar "sof" juftlarning bir-biriga yopishishi natijasidir.
p-orbitallar (R
qo'shni uglerod atomlari. Ushbu modelga asoslangan asetilendagi burchaklarni bog'lash
180 ° ga teng va molekula chiziqli konformatsiyaga ega, bu esa imkonsiz qiladi
cis-trans izomeriyasi uch tomonlama bog'lanishda.
3.2 Alkinlarni olish usullari.
Asetilen uglevodorodlarini olishning eng keng tarqalgan usuli hisoblanadi
ishqorlarning spirtli eritmasining to'yingan digalogen hosilalariga ta'siri
atomlarning vicinal (a) yoki geminal (b) joylashuviga ega uglevodorodlar
halogen
a) CH2Br –CH2Br -> SNSN + 2NVg
b) CH3-CH2-CHCl2 -> SNz-SN+2ISl
CH3-CH2-CCl2-CH3 -> SNz-S S-SNz + 2NS1
Vicinal digalogen hosilalari odatda qo'shilishi bilan tayyorlanadi
galogenlar etilen uglevodorodlarga, keyin reaksiya (a) deb hisoblash mumkin
etilen uglevodorodlarini asetilen uglevodorodlariga aylantirish reaksiyasi.
Geminal digalogen hosilalari (bir uglerod atomidagi ikkala halogen atomi)
ketonlar yoki aldegidlarning hosilalari va shuning uchun yordami bilan
reaktsiyalar (b) karbonil birikmalaridan alkinlarga o'tishni amalga oshirishi mumkin.
Vodorod galogenidlarini yo'q qilishda allaqachon ma'lum bo'lgan Zaitsev qoidasi qo'llaniladi, bu
vodorod kichikroq miqdorni o'z ichiga olgan uglerod atomidan ajralib chiqadi
vodorod atomlari.
Asetilen to'g'ridan-to'g'ri yuqori haroratli yorilishdan olinishi mumkin
(termal yoki elektrotermik) metan yoki undan murakkab
uglevodorodlar:
2SN4N-SS-N + ZN2
3.3 Alkinlarning vakillari.
Alkanlar va alkenlar singari, oddiy alkinlarning gomologik qatorining quyi a'zolari
sharoitlar - gazsimon moddalar. Jadval ma'lumotlari 22 asosiy ekanligini ko'rsatadi
ko'rib chiqilayotgan sinflarga kiruvchi uglevodorodlarning fizik-kimyoviy xususiyatlari kam
bir-biridan farq qiladi (jadvalga qarang).
| Formula | Ism | T. pl., °C | Qaynatish harorati, °C | D4 |
HCC- CH2CH3 CH3CCCH3 | Asetilen propin | (vozg, -23) 9 | 0,6200 (-84 ° C da) 0,6785 (-27 ° C da) 0,669b (-10 ° C da) 0,6880 (25 ° C da) | |
4. ALKANLAR, ALKINLAR, ALKENLARNING QO'LLANISHI
Alkenlar alkanlar, asetilen va aromatik uglevodorodlar bilan birga
og'ir sanoat uchun asosiy xom ashyo manbalaridan biri hisoblanadi
(katta miqyosda) organik sintez.
Etilen polietilenga qayta ishlash uchun juda katta miqdorda ishlatiladi va
etil spirti, u etilen glikolga qayta ishlanadi va ishlatiladi
meva pishishini tezlashtirish uchun issiqxonalar.
Propilen polipropilen, aseton va izopropil spirtiga qayta ishlanadi.
Asetilen sanoatda juda muhim rol o'ynaydi. Uning dunyosi
ishlab chiqarish bir necha million tonnaga etadi. Katta miqdor
asetilen metalllarni payvandlashda, kuyganda ishlatiladi
kislorodda harorat 2800 ° S ga etadi. Bu sezilarli darajada yuqori
kislorodda vodorodning yonishidan ko'ra harorat, yonish haqida gapirmasa ham bo'ladi
metan Buning sababi CO2 ning issiqlik sig'imi bilan solishtirganda sezilarli darajada pastroqdir
H2O, alkanlarning yonishi paytida alkinlarga qaraganda ko'proq hosil bo'ladi:
2SzN6 + 7O2 -> 4SO2 + 6N2O
2C2H2 + 5O2 -> 4SO2 + 3N2O
Karbiddan olingan asetilenning yoqimsiz hidi PH3 aralashmalari bilan bog'liq
va AsH3, sof asetilen barcha quyi uglevodorodlar (benzin) kabi hidlanadi.
Asetilen va uning havo bilan aralashmalari juda portlovchi; asetilen saqlanadi va
singdiruvchi aseton eritmalari shaklida silindrlarda tashiladi
gözenekli materiallar.
NEFT VA UNNI QAYTA QILISH
Yog 'tarkibi. To'yingan uglevodorodlarning asosiy tabiiy manbai
neft hisoblanadi. Yog'larning tarkibi sohaga qarab o'zgaradi,
ammo oddiy distillash paytida barcha moylar odatda quyidagi fraktsiyalarga bo'linadi:
gaz fraktsiyasi, benzin, samolyot yoqilg'isi, kerosin, dizel yoqilg'isi,
kerosin, moyli smola.
Gaz fraktsiyasi(qaynoq nuqtasi 40◦C gacha) normal va o'z ichiga oladi
S ga qadar shoxlangan alkanlar, asosan propan va butanlar. dan tabiiy gaz
gaz konlari asosan metan va etandan iborat.
Aviatsiya benzini(bp 40-180 °C) uglevodorodlarni o'z ichiga oladi
C6 - C10 Benzinda 100 dan ortiq individual birikmalar topilgan,
Bularga toʻgʻri va shoxlangan alkanlar, sikloalkanlar va
alkilbenzollar (arenlar).
Reaktiv yoqilg'i(bp 150-280 ° S).
Traktor kerosini(t, qaynash harorati 110-300 ° C) tarkibida C7-C14 uglevodorodlar mavjud.
Dizel yoqilg'isi(bp. 200-330 ° C), shu jumladan
uglevodorodlar C13 - C18, katta miqyosda yorilishga, burilishlarga duchor bo'ladi
molekulyar og'irligi past bo'lgan alkanlarga (va alkenlarga) aylanadi (pastga qarang).
Yog 'moylari(bp 340-400°C) tarkibida C18 - C25 uglevodorodlar mavjud.
Neft parafin(bp 320-500 °C), tarkibida uglevodorodlar mavjud
C26-C38, undan vazelin ajratiladi. Distillashdan keyingi qoldiq odatda deyiladi
asfalt yoki smola.
Turli toifadagi uglevodorodlardan tashqari, neft tarkibida kislorod,
oltingugurt va azot o'z ichiga olgan moddalar; ba'zan ularning umumiy mazmuniga etadi
bir necha foizgacha.
Hozirgi vaqtda eng mashhur nazariya organik nazariyadir.
o'simliklar va hayvonlarning o'zgarishi mahsuloti sifatida neftning kelib chiqishi
qoldiqlari Buni neft namunalarida qoldiqlar topilganligi tasdiqlaydi
porfirinlar, o'simlik va hayvonlarning steroidlari va deb ataladiganlar
"Kimofossillar" - plankton tarkibidagi turli xil bo'laklar.
Garchi neft eng qimmatli tabiiy manba ekanligi umumiy qabul qilingan bo'lsa-da
kimyoviy xom ashyo, hali ham neft va neft mahsulotlarining asosiy miqdori
ichki yonuv dvigatellari (benzin), dizel dvigatellari va reaktiv dvigatellarda kuyishlar
dvigatellar (kerosin).
Dvigatel yoqilg'isi. Oktan soni. Turli xil kelib chiqadigan benzinlar
ichki yonuv dvigatellarida boshqacha yo'l tutish.
Kichik o'lchamlar bilan dvigatel quvvatini maksimal darajada oshirishga intilish va
massa, ular silindrdagi yonuvchi aralashmaning siqilish darajasini oshirishga harakat qilishadi. Biroq, ichida
Majburiy yoqish bilan ishlaydigan yuqori tezlikda ishlaydigan to'rt taktli dvigatellar,
bu holda, ba'zida aralashmaning muddatidan oldin yonishi sodir bo'ladi -
portlash. Bu dvigatel quvvatini pasaytiradi va eskirishni tezlashtiradi. Bu hodisa
suyuq yoqilg'ining tarkibi bilan bog'liq, chunki uglevodorodlar qachon turli tuzilishga ega
Dvigatel yoqilg'isi sifatida foydalanilganda, ular boshqacha harakat qilishadi. Eng yomoni
ko'rsatkichlar normal tuzilishdagi parafinlar uchundir.
Yuqori portlash potentsialiga ega bo'lgan yonuvchan moddalar uchun standart sifatida qabul qilingan
normal geptan. Parafinning uglerod zanjiri qanchalik shoxlangan
uglevodorod bo'lsa, uning silindrda yonishi qanchalik yaxshi bo'lsa va darajasi shunchalik yuqori bo'ladi
yonuvchan aralashmaning siqilishiga erishish mumkin. Standart motor yoqilg'isi sifatida
2, 2, 4-trimetilpentan (odatda izooktan deb ataladi) yaxshi qabul qilinadi.
taqillatishga qarshi xususiyatlar. Buning aralashmalarini turli nisbatlarda tuzish
p-heptapli oktan, ularning dvigateldagi xatti-harakatlarini sinov sub'ektining xatti-harakati bilan solishtiring
benzin sinovdan o'tkazilmoqda, keyin ular ikkinchisi borligini aytishadi oktan soni 70
nolga teng qabul qilingan).
Dvigatellar uchun yoqilg'ining portlash qarshiligini oshirish usullaridan biri
uchqunni yoqish ilova hisoblanadi taqillatishga qarshi vositalar.
Antiknock agentlari - bu benzinga (0,5% dan ko'p bo'lmagan) qo'shiladigan moddalar
antidetopatogen xususiyatlarni yaxshilash. Etarlicha ta'sirga qarshi vosita
hisoblanadi tetraetil qo'rg'oshin(TES) Pb (C2H5)4
Biroq, issiqlik elektr stansiyalarining benzini va uning yonish mahsulotlari juda zaharli hisoblanadi. Hozirda
marganets-organik birikmalarga asoslangan yangi anti-knock agentlari topildi
sikloC5H5Mn (CO)5: ular kamroq zaharli va
taqillatishga qarshi eng yaxshi xususiyatlarga ega. Bularni qo'shish
benzinning yaxshi navlari uchun taqillatishga qarshi vositalar sizga yoqilg'ini olish imkonini beradi
oktan soni 135 gacha.
Raketa va dizel dvigatellari uchun, aksincha, yoqilg'i bilan
eng past haroratga ega bo'lgan uglerod atomlarining oddiy zanjiri
yonish. Bu xususiyat qabul qilinadi
ichida baholang setan raqamlari. Uglevodorodning setan soni 100 ga teng
n-Sc,Nd4 va 0 raqami 1-metilnaftalindir.
CO+H2 dan uglevodorodlar sintezi. Mayda maydalangan nikeldan o'tish
250 ° C da uglerod oksidi (II) va vodorod aralashmasi, metan olinishi mumkin:
CO+3N2CH4+H2O
Agar bu reaksiya 100-200 atm bosim va 400 ° S gacha bo'lgan haroratda amalga oshirilsa,
Natijada, asosan, kislorod o'z ichiga olgan mahsulotlardan iborat aralashma,
ular orasida spirtli ichimliklar ustunlik qiladi; bu aralashma nomini oldi baland qavat.
Temir-kobalt katalizatorlari va 200 ° C haroratda foydalanilganda,
alkanlar aralashmasi - sintin.
nSO + (2n + 1) N2 SnN2n + 2 + H2O
Sintin va sintol keng ko'lamli organik sintez mahsulotlari va
ko'pgina kimyo sanoati uchun xom ashyo sifatida keng qo'llaniladi.
Klatratlar. Neftning sintin va benzin fraktsiyalari uglevodorodlar aralashmalaridan iborat
oddiy tuzilish va tarvaqaylab ketgan zanjirlar bilan. Yaqinda samarali
Oddiy zanjirli va tarmoqlangan organik birikmalarni ajratish usuli;
odatda deyiladi klatrat ajratish usuli. Uchun
Karbamid uglevodorodlarni ajratish uchun ishlatilgan. Karbamid kristallari
kristallar ichida tor olti burchakli bo'ladigan tarzda qurilgan
kanallar. Bu kanallarning diametri shunday
adsorbsion kuchlar tufayli faqat normal tuzilishdagi uglevodorodlar. Shuning uchun, qachon
organik birikmalar aralashmasini karbamid bilan qayta ishlash (yoki boshqa
birikmalar) oddiy uglerod atomlari zanjiriga ega bo'lgan moddalar kristallanadi
u bilan birgalikda komplekslar shaklida. Bu usul, albatta, juda katta
Kelajakda yanada samarali klatrat hosil qiluvchilar topiladi.
Uglevodorodlarning xarakterli kimyoviy xossalari: alkanlar, alkenlar, dienlar, alkinlar, aromatik uglevodorodlar
Alkanlar
Alkanlar uglevodorodlar boʻlib, molekulalarida atomlari bir bogʻ bilan bogʻlangan va $C_(n)H_(2n+2)$ umumiy formulasiga mos keladi.
Metanning gomologik qatori
Siz allaqachon bilganingizdek, gomologlar- bular tuzilishi va xossalari bo'yicha o'xshash va bir yoki bir nechta $CH_2$ guruhlari bilan farq qiluvchi moddalardir.
Toʻyingan uglevodorodlar metanning gomologik qatorini tashkil qiladi.
Izomeriya va nomenklatura
Alkanlar deb atalmish bilan tavsiflanadi strukturaviy izomeriya. Strukturaviy izomerlar uglerod skeletining tuzilishida bir-biridan farq qiladi. Ma'lumki, strukturaviy izomerlar bilan tavsiflangan eng oddiy alkan butandir:
Keling, alkanlar uchun IUPAC nomenklaturasining asoslarini batafsil ko'rib chiqaylik:
1. Asosiy sxemani tanlash.
Uglevodorod nomining shakllanishi asosiy zanjirni aniqlashdan boshlanadi - molekuladagi uglerod atomlarining eng uzun zanjiri, go'yo uning asosi.
2.
Asosiy zanjirning atomlariga raqamlar berilgan. Asosiy zanjirning atomlarini raqamlash o'rinbosar eng yaqin bo'lgan uchidan boshlanadi (A, B tuzilmalari). Agar o'rinbosarlar zanjir oxiridan teng masofada joylashgan bo'lsa, raqamlash ular ko'proq bo'lgan oxiridan boshlanadi (B tuzilmasi). Agar turli xil o'rinbosarlar zanjirning uchlaridan teng masofada joylashgan bo'lsa, raqamlash eng kattasi eng yaqin bo'lgan oxiridan boshlanadi (D tuzilmasi). Старшинство углеводородных заместителей определяется по тому, в каком порядке следует в алфавите буква, с которой начинается их название: метил (—$СН_3$), затем пропил ($—СН_2—СН_2—СН_3$), этил ($—СН_2—СН_3$ ) va hokazo.
E'tibor bering, o'rnini bosuvchining nomi qo'shimchani almashtirish orqali yasaladi -an qo‘shimchasini olmoq -il tegishli alkan nomi bilan.
3. Ismning shakllanishi.
Ismning boshida raqamlar ko'rsatilgan - o'rnini bosuvchi moddalar joylashgan uglerod atomlarining raqamlari. Agar ma'lum bir atomda bir nechta o'rinbosar bo'lsa, unda nomdagi tegishli raqam vergul bilan ajratilgan holda ikki marta takrorlanadi ($2,2-$). Raqamdan keyin o'rnini bosuvchilar soni defis bilan ko'rsatiladi ( di- ikki, uch- uch, tetra- to'rtta, penta- besh) va deputatning ismi ( metil, etil, propil). Keyin, bo'sh joy yoki defissiz, asosiy zanjirning nomi. Asosiy zanjir uglevodorod deb ataladi - metanning gomologik seriyasining a'zosi ( metan, etan, propan va boshqalar.).

Strukturaviy formulalari yuqorida keltirilgan moddalarning nomlari quyidagicha:
— A tuzilmasi: $2$ -metilpropan;
— B tuzilmasi: $3$ -etilgeksan;
— B tuzilmasi: $2,2,4$ - trimetilpentan;
— G tuzilmasi: $2$ -metil$4$-etilgeksan.
Alkanlarning fizik va kimyoviy xossalari
Jismoniy xususiyatlar. Metanning gomologik qatorining dastlabki to'rtta vakili gazlardir. Ulardan eng oddiyi metan, rangsiz, ta'msiz va hidsiz gazdir (gazning hidi, uni sezganingizdan so'ng, siz $104 $ deb atashingiz kerak, merkaptanlarning hidi bilan aniqlanadi - metanga maxsus qo'shilgan oltingugurt saqlovchi birikmalar. maishiy va sanoat gaz moslamalari , shunda ularning yonida joylashgan odamlar hid orqali sizib chiqayotganini aniqlashlari mumkin).
$S_5N_(12)$ dan $S_(15)N_(32)$ gacha tarkibidagi uglevodorodlar suyuqlikdir; og'irroq uglevodorodlar qattiq moddalardir.
Alkanlarning qaynash va erish nuqtalari uglerod zanjiri uzunligi ortishi bilan asta-sekin ortadi. Barcha uglevodorodlar suvda yomon eriydi, suyuq uglevodorodlar keng tarqalgan organik erituvchilardir.
Kimyoviy xossalari.
1. Almashtirish reaksiyalari. Alkanlar uchun eng xarakterli reaktsiyalar erkin radikallarni almashtirish reaktsiyalari bo'lib, ular davomida vodorod atomi galogen atomi yoki biron bir guruh bilan almashtiriladi.
Eng xarakterli reaksiyalar tenglamalarini keltiramiz.
Galogenlash:
$CH_4+Cl_2→CH_3Cl+HCl$.
Haddan tashqari halogen bo'lsa, xlorlash barcha vodorod atomlarini xlor bilan to'liq almashtirishgacha davom etishi mumkin:
$CH_3Cl+Cl_2→HCl+(CH_2Cl_2)↙(\text"diklorometan (metilenxlorid)")$,
$CH_2Cl_2+Cl_2→HCl+(CHSl_3)↙(\text"triklorometan(xloroform)")$,
$CHCl_3+Cl_2→HCl+(CCl_4)↙(\text"uglerod tetraxlorid(uglerod tetraxlorid)")$.
Hosil boʻlgan moddalar organik sintezlarda erituvchi va boshlangʻich material sifatida keng qoʻllaniladi.
2. Dehidrogenatsiya (vodorodni yo'q qilish). Alkanlarni katalizator ($Pt, Ni, Al_2O_3, Cr_2O_3$) orqali yuqori haroratda ($400-600°C$) oʻtkazganda vodorod molekulasi ajralib chiqadi va alken hosil boʻladi:
$CH_3—CH_3→CH_2=CH_2+H_2$
3. Uglerod zanjirining buzilishi bilan kechadigan reaksiyalar. Barcha to'yingan uglevodorodlar yonmoqdalar karbonat angidrid va suv hosil bo'lishi bilan. Muayyan nisbatlarda havo bilan aralashtirilgan gazsimon uglevodorodlar portlashi mumkin. To'yingan uglevodorodlarning yonishi erkin radikal ekzotermik reaktsiya bo'lib, juda ko'p katta ahamiyatga ega alkanlarni yoqilg'i sifatida ishlatganda:
$SN_4+2O_2→SO_2+2N_2O+880 kJ.$
IN umumiy ko'rinish Alkanlarning yonish reaksiyasini quyidagicha yozish mumkin:
$C_(n)H_(2n+2)+((3n+1)/(2))O_2→nCO_2+(n+1)H_2O$
Uglevodorodlarning termik bo‘linishi:
$C_(n)H_(2n+2)(→)↖(400-500°C)C_(n-k)H_(2(n-k)+2)+C_(k)H_(2k)$
Jarayon erkin radikal mexanizm orqali sodir bo'ladi. Haroratning oshishi uglerod-uglerod aloqasining gomolitik ajralishiga va erkin radikallarning paydo bo'lishiga olib keladi:
$R—CH_2CH_2:CH_2—R→R—CH_2CH_2·+·CH_2—R$.
Bu radikallar bir-biri bilan oʻzaro taʼsirlashib, vodorod atomini almashtirib, alkan molekulasi va alken molekulasini hosil qiladi:
$R—CH_2CH_2·+·CH_2—R→R—CH=CH_2+CH_3—R$.
Uglevodorod krekingining sanoat jarayoni asosida termal parchalanish reaksiyalari yotadi. Bu jarayon neftni qayta ishlashning eng muhim bosqichidir.
Metan $1000°C$ haroratgacha qizdirilganda metan pirolizi boshlanadi - oddiy moddalarga parchalanadi:
$CH_4(→)↖(1000°C)C+2H_2$
$1500°C$ haroratgacha qizdirilganda asetilen hosil boʻlishi mumkin:
$2CH_4(→)↖(1500°C)CH=CH+3H_2$
4. Izomerizatsiya. Chiziqli uglevodorodlar izomerizatsiya katalizatori (alyuminiy xlorid) bilan qizdirilganda, tarvaqaylab ketgan uglerod skeleti bo'lgan moddalar hosil bo'ladi:
5. Aromatizatsiya. Zanjirda olti yoki undan ortiq uglerod atomiga ega alkanlar katalizator ishtirokida sikllanadi va benzol va uning hosilalarini hosil qiladi:

Alkanlarning erkin radikal reaksiyaga kirishishining sababi nima? Alkan molekulalaridagi barcha uglerod atomlari $sp^3$ gibridlanish holatidadir. Bu moddalarning molekulalari kovalent qutbsiz $C-C$ (uglerod-uglerod) va zaif qutbli $C-H$ (uglerod-vodorod) aloqalari yordamida qurilgan. Ular elektron zichligi oshgan yoki kamaygan joylarni yoki oson polarizatsiyalanadigan bog'lanishlarni o'z ichiga olmaydi, ya'ni. tashqi omillar (ionlarning elektrostatik maydonlari) ta'sirida elektron zichligi o'zgarishi mumkin bo'lgan bunday bog'lanishlar. Binobarin, alkanlar zaryadlangan zarralar bilan reaksiyaga kirishmaydi, chunki alkan molekulalaridagi aloqalar geterolitik mexanizm bilan uzilmaydi.
Alkenlar
To'yinmaganlarga molekulalaridagi uglerod atomlari o'rtasida bir nechta bog'langan uglevodorodlar kiradi. Cheksiz alkenlar, alkadienlar (polienlar), alkinlar. Tarkibida halqada qoʻsh bogʻ boʻlgan siklik uglevodorodlar (sikloalkenlar), shuningdek, halqada oz sonli uglerod atomlari (uch yoki toʻrt atom) boʻlgan sikloalkanlar ham toʻyinmagan xarakterga ega. To'yinmaganlik xususiyati bu moddalarning to'yingan yoki to'yingan uglevodorodlar - alkanlar hosil bo'lishi bilan qo'shilish reaktsiyalariga, birinchi navbatda vodorodga kirish qobiliyati bilan bog'liq.
Alkenlar molekulada bitta bog'lardan tashqari, uglerod atomlari orasidagi bitta qo'sh bog'ni o'z ichiga olgan va $C_(n)H_(2n)$ umumiy formulasiga mos keladigan asiklik uglevodorodlardir.
Uning ikkinchi nomi olefinlar- alkenlar to'yinmagan yog 'kislotalari (oleik, linoleik) bilan o'xshashlik yo'li bilan olingan, ularning qoldiqlari suyuq yog'lar - yog'lar (lot. oleum- moy).
Etenning gomologik qatori
Tarmoqlanmagan alkenlar etenning (etilen) gomologik qatorini hosil qiladi:
$S_2N_4$ - eten, $S_3N_6$ - propen, $S_4N_8$ - buten, $S_5N_(10)$ - penten, $S_6N_(12)$ - geksen va boshqalar.
Izomeriya va nomenklatura
Alkenlar ham alkanlar kabi tuzilish izomeriyasi bilan ajralib turadi. Strukturaviy izomerlar uglerod skeletining tuzilishida bir-biridan farq qiladi. Strukturaviy izomerlar bilan tavsiflangan eng oddiy alken butendir:

Strukturaviy izomeriyaning alohida turi qo'sh bog'lanish pozitsiyasining izomeriyasidir:
$CH_3—(CH_2)↙(buten-1)—CH=CH_2$ $CH_3—(CH=CH)↙(buten-2)—CH_3$
Yagona uglerod-uglerod aloqasi atrofida uglerod atomlarining deyarli erkin aylanishi mumkin, shuning uchun alkan molekulalari turli xil shakllarga ega bo'lishi mumkin. Qo'sh bog' atrofida aylanish mumkin emas, bu alkenlarda izomeriyaning boshqa turi - geometrik yoki cis-trans izomeriyaning paydo bo'lishiga olib keladi.

Cis- izomerlari bilan farqlanadi trans - izomerlar fazoviy tartibga solish$p$ bog'lanish tekisligiga nisbatan molekula bo'laklari (bu holda metil guruhlari) va, demak, xossalari.
Alkenlar sikloalkanlarga izomerdir (sinflararo izomeriya), masalan:

Alkenlar uchun IUPAC nomenklaturasi alkanlarnikiga o'xshaydi.
1. Asosiy sxemani tanlash.
Uglevodorodni nomlash asosiy zanjirni - molekuladagi uglerod atomlarining eng uzun zanjirini aniqlashdan boshlanadi. Alkenlar bo'lsa, asosiy zanjirda qo'sh bog' bo'lishi kerak.
2. Asosiy zanjir atomlarini raqamlash.
Asosiy zanjirning atomlarini raqamlash qo'sh bog'lanish eng yaqin bo'lgan uchidan boshlanadi. Masalan, to'g'ri ulanish nomi:

Kutilganidek, $2$-metilheksen-$4$ emas, balki $5$-metilheksen-$2$.
Agar qo'sh bog'lanishning pozitsiyasi zanjirdagi atomlarning raqamlanishining boshlanishini aniqlay olmasa, u to'yingan uglevodorodlar kabi o'rinbosarlarning pozitsiyasi bilan aniqlanadi.

3. Ismning shakllanishi.
Alkenlarning nomlari ham alkanlarning nomlari kabi shakllanadi. Ismning oxirida qo'sh bog'lanish boshlanadigan uglerod atomining raqamini va birikmaning alkenlar sinfiga tegishli ekanligini ko'rsatadigan qo'shimchani ko'rsating - -en.
Masalan:

Alkenlarning fizik va kimyoviy xossalari
Jismoniy xususiyatlar. Alkenlarning gomologik qatorining dastlabki uchta vakili gazlardir; $S_5N_(10)$ - $S_(16)N_(32)$ tarkibidagi moddalar - suyuqliklar; Yuqori alkenlar qattiq moddalardir.
Aralashmalarning molekulyar og'irligi oshishi bilan qaynash va erish nuqtalari tabiiy ravishda ortadi.
Kimyoviy xossalari.
Qo'shilish reaktsiyalari. Shuni eslatib o'tamiz o'ziga xos xususiyat vakillari to'yinmagan uglevodorodlar— alkenlar — qoʻshilish reaksiyalariga kirishish qobiliyati. Ushbu reaktsiyalarning aksariyati mexanizmga muvofiq davom etadi
1. Alkenlarning gidrogenlanishi. Alkenlar gidrogenlash katalizatorlari, metallar - platina, palladiy, nikel ishtirokida vodorod qo'shishga qodir:
$CH_3—CH_2—CH=CH_2+H_2(→)↖(Pt)CH_3—CH_2—CH_2—CH_3$.
Bu reaktsiya atmosfera va ko'tarilgan bosimda sodir bo'ladi va yuqori haroratni talab qilmaydi, chunki ekzotermikdir. Harorat ko'tarilganda, xuddi shu katalizatorlar teskari reaktsiyaga olib kelishi mumkin - dehidrogenatsiya.
2. Galogenlash (galogenlarni qo'shish). Alkenning bromli suv yoki bromning organik erituvchidagi eritmasi ($CCl_4$) bilan oʻzaro taʼsiri alkenga halogen molekulasi qoʻshilishi va digalogen alkanlarning hosil boʻlishi natijasida bu eritmalarning tez rangsizlanishiga olib keladi:
$CH_2=CH_2+Br_2→CH_2Br—CH_2Br$.
3.
$CH_3-(CH)↙(propen)=CH_2+HBr→CH_3-(CHBr)↙(2-bromopropen)-CH_3$
Bu reaktsiya bo'ysunadi Markovnikov qoidasi:
Alkenga vodorod halidi qo'shilsa, vodorod ko'proq vodorodlangan uglerod atomiga qo'shiladi, ya'ni. vodorod atomlari ko'p bo'lgan atomga, galogen esa kamroq vodorodlanganga.
Alkenlarning hidratsiyasi spirtlar hosil bo'lishiga olib keladi. Masalan, etenga suv qo'shilishi quyidagilardan biri asosida yotadi sanoat usullari etil spirtini olish:
$(CH_2)↙(eten)=CH_2+H_2O(→)↖(t,H_3PO_4)CH_3-(CH_2OH)↙(etanol)$
E'tibor bering, birlamchi spirt (birlamchi uglerodda gidrokso guruhi bilan) faqat eten gidratlanganda hosil bo'ladi. Propen yoki boshqa alkenlar gidratlanganda ikkilamchi spirtlar hosil bo'ladi.

Bu reaktsiya ham Markovnikov qoidasiga muvofiq davom etadi - vodorod kationi ko'proq vodorodlangan uglerod atomiga, gidroksoguruh esa kamroq vodorodlangan atomga biriktiriladi.
5. Polimerizatsiya. Qo'shishning alohida holati alkenlarning polimerizatsiya reaktsiyasidir:
$nCH_2(=)↙(eten)CH_2(→)↖(UV nuri, R)(...(-CH_2-CH_2-)↙(polietilen)...)_n$
Ushbu qo'shilish reaktsiyasi erkin radikal mexanizm orqali sodir bo'ladi.
6. Oksidlanish reaktsiyasi.
Har qanday kabi organik birikmalar, alkenlar kislorodda yonib $SO_2$ va $N_2O$ hosil qiladi:
$SN_2=SN_2+3O_2→2SO_2+2N_2O$.
Umuman:
$C_(n)H_(2n)+(3n)/(2)O_2→nCO_2+nH_2O$
Eritmalarda oksidlanishga chidamli alkanlardan farqli ravishda alkenlar kaliy permanganat eritmalari bilan oson oksidlanadi. Neytral yoki gidroksidi eritmalarda alkenlar diollarga (dihidrik spirtlar) oksidlanadi va oksidlanishdan oldin qo'sh aloqa mavjud bo'lgan atomlarga gidroksil guruhlari qo'shiladi:

Alkadienlar (dien uglevodorodlari)
Alkadienlar molekulada bitta bog'lardan tashqari, uglerod atomlari orasidagi ikkita qo'sh bog'lanishni o'z ichiga olgan va $C_(n)H_(2n-2)$ umumiy formulasiga mos keladigan asiklik uglevodorodlardir.
ga qarab nisbiy pozitsiya qo'sh bog'lanish, dienlarning uch turi mavjud:
- alkadienlar bilan jamlangan qo'sh bog'lanishlarni tartibga solish:
- alkadienlar bilan konjugatsiyalangan ikki tomonlama aloqalar;
$CH_2=CH—CH=CH_2$;
- alkadienlar bilan izolyatsiya qilingan ikki tomonlama aloqalar
$CH_2=CH—CH_2—CH=CH_2$.
Ushbu uch turdagi alkadienlar tuzilishi va xossalari bo'yicha bir-biridan sezilarli darajada farq qiladi. Toʻplangan bogʻlarga ega alkadienlardagi markaziy uglerod atomi (ikki qoʻsh bogʻ hosil qiluvchi atom) $sp$-gibridlanish holatida boʻladi. U bir to g ri chiziqda yotgan va qarama-qarshi yo nalishga yo naltirilgan ikkita $s$-bog lanishni va perpendikulyar tekislikda yotgan ikkita $p$-bog ni hosil qiladi. $p$-bog'lar har bir uglerod atomining gibridlanmagan p-orbitallari hisobiga hosil bo'ladi. Izolyatsiya qilingan qo'sh bog'li alkadienlarning xossalari juda o'ziga xosdir, chunki konjugat $p$-bog'lar bir-biriga sezilarli ta'sir ko'rsatadi.
Konjugatsiyalangan $p$-bog'larni hosil qiluvchi p-orbitallar amalda yagona tizimni tashkil qiladi (u $p$-tizim deb ataladi), chunki qo'shni $p$-bog'larning p-orbitallari qisman ustma-ust tushadi.
Izomeriya va nomenklatura
Alkadienlar ham strukturaviy izomeriya, ham sis-, trans-izomeriya bilan tavsiflanadi.
Strukturaviy izomeriya.
— uglerod skeleti izomeriyasi:

— Ko'p bog'lanish pozitsiyasining izomeriyasi:
$(CH_2=CH—CH=CH_2)↙(butadien-1,3)$ $(CH_2=C=CH—CH_3)↙(butadien-1,2)$
Cis-, trans- izomeriya (fazoviy va geometrik)
Masalan:
Alkadienlar alkinlar va sikloalkenlar sinflarining izomer birikmalaridir.
Alkadien nomini hosil qilishda qo'sh bog'lanish raqamlari ko'rsatiladi. Asosiy zanjirda ikkita ko'p bog'lanish bo'lishi kerak.
Masalan:

Alkadienlarning fizik va kimyoviy xossalari
Jismoniy xususiyatlar.
Oddiy sharoitda propandien-1,2, butadien-1,3 gazlar, 2-metilbutadien-1,3 uchuvchi suyuqlikdir. Izolyatsiya qilingan qoʻsh bogʻli alkadienlar (ulardan eng oddiyi pentadien-1,4) suyuqlikdir. Yuqori dienlar qattiq moddalardir.
Kimyoviy xossalari.
Izolyatsiya qilingan qoʻsh bogʻli alkadienlarning kimyoviy xossalari alkenlarning xossalaridan unchalik farq qilmaydi. Konjugatsiyalangan bog'langan alkadienlar o'ziga xos xususiyatlarga ega.
1. Qo'shilish reaktsiyalari. Alkadienlar vodorod, galogenlar va vodorod galogenidlarini qo'shishga qodir.
Alkadienlarni konjugatsiyalangan bog'lanishlarga qo'shishning o'ziga xos xususiyati molekulalarni 1 va 2 pozitsiyalarda ham, 1 va 4 pozitsiyalarda ham qo'shish qobiliyatidir.

Mahsulotlarning nisbati mos keladigan reaktsiyalarni o'tkazish shartlari va usuliga bog'liq.
2.Polimerlanish reaktsiyasi. Eng muhim mulk dienlar - kationlar yoki erkin radikallar ta'sirida polimerlanish qobiliyati. Ushbu birikmalarning polimerizatsiyasi sintetik kauchuklarning asosidir:
$nCH_2=(CH—CH=CH_2)↙(butadien-1,3)→((... —CH_2—CH=CH—CH_2— ...)_n)↙(\text"sintetik butadien kauchuk")$ .
Konjugatsiyalangan dienlarning polimerizatsiyasi 1,4-qo'shimcha sifatida davom etadi.
Bunday holda, qo'sh bog'lanish birlikda markaziy bo'lib chiqadi va elementar birlik, o'z navbatida, ikkalasini ham qabul qilishi mumkin. cis-, shunday trans - konfiguratsiya

Alkinlar
Alkinlar molekulada bitta bog'lardan tashqari, uglerod atomlari orasidagi bir uchlik bog'ni o'z ichiga olgan va $C_(n)H_(2n-2)$ umumiy formulasiga mos keladigan asiklik uglevodorodlardir.
Etinning gomologik qatori
To'g'ri zanjirli alkinlar etin (atsetilen) ning gomologik qatorini hosil qiladi:
$S_2N_2$ - etin, $S_3N_4$ - propin, $S_4N_6$ - butin, $S_5N_8$ - pentin, $S_6N_(10)$ - geksin va boshqalar.
Izomeriya va nomenklatura
Alkinlar, alkenlar singari, strukturaviy izomeriya bilan tavsiflanadi: uglerod skeletining izomeriyasi va ko'p bog'lanish pozitsiyasining izomeriyasi. Alkin sinfining ko'p bog'lanish holatining strukturaviy izomerlari bilan tavsiflangan eng oddiy alkin butindir:
$SN_3—(SN_2)↙(butin-1)—S≡SN$ $SN_3—(S≡S)↙(butin-2)—SN_3$
Pentindan boshlab alkinlarda uglerod skeletining izomeriyasi mumkin:

Uch tomonlama bog'lanish uglerod zanjirining chiziqli tuzilishini qabul qilganligi sababli, geometrik ( cis-, trans-) alkinlar uchun izomeriya mumkin emas.
Ushbu sinfdagi uglevodorod molekulalarida uchlik bog'lanishning mavjudligi qo'shimcha orqali aks ettiriladi -in, va uning zanjirdagi holati uglerod atomining soni.
Masalan:

Boshqa sinflarning birikmalari alkinlarga izomerdir. Shunday qilib, kimyoviy formula$S_6N_(10)$ tarkibida geksin (alkin), geksadien (alkadien) va siklogeksen (sikloalken) mavjud:

Alkinlarning fizik va kimyoviy xossalari
Jismoniy xususiyatlar. Alkinlarning, shuningdek alkenlarning qaynash va erish nuqtalari birikmalarning molekulyar og'irligi oshishi bilan tabiiy ravishda ortadi.
Alkinlarning o'ziga xos hidi bor. Ular alkanlar va alkenlarga qaraganda suvda yaxshi eriydi.
Kimyoviy xossalari.
Qo'shilish reaktsiyalari. Alkinlar toʻyinmagan birikmalar boʻlib, qoʻshilish reaksiyalariga kirishadi. Ko'pincha reaktsiyalar elektrofil qo'shilishi.
1. Galogenlash (galogen molekulasini qo'shish). Alkin ikkita halogen molekulasini (xlor, brom) biriktira oladi:
$CH≡CH+Br_2→(CHBr=CHBr)↙(1,2-dibromoetan),$
$CHBr=CHBr+Br_2→(CHBr_2-CHBr_2)↙(1,1,2,2-tetrabrometan)$
2. Gidrogalogenlash (galogen vodorod qo'shilishi). Elektrofil mexanizm orqali sodir bo'ladigan vodorod galogenidining qo'shilish reaktsiyasi ham ikki bosqichda sodir bo'ladi va ikkala bosqichda ham Markovnikov qoidasi qondiriladi:
$CH_3-C≡CH+Br→(CH_3-CBr=CH_2)↙(2-bromopropen),$
$CH_3-CBr=CH_2+HBr→(CH_3-CHBr_2-CH_3)↙(2,2-dibromopropan)$
3. Hidratsiya (suv qo'shilishi). Ketonlar va aldegidlarning sanoat sintezi uchun suv qo'shilishi (gidratlanish) reaktsiyasi katta ahamiyatga ega. Kucherovning munosabati:
4. Alkinlarning gidrogenlanishi. Alkinlar vodorodni metall katalizatorlar ($Pt, Pd, Ni$) ishtirokida qo‘shadilar:
$R-C≡C-R+H_2(→)↖(Pt)R-CH=CH-R,$
$R-CH=CH-R+H_2(→)↖(Pt)R-CH_2-CH_2-R$
Uchlik bog'lanish ikkita reaktiv $p$ aloqani o'z ichiga olganligi sababli, alkanlar vodorodni bosqichma-bosqich qo'shadilar:
1) trimerizatsiya.
Etin faollashtirilgan ugleroddan o'tkazilganda mahsulotlar aralashmasi hosil bo'ladi, ulardan biri benzoldir:

2) dimerizatsiya.
Asetilenning trimerizatsiyasidan tashqari, uning dimerizatsiyasi ham mumkin. Bir valentli mis tuzlari ta'sirida vinil asetilen hosil bo'ladi:
$2HC≡CH→(HC≡C-CH=CH_2)↙(\text"buten-1-in-3(vinilatsetilen)")$
Ushbu modda xloropren ishlab chiqarish uchun ishlatiladi:
$HC≡C-CH=CH_2+HCl(→)↖(CaCl)H_2C=(CCl-CH)↙(xloropren)=CH_2$
polimerizatsiya natijasida xloropren kauchuk olinadi:
$nH_2C=CCl-CH=CH_2→(...-H_2C-CCl=CH-CH_2-...)_n$
Alkinlarning oksidlanishi.
Etin (atsetilen) kislorodda yonib, juda katta miqdorda issiqlik chiqaradi:
$2C_2H_2+5O_2→4CO_2+2H_2O+2600kJ$ Kislorod-atsetilen mash’alining ta’siri shu reaksiyaga asoslangan bo‘lib, uning alangasi juda yuqori haroratga ega (3000°C$ dan ortiq), bu esa undan foydalanish imkonini beradi. metallarni kesish va payvandlash.
Havoda asetilen tutunli alanga bilan yonadi, chunki uning molekulasidagi uglerod miqdori etan va eten molekulalariga qaraganda yuqori.
Alkinlar, alkenlar kabi, kaliy permanganatning kislotali eritmalarini rangini o'zgartiradi; Bunday holda, bir nechta aloqa yo'q qilinadi.
Kislorodli birikmalarni olishning asosiy usullarini tavsiflovchi reaktsiyalar
1. Galoalkanlarning gidrolizi. Siz allaqachon bilasizki, spirtlar vodorod galogenidlari bilan reaksiyaga kirishganda halokenalkanlarning hosil bo'lishi teskari reaktsiyadir. Shu sababli, spirtli ichimliklarni olish mumkinligi aniq haloalkanlarning gidrolizi- bu birikmalarning suv bilan reaksiyalari:
$R-Cl+NaOH(→)↖(H_2O)R-OH+NaCl+H_2O$
Ko'p atomli spirtlarni har bir molekulada birdan ortiq halogen atomi bo'lgan galoidalkanlarni gidrolizlash orqali olish mumkin. Masalan:
2. Alkenlarning hidratsiyasi- alken molekulasining $p$ aloqasi orqali suv qo'shilishi - sizga allaqachon tanish, masalan:
$(CH_2=CH_2)↙(eten)+H_2O(→)↖(H^(+))(C_2H_5OH)↙(etanol)$
Propenning hidratsiyasi, Markovnikov qoidasiga muvofiq, ikkilamchi spirt - propanol-2 hosil bo'lishiga olib keladi:

3. Aldegidlar va ketonlarning gidrogenlanishi. Siz allaqachon bilasizki, engil sharoitda spirtlarning oksidlanishi aldegidlar yoki ketonlarning hosil bo'lishiga olib keladi. Spirtli ichimliklarni aldegidlar va ketonlarni gidrogenlash (vodorod bilan qaytarilishi, vodorod qo'shilishi) yo'li bilan olish mumkinligi aniq:

4. Alkenlarning oksidlanishi. Yuqorida aytib o'tilganidek, glikollarni alkenlarni kaliy permanganatning suvli eritmasi bilan oksidlash orqali olish mumkin. Masalan, etilen glikol (etandiol-1,2) etilenning (eten) oksidlanishidan hosil bo'ladi:
$CH_2=CH_2+[O]+H_2O(→)↖(KMnO_4)HO-CH_2-CH_2-OH$
5. Spirtli ichimliklar ishlab chiqarishning o'ziga xos usullari. Ba'zi spirtli ichimliklar ularga xos bo'lgan usullar yordamida olinadi. Shunday qilib, metanol sanoatda vodorodning uglerod oksidi (II) (uglerod oksidi) bilan katalizator (rux oksidi) yuzasida yuqori bosim va yuqori haroratda o'zaro ta'sirida ishlab chiqariladi:
$CO+2H_2(→)↖(t,p,ZnO)CH_3-OH$
Ushbu reaktsiya uchun zarur bo'lgan aralash uglerod oksidi va vodorod sintez gazi ($CO + nH_2O$) deb ham ataladigan suv bug'ini issiq ko'mirdan o'tkazish orqali olinadi:
$C+H_2O(→)↖(t)CO+H_2-Q$
6. Glyukoza fermentatsiyasi. Etil (sharob) spirtini ishlab chiqarishning bu usuli insonga qadim zamonlardan beri ma'lum bo'lgan:
$(C_6H_(12)O_6)↙(glyukoza)(→)↖(xamirturush)2C_2H_5OH+2CO_2$
Aldegidlar va ketonlarni olish usullari
Aldegidlar va ketonlar ishlab chiqarilishi mumkin oksidlanish yoki spirtli ichimliklarni suvsizlantirish. Yana bir bor ta'kidlab o'tamizki, birlamchi spirtlarning oksidlanishi yoki suvsizlanishi aldegidlarni, ikkilamchi spirtlarni esa - ketonlarni hosil qilishi mumkin:

Kucherovning reaktsiyasi. Gidratsiya reaktsiyasi natijasida asetilen atsetaldegidni hosil qiladi va asetilen gomologlaridan ketonlar olinadi:

Isitilganda kaltsiy yoki bariy tuzlari karboksilik kislotalar keton va metall karbonat hosil qiladi:

Karboksilik kislotalarni olish usullari
Karboksilik kislotalarni birlamchi aldegid spirtlarini oksidlash orqali olish mumkin:

Aromatik karboksilik kislotalar benzol gomologlarining oksidlanishi natijasida hosil bo'ladi:

Turli xil karboksilik kislota hosilalari gidrolizlanishi natijasida ham kislotalar hosil bo'ladi. Shunday qilib, esterning gidrolizi spirt va karboksilik kislota hosil qiladi. Yuqorida aytib o'tilganidek, kislota-katalizli esterifikatsiya va gidroliz reaktsiyalari teskari bo'ladi:
Esterning gidrolizlanishi suvli eritma gidroksidi qaytarilmas tarzda davom etadi, bu holda esterdan kislota emas, balki uning tuzi hosil bo'ladi.