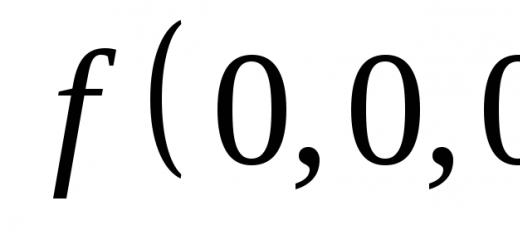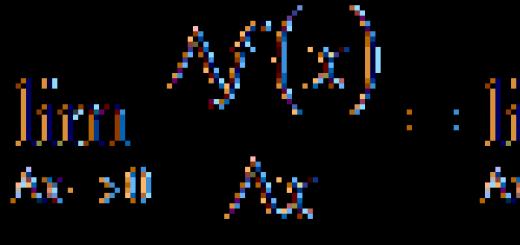MA'RUZA MAVZU: AMINLAR VA AMİNOSKOLLAR
Savollar:
umumiy xususiyatlar: tuzilishi, tasnifi, nomenklaturasi.
Qabul qilish usullari
Kimyoviy xossalari
Shaxsiy vakillar. Identifikatsiya qilish usullari.
Umumiy xarakteristikalar: tuzilishi, tasnifi, nomenklaturasi
Ominlar ammiakning hosilalari bo'lib, ularning molekulasi uglevodorod radikallari bilan almashtirilgan vodorod atomlariga ega.
Tasniflash
1- Ammiakning almashtirilgan vodorod atomlari soniga qarab aminlar farqlanadi.:
– asosiy aminokislotalarni o'z ichiga oladi (-NH 2), umumiy formula: R–NH 2,
– ikkinchi darajali imino guruhini (-NH) o'z ichiga oladi;
umumiy formula: R 1 –NH–R 2
– uchinchi darajali tarkibida azot atomi bor, umumiy formulasi: R 3 –N
To'rtlamchi azot atomiga ega bo'lgan birikmalar ham ma'lum: to'rtlamchi ammoniy gidroksid va uning tuzlari.
2- Radikalning tuzilishiga qarab aminlar ajratiladi:
- alifatik (to'yingan va to'yinmagan)
- alitsiklik
- aromatik (yadroda aminokislota yoki yon zanjirni o'z ichiga olgan)
- geterotsiklik.
Ominlarning nomenklaturasi, izomeriyasi
1. Ratsional nomenklatura bo'yicha aminlarning nomlari odatda ularning tarkibiga kiruvchi uglevodorod radikallari nomlaridan oxiri qo'shilgan holda olinadi. -amin : metilamin CH 3 – NH 2, dimetilamin CH 3 – NH – CH 3, trimetilamin (CH 3) 3 N, propilamin CH 3 CH 2 CH 2 – NH 2, fenilamin C 6 H 5 – NH 2 va boshqalar.
2. IUPAC nomenklaturasiga ko'ra, aminokislotalar funktsional guruh va uning nomi sifatida qaraladi amino asosiy zanjir nomidan oldin joylashtirilgan:
Aminlarning izomeriyasi radikallarning izomeriyasiga bog'liq.
Ominlarni ishlab chiqarish usullari
Ominlar turli usullar bilan tayyorlanishi mumkin.
A) Galoalkillarning ammiakga ta'siri
2NH 3 + CH 3 I ––® CH 3 – NH 2 + NH 4 I
B) Nitrobenzolni molekulyar vodorod bilan katalitik gidrogenlash:
C 6 H 5 NO 2 ––® C 6 H 5 NH 2 + H 2 O
nitrobenzol mushuk anilin
B) Spirtlar bilan alkillash orqali quyi aminlarni (C 1 – C 4) olish:
350 0 S, Al 2 O 3
R–OH + NH 3 –––––––––––® R–NH 2 +H 2 O
350 0 S, Al 2 O 3
2R–OH + NH 3 –––––––––––® R 2 –NH +2H 2 O
350 0 S, Al 2 O 3
3R–OH + NH 3 –––––––––––® R 3 –N + 3H 2 O
Aminlarning fizik xossalari
Metilamin, dimetilamin va trimetilamin gazlar, aminlar qatorining o'rta a'zolari suyuqliklar, undan yuqori - qattiq moddalar. O'sish bilan molekulyar og'irlik aminlar, ularning zichligi ortadi, qaynash nuqtasi ortadi va suvda eruvchanligi pasayadi. Yuqori aminlar suvda erimaydi. Pastki aminlar buzilgan baliq hidini biroz eslatuvchi yoqimsiz hidga ega. Yuqori aminlar hidsiz yoki juda engil hidga ega. Aromatik aminlar rangsiz suyuqliklar yoki qattiq moddalar, yoqimsiz hidga ega va zaharli.
Ominlarning kimyoviy xossalari
Kimyoviy xatti-harakatlar aminlar molekulada aminokislotalarning mavjudligi bilan aniqlanadi. Tashqi tomondan elektron qobiq Azot atomida 5 ta elektron mavjud. Ammiak molekulasida bo'lgani kabi, amin molekulasida ham azot atomi uchta elektronni uchta kovalent bog'lanish hosil qilish uchun sarflaydi, ikkitasi esa erkin qoladi.
Azot atomida erkin elektron juftining mavjudligi unga protonni biriktirish qobiliyatini beradi, shuning uchun aminlar ammiakga o'xshaydi, asosiy xossalarini namoyon qiladi, gidroksidlar va tuzlar hosil qiladi.
Tuz hosil bo'lishi. Kislotali aminlar tuzlarni beradi, ular kuchli asos ta'sirida yana erkin aminlarni beradi:
Ominlar kuchsiz uglerod kislotasi bilan ham tuzlar hosil qiladi:
Ammiak singari, aminlar ham protonlarning zaif dissotsiatsiyalanuvchi almashtirilgan ammoniy kationiga bog'lanishi tufayli asosiy xususiyatlarga ega:
| |
Omin suvda eritilganda, suv protonlarining bir qismi kation hosil qilish uchun sarflanadi; Shunday qilib, eritmada gidroksid ionlarining ortiqcha miqdori paydo bo'ladi va u lakmus eritmalarini bo'yash uchun etarli ishqoriy xususiyatlarga ega. Moviy rang va malinaga fenolftalein kiradi. Cheklovchi qator aminlarining asosligi juda kichik chegaralarda o'zgarib turadi va ammiakning asosligiga yaqin.
Metil guruhlarining ta'siri metil va dimetilaminning asosligini biroz oshiradi. Trimetilamin bo'lsa, metil guruhlari allaqachon hosil bo'lgan kationning hal qilinishiga to'sqinlik qiladi va uning barqarorligini, shuning uchun uning asosligini kamaytiradi.
Omin tuzlarini kompleks birikmalar deb hisoblash kerak. Ulardagi markaziy atom azot atomi bo'lib, uning koordinatsion soni to'rtta. Vodorod yoki alkil atomlari azot atomi bilan bog'langan va ichki sferada joylashgan; kislota qoldig'i tashqi sferada joylashgan.
Ominlarning asillanishi. Organik kislotalarning ba'zi hosilalari (galogen kislotalar, angidridlar va boshqalar) birlamchi va ikkilamchi aminlarga ta'sir qilganda amidlar hosil bo'ladi:
Azot kislotali ikkilamchi aminlar beradi nitrozaminlar- suvda ozgina eriydigan sarg'ish suyuqliklar:
Uchinchi darajali aminlar sovuqda suyultirilgan azot kislotasi ta'siriga chidamli (ular azot kislotasi tuzlarini hosil qiladi), og'irroq sharoitlarda radikallardan biri bo'linadi va nitrozoamin hosil bo'ladi.
Diaminlar
Diaminlar biologik jarayonlarda muhim rol o'ynaydi. Qoida tariqasida, ular suvda oson eriydi, xarakterli hidga ega va kuchli ishqoriy reaktsiya, havoning CO 2 bilan o'zaro ta'sir qiladi. Diaminlar ikki ekvivalent kislota bilan barqaror tuzlar hosil qiladi.
Etilendiamin (1,2-etandiamin) H 2 NCH 2 CH 2 NH 2. Bu eng oddiy diamin; ammiakning etilen bromidga ta'sirida olinishi mumkin:
Tetrametilendiamin (1,4-butandiamin), yoki putressin, NH 2 CH 2 CH 2 CH 2 CH 2 NH 2 va pentametilendiamin (1,5-pentandiamin) NH 2 CH 2 CH 2 CH 2 CH 2 CH 2 NH 2 yoki kadaverin. Ular oqsil moddalarining parchalanish mahsulotlarida topilgan; diaminokislotalarning dekarboksillanishi natijasida hosil bo'ladi va deyiladi ptomenlar(yunon tilidan - jasad), ular ilgari "kadavra zaharlari" hisoblangan. Hozirgi vaqtda chirigan oqsillarning zaharliligi ptomainlar tomonidan emas, balki boshqa moddalar mavjudligi bilan bog'liqligi aniqlandi.
Putresin va kadaverin ko'plab mikroorganizmlar (masalan, qoqshol va vabo qo'zg'atuvchisi) va qo'ziqorinlarning hayotiy faoliyati natijasida hosil bo'ladi; ular pishloq, ergot, chivin agari va pivo xamirturushida uchraydi.
Ba'zi diaminlar poliamid tolalari va plastmassalar ishlab chiqarish uchun xom ashyo sifatida ishlatiladi. Shunday qilib, geksa-metilendiamin NH 2 CH 2 CH 2 CH 2 CH 2 CH 2 CH 2 NH 2 dan juda qimmatli sintetik tola olindi - neylon(AQSh) yoki anid(Rossiya).
Amino spirtlari
Amino spirtlari- molekulasi tarkibida aminokislotalar va gidroksi guruhlari bo'lgan aralash funksiyali birikmalar.
Aminoetanol(etanolamin) HO-CH 2 CH 2 -NH 2 yoki kolamin.
Etanolamin qalin yog'li suyuqlik bo'lib, har jihatdan suv bilan aralashadi va kuchli ishqoriy xususiyatlarga ega. Monoetanolamin bilan bir qatorda dietanolamin va trietanolamin ham olinadi:
Cholin tarkibiga kiradi lesitinlar- yog'ga o'xshash, hayvon va o'simlik organizmlarida juda ko'p uchraydigan va ulardan ajratib olinadigan moddalar. Xolin kristalli, yuqori gigroskopik massa bo'lib, havoda oson eriydi. U kuchli ishqoriy xususiyatlarga ega va kislotalar bilan oson tuzlar hosil qiladi.
Xolin sirka angidrid bilan atsillanganda u hosil bo'ladi xolin asetat, ham chaqiriladi atsetilxolin:
 |
Asetilkolin juda muhim biokimyoviy rol o'ynaydi, chunki u asab retseptorlaridan mushaklarga qo'zg'alishni uzatuvchi vositachi (mediator).
N, masalan. CH 3 NH 2 -metilamin, CH 3 NHC 3 H 7 - metilpropilamin, (C 2 H 5) 3 N -. “ ”, “ ” va hokazo prefiksni qoʻshish orqali hosil qilingan nomlar ham qoʻllaniladi. umumiy belgiga, masalan, C 2 H 5 CH (NH 2) CH 2 CH 3 - 3-aminopentan tipidagi birikma. Ko'pchilik aromatikdir. masalan, arzimas nomlarga ega. C 6 H 5 NH 2 - , CH 3 C 6 H 4 NH 2 - va CH 3 OS 6 H 4 NH 2 - (mos ravishda "" va "" dan). Yuqori alifatik oddiy tuzilish ba'zan deyiladi radikallar nomlari bilan yog'lilar, ular sintez qilingan, masalan. , trilaurilamin.
IQ spektrlarida 3380-3400 sm -1 va 3320-3340 sm -1 hududlarda birlamchi alkilaminlar uchun eritmadagi NH bog'lanishlarining xarakterli cho'zuvchi tebranishlari kuzatiladi; asosiy aromatik moddalar uchun - 3500-3300 sm -1 mintaqada ikkita assimilyatsiya chizig'i (simmetrik va assimetrik cho'zish tebranishlari tufayli N-H aloqalari); alifatik uchun va aromatik ikkilamchi amiov - bitta chiziqli resp. mintaqada 3360-3310 sm -1 va viloyatda 3500-3300 sm -1; uchinchi darajalilar bu sohada so'rilmaydi. Kimyoviy spektrlarda siljish daqiqada 1-5 ppm. Alifatich. UV va ko'rinadigan hududlarda so'rilmaydi, aromatik. UV spektrlarida ular -o'tishlar tufayli ikkita yutilish zonasiga ega.
Isitilganda uglerod kislotalari, ularning xlor angidridlari yoki birlamchi va ikkilamchi asillanishlar bilan N-almashtirilgan amidlarni hosil qiladi, masalan: RNH 2 + CH 3 COOH -> RNHCOCH 3 + H 2 O. engil sharoitlarda reaksiyaga kirishadi, hatto osonroq -, olib borilgan. huzurida chiqish. , bu mintaqada hosil bo'lgan HC1 ni bog'laydi. Dikarbonik birikmalar bilan bo'lganda, ularning efirlari yoki hosil bo'ladi. Asillanganlar zaif asosiy xususiyatlarga ega.
HNO 2 alifatik ta'siri ostida. asosiylari N 2 va H 2 O ning chiqishi bilan, ikkilamchi - N-nitrozaminlar R 2 NNO ga aylanadi. Uchinchi darajali moddalar normal haroratda HNO 2 bilan reaksiyaga kirishmaydi. HNO 2 bilan eritma alifatik uchun ishlatiladi. . O'zaro aloqada bo'lganda asosiy aromatik HNO 2 bilan kislotali muhitda quyidagilar hosil bo'ladi: ArNH 2 + HNO 2 + HC1 -> ArCl - + 2H 2 O. Xuddi shu sharoitda ikkilamchi aromatik. N-nitrozaminlarga, uchinchi darajalilari para-nitrozo hosilalariga aylanadi. Birlamchi alitsiklik HNO 2 shakli bilan, bu ko'pincha tsiklning torayishi yoki kengayishi bilan birga keladi (qarang).
Alifatich. birlamchi va ikkilamchi o'zaro ta'sirlar. C1 2 yoki Br 2 bilan N-galogen bilan almashtirilganlarni hosil qiladi. COC1 2 bilan birlamchi RNCO yoki o'rnini bosmagan (RNH) 2 CO ni hosil qiladi, ikkilamchi - tetrasubstitusiyalangan R 2 NCONR 2. Asosiy bo'lganlar bilan muloqot qilish oson. s, azometinlarni berish (), masalan:
Birlamchi va ikkilamchi birikmalar oʻzaro taʼsirlashganda gidroksietil hosilalari hosil boʻladi, masalan: C 6 H 5 NH 2 + C1CH 2 CH 2 OH -> C 6 H 5 NHCH 2 CH 2 OH + HCl. Ko'pincha bu bir xil birikmalarning sintezi uchun. ishlatiladigan, huzurida bilan reaksiyaga baliq ovlash liniyasi. oz miqdorda H 2 O: 
NH 3 o'rniga ishlatilganda birlamchi yoki ikkilamchi, ikkilamchi va (yoki) uchinchi darajali olinadi. Bu usul () N-alkil va N,N-dialkilanilinlarni olish uchun keng tarqalgan. O'zaro ta'sirni olish uchun shunga o'xshash usul ishlab chiqilgan. NH 3 bilan. Ular NH 3 bilan juda oson reaksiyaga kirishib, hosil qiladi (qarang).
5. Alifatik amidlarning nisbati. va aromatik uglerod to'plamlari C1 2, Br 2 yoki I 2 ishqoriy eritmalari bilan birlamchi eritmalarni hosil qiladi. Bunday holda, uglerod zanjiri bir () ga qisqartiriladi.
6. Alkil va arilgalogenidlar ishtirok etgan eritmalar. Quyidagi bilan alkilgalogenidlar bilan K. (qarang) sof birlamchi alifatikalar olinadi: 
Arilgalogenidlar NH 3 bilan qiyinchilik bilan reaksiyaga kirishadi, shuning uchun sanoatda ular kuchli elektron tortib oluvchi o'rinbosarlar, ko'pincha nitro yoki sulfoguruhlar tomonidan faollashtirilgan birikmalardan foydalanadilar. Shu tarzda parchalanish olinadi.
Aminlarning tasnifi xilma-xil bo'lib, qaysi strukturaviy xususiyat asos qilib olinganligi bilan belgilanadi.
Raqamga qarab organik guruhlar azot atomi bilan bog'liq bo'lganlar ajralib turadi:
birlamchi aminlar azot RNH 2 ustidagi bitta organik guruh
ikkilamchi aminlar azot R 2 NH bo'yicha ikkita organik guruh, organik guruhlar har xil bo'lishi mumkin R "R" NH
uchinchi darajali aminlar azot R 3 N yoki R "R" R "" N ustida uchta organik guruh
Azot bilan bog'liq bo'lgan organik guruhning turiga ko'ra alifatik CH 3 N6H 5 N ajratiladi.
Molekuladagi aminokislotalar soniga ko'ra aminlar monoaminlar CH 3 NH 2, diaminlar H 2 N(CH 2) 2 NH 2, triaminlar va boshqalarga bo'linadi.
Ominlarning nomenklaturasi.
azot bilan bog'liq bo'lgan organik guruhlar nomiga "amin" so'zi qo'shiladi va guruhlar alifbo tartibida, masalan, CH 3 NHC 3 H 7 metilpropilamin, CH 3 N (C 6 H 5) 2 metildifenilamin. Qoidalar, shuningdek, nomni aminokislotalar o'rnini bosuvchi sifatida qabul qilingan uglevodorod asosida tuzishga imkon beradi. Bunday holda, uning pozitsiyasi raqamli indeks yordamida ko'rsatiladi: C 5 H 3 C 4 H 2 C 3 H(NH 2) C 2 H 2 C 1 H 3 3-aminopentan (yuqori ko'k raqamli indekslar raqamlash tartibini ko'rsatadi. C atomlari). Ba'zi aminlar uchun ahamiyatsiz (soddalashtirilgan) nomlar saqlanib qolgan: C 6 H 5 NH 2 anilin (nomenklatura qoidalariga ko'ra nomi fenilamin).
Ba'zi hollarda o'rnatilgan nomlar qo'llaniladi, ular buzilgan to'g'ri nomlar: H 2 NCH 2 CH 2 OH monoetanolamin (to'g'ri 2-aminoetanol); (OHCH 2 CH 2) 2 NH dietanolamin, to'g'ri nomi bis (2-gidroksietil) amin. Kimyoda ahamiyatsiz, buzilgan va tizimli (nomenklatura qoidalariga muvofiq tuzilgan) nomlar ko'pincha birga bo'ladi.
Aminlarning fizik xossalari.
Ominlar qatorining birinchi vakillari metilamin CH 3 NH 2, dimetilamin (CH 3) 2 NH, trimetilamin (CH 3) 3 N va etilamin C 2 H 5 NH 2 xona haroratida gazsimon, keyin sonining ortishi bilan. R dagi atomlarning soni aminlar suyuqlikka aylanadi va zanjir uzunligi R 10 C gacha ko'tarilishi bilan atomlar kristalli moddalar. Zanjir uzunligi R ortishi va azot bilan bog'liq bo'lgan organik guruhlar sonining ko'payishi (ikkilamchi va uchinchi darajali aminlarga o'tish) aminlarning suvda eruvchanligi kamayadi. Aminlarning hidi ammiak hidiga o'xshaydi, yuqori (katta R bilan) aminlar deyarli hidsizdir.
Ominlarning kimyoviy xossalari.
Aminlarning neytral molekulalarni qo'shish qobiliyati (masalan, ammoniy tuzlariga o'xshash organoammoniy tuzlari hosil bo'lgan vodorod galogenidlari HHal). noorganik kimyo. Yangi bog'lanish hosil qilish uchun azot donor vazifasini bajaradigan yolg'iz elektron juftligini ta'minlaydi. Bog` hosil bo`lishida ishtirok etuvchi H+ proton (galogen vodoroddan) akseptor (qabul qiluvchi) rolini o`ynaydi, bunday bog` donor-akseptor deb ataladi (1-rasm). Rivojlanayotgan kovalent bog'lanish NH aminda mavjud bo'lgan NH bog'lariga to'liq ekvivalentdir.
Uchinchi darajali aminlar ham HCl qo'shadi, ammo hosil bo'lgan tuz kislota eritmasida qizdirilsa, u parchalanadi va R N atomidan ajralib chiqadi:
(C 2 H 5) 3 N+ HCl ® [(C 2 H 5) 3 N H]Cl
[(C 2 H 5) 3 N H]Cl ® (C 2 H 5) 2 N H + C 2 H 5 Cl
Bu ikki reaksiyani solishtirganda, C 2 H 5 guruhi va H ning o'rin almashayotgandek tuyulishi aniq bo'ladi, natijada uchinchi darajali amindan ikkilamchi amin hosil bo'ladi.
Suvda erigan aminlar protonni xuddi shu tarzda ushlaydi, natijada eritmada OH ionlari paydo bo'ladi, bu an'anaviy ko'rsatkichlar yordamida aniqlanishi mumkin bo'lgan ishqoriy muhitning shakllanishiga mos keladi.
C2H5 N H 2 + H 2 O ® + + OH
Donor-akseptor bog'lanish hosil bo'lishi bilan aminlar nafaqat HCl, balki haloalkil RCl ni ham qo'shishi mumkin va shu bilan yangi NR bog'ini hosil qiladi, bu ham mavjud bo'lganlarga tengdir. Agar biz boshlang'ich material sifatida uchinchi darajali amin olsak, biz tetraalkilamoniy tuzini olamiz (bitta N atomida to'rtta R guruhi):
(C 2 H 5) 3 N+ C 2 H 5 I ® [(C 2 H 5) 4 N]I
Ushbu tuzlar suvda va ba'zi organik erituvchilarda eriydi va ionlarni hosil qiladi:
[(C 2 H 5) 4 N]I ® [(C 2 H 5) 4 N] + + I
Bunday eritmalar, ionli barcha eritmalar kabi, amalga oshiradi elektr toki. Tetraalkilamoniy tuzlarida halogen H2O guruhi bilan almashtirilishi mumkin:
[(CH 3) 4 N]Cl + AgOH ® [(CH 3) 4 N]OH + AgCl
Olingan tetrametilamoniy gidroksid ishqorlarga o'xshash xususiyatlarga ega kuchli asosdir.
Birlamchi va ikkilamchi aminlar azot kislotasi HON=O bilan reaksiyaga kirishadi, lekin ular turlicha reaksiyaga kirishadi. Birlamchi spirtlar birlamchi aminlardan hosil bo'ladi:
C2H5 N H2+H N O 2 ® C 2 H 5 OH + N 2 +H 2 O
Birlamchi aminlardan farqli o'laroq, ikkilamchi aminlar azot kislotasi bilan sariq, yomon eriydigan nitrozaminlarni hosil qiladi - >NN = O fragmentini o'z ichiga olgan birikmalar:
(C 2 H 5) 2 N H+H N O 2 ® (C 2 H 5) 2 N N=O + H2O
Uchinchi darajali aminlar oddiy haroratda azot kislotasi bilan reaksiyaga kirishmaydi, shuning uchun azot kislotasi birlamchi, ikkilamchi va uchinchi darajali aminlarni ajratish imkonini beruvchi reaktivdir.
Ominlar bilan kondensatsiyalanganda karboksilik kislotalar kislota amidlari C (O) N fragmenti bilan hosil bo'lgan birikmalardir
Ominlarning aldegidlar va ketonlar bilan kondensatsiyasi Shiff asoslari deb ataladigan moddalar - N=C2 fragmentini o'z ichiga olgan birikmalar hosil bo'lishiga olib keladi.
Birlamchi aminlar fosgen Cl 2 C=O bilan oʻzaro taʼsirlashganda N=C=O guruhiga ega boʻlgan birikmalar hosil boʻladi, ular izosiyanatlar deb ataladi (2D-rasm, ikkita izosiyanat guruhi bilan birikma olish).
Aromatik aminlar orasida eng mashhuri anilin (fenilamin) C 6 H 5 NH 2 dir. Uning xossalari alifatik aminlarga yaqin, ammo asosliligi unchalik aniq emas suvli eritmalar ishqoriy muhit hosil qilmaydi. Alifatik aminlar kabi kuchli mineral kislotalar bilan ammoniy tuzlarini [C 6 H 5 NH 3 ] + Cl hosil qilishi mumkin. Anilin azot kislotasi bilan reaksiyaga kirishganda (HCl ishtirokida) RN=N fragmentini o'z ichiga olgan diazo birikma hosil bo'ladi, u diazonium tuzi deb ataladigan ion tuzi shaklida olinadi (3A-rasm). Shunday qilib, azot kislotasi bilan o'zaro ta'sir alifatik aminlar bilan bir xil tarzda davom etmaydi. Anilindagi benzol halqasi reaktivlik xususiyatiga ega aromatik birikmalar (sm. AROMATIKLIK), galogenlanish jarayonida vodorod atomlari orto- Va juft-aminokislotalarning pozitsiyalari almashtiriladi, buning natijasida turli darajadagi almashinish darajasiga ega bo'lgan xloroanilinlar paydo bo'ladi (3B-rasm). Sulfat kislotaning ta'siri sulfonlanishga olib keladi juft-aminokislotaga joylashishi, sulfanilik kislota deb ataladigan hosil bo'ladi (3B-rasm).
Aminlarni tayyorlash.
Ammiak haloalkillar, masalan, RCl bilan reaksiyaga kirishganda, birlamchi, ikkilamchi va uchinchi darajali aminlar aralashmasi hosil bo'ladi. Hosil boʻlgan HCl qoʻshimcha mahsuloti aminlar bilan birikib ammoniy tuzini hosil qiladi, ammo agar ammiak koʻp boʻlsa, tuz parchalanib, jarayon toʻrtlamchi ammoniy tuzlari hosil boʻlishiga olib keladi (4A-rasm). Alifatik alkil galogenidlardan farqli o'laroq, arilgalogenidlar, masalan, C 6 H 5 Cl, ammiak bilan katta qiyinchilik bilan reaksiyaga kirishadi; sintez faqat mis o'z ichiga olgan katalizatorlar bilan mumkin. Sanoatda alifatik aminlar 300-500 ° C va 1-20 MPa bosimda spirtlarning NH 3 bilan katalitik o'zaro ta'siridan olinadi, natijada birlamchi, ikkilamchi va uchinchi darajali aminlar aralashmasi hosil bo'ladi (4B-rasm).
Aldegidlar va ketonlar chumoli kislota HCOONH 4 ning ammoniy tuzi bilan oʻzaro taʼsirlashganda birlamchi aminlar hosil boʻladi (4C-rasm), aldegid va ketonlarning birlamchi aminlar bilan reaksiyasi (chumoli kislotasi HCOOH ishtirokida) ikkilamchi aminlar hosil boʻladi (4-rasm). 4D).
Nitro birikmalar (tarkibida NO 2 guruhi) qaytarilganda birlamchi aminlarni hosil qiladi. N.N.Zinin tomonidan taklif etilgan bu usul alifatik birikmalar uchun kam qoʻllaniladi, lekin aromatik aminlar olish uchun muhim ahamiyatga ega va anilinni sanoat ishlab chiqarishiga asos boʻlgan (4D-rasm).
Ominlar alohida birikmalar sifatida kamdan-kam ishlatiladi, masalan, polietilenpoliamin [-C 2 H 4 NH-] kundalik hayotda ishlatiladi. n(savdo nomi PEPA) epoksi qatronlar uchun qattiqlashtiruvchi sifatida. Ominlarning asosiy ishlatilishi turli xillarni tayyorlashda oraliq mahsulot sifatida ishlatiladi organik moddalar. Etakchi rol anilinga tegishli bo'lib, uning asosida anilin bo'yoqlarining keng assortimenti ishlab chiqariladi va rangli "ixtisoslashuv" anilinning o'zini olish bosqichida allaqachon o'rnatilgan. Gomologlarsiz o'ta toza anilin sanoatda "ko'k uchun anilin" deb ataladi (kelajakdagi bo'yoq rangini anglatadi). "Qizil uchun anilin" tarkibida anilinga qo'shimcha ravishda aralashma bo'lishi kerak orto- Va juft-toluidin (CH 3 C 6 H 4 NH 2).
Alifatik diaminlar poliamidlarni ishlab chiqarish uchun boshlang'ich birikmalardir, masalan, neylon (2-rasm), u tolalar, polimer plyonkalar, shuningdek, mashinasozlikda komponentlar va qismlarni ishlab chiqarish uchun keng qo'llaniladi (poliamid tishli).
Alifatik diizosiyanatlardan (2-rasm) poliuretanlar olinadi, ular texnik kompleksga ega. muhim xususiyatlar: elastiklik va juda yuqori aşınma qarshilik (poliuretan poyafzal tagliklari), shuningdek, keng turdagi materiallarga yaxshi yopishish (poliuretan yopishtiruvchi) bilan birlashtirilgan yuqori quvvat. Ular ko'pikli shaklda (poliuretan ko'piklari) ham keng qo'llaniladi.
Yallig'lanishga qarshi preparatlar sulfanilamidlar sulfanilik kislota asosida sintezlanadi (3-rasm).
Diazonium tuzlari (2-rasm) fotosensitiv materiallarda nusxa ko'chirish uchun ishlatiladi, bu an'anaviy kumush galoidli fotografiyani chetlab o'tgan tasvirni olish imkonini beradi ( sm. QORA NUSHIRA OLISH).
Mixail Levitskiy
I. Amin molekulasidagi uglevodorod radikallari soniga ko'ra:
Birlamchi aminlar R-NH 2
(vodorod atomi aminokislota -NH 2 bilan almashtirilgan uglevodorodlarning hosilalari),
Ikkilamchi aminlar R-NH-R"
II. Uglevodorod radikalining tuzilishiga ko'ra:
Alifatik, masalan: C 2 H 5 -NH 2 etilamin



Yakuniy birlamchi aminlar
Umumiy formula C n H 2n+1 NH 2 (n ≥ 1); yoki C n H 2n+3 N (n ≥ 1)
Nomenklatura
Ominlarning nomlari (ayniqsa, ikkilamchi va uchinchi darajali) odatda radikal-funksional nomenklatura bo'yicha, radikallarni alifbo tartibida sanab, sinf nomi - amin qo'shib beriladi. Birlamchi aminlarning o'rnini bosuvchi nomenklaturaga ko'ra nomlari asosiy uglevodorodning nomi va amin qo'shimchasidan iborat.
CH3-NH2 metanamin (metilamin)
CH 3 -CH 2 -NH 2 etamin (etilamin)


Birlamchi aminlar ko'pincha uglevodorodlarning hosilalari deb ataladi, ularning molekulalarida bir yoki bir nechta vodorod atomlari NH 2 amino guruhlari bilan almashtiriladi. Aminoguruh o'rnini bosuvchi sifatida qabul qilinadi va uning joylashuvi nom boshida raqam bilan ko'rsatiladi. Masalan:
H 2 N-CH 2 -CH 2 -CH 2 -CH 2 -NH 2 1,4-diaminobutan.
Bu usulga muvofiq anilin (fenilamin) C 6 H 5 NH 2 aminobenzol deb ataladi.
To'yingan aminlarning gomologik qatori
CH 3 NH 2 - metilamin (birlamchi amin), (CH 3) 2 NH - dimetilamin (ikkilamchi amin), (CH 3) 3 N - trimetilamin (uchlamchi amin) va boshqalar.
Izomerizm
Strukturaviy izomeriya
C 4 H 9 NH 2 dan boshlangan uglerod skeleti:




C 3 H 7 NH 2 dan boshlangan aminokislotalarning pozitsiyalari:

Vodorod atomlarini azot bilan almashtirish darajasining o'zgarishi bilan bog'liq aminokislotalarning izomeriyasi:

Fazoviy izomeriya
C 4 H 9 NH 2 dan boshlab optik izomeriya mumkin:
Optik (oyna) izomerlar fazoviy izomerlar bo'lib, ularning molekulalari ob'ekt sifatida bir-biriga bog'langan va mos kelmaydigan oyna tasviri (chap va o'ng qo'llar kabi).

Jismoniy xususiyatlar
Eng past chegaralovchi aminlar - gazsimon moddalar; o'rtacha a'zolar gomologik qator- suyuqliklar; yuqori aminlar qattiq moddalardir. Metilamin ammiak hidiga ega, boshqa quyi aminlar seld sho'r suvi hidini eslatuvchi o'tkir yoqimsiz hidga ega.
Pastki aminlar suvda yaxshi eriydi, uglevodorod radikali ortishi bilan aminlarning eruvchanligi pasayadi. Ominlar oqsillarni o'z ichiga olgan organik qoldiqlarning parchalanishi paytida hosil bo'ladi. Inson va hayvon organizmlarida aminokislotalardan (biogen aminlar) bir qancha aminlar hosil bo'ladi.
Kimyoviy xossalari
Ominlar, ammiak kabi, asoslarning aniq xossalarini namoyon qiladi, bu esa azot atomining aminlari molekulalarida yolg'iz juft elektronga ega bo'lganligi bilan bog'liq.
1. Suv bilan o'zaro ta'siri
Ominlarning suvdagi eritmalari ishqoriy reaksiyaga ega.
2. Kislotalar bilan o'zaro ta'siri (tuzlarning hosil bo'lishi)

Ominlar ishqorlar ta'sirida tuzlaridan ajralib chiqadi:
Cl + NaOH → CH 3 CH 2 NH 2 + NaCl + H 2 O
3. Ominlarning yonishi
4CH 3 NH 2 + 9O 2 → 4CO 2 + 10H 2 O + 2N 2
4. Azot kislotasi bilan reaksiya (birlamchi aminlar bilan ikkilamchi va uchinchi darajali aminlar orasidagi farq)
HNO 2 ta'sirida birlamchi aminlar azot ajralib chiqishi bilan spirtlarga aylanadi:
C 2 H 5 NH 2 + HNO 2 → C 2 H 5 OH + N 2 + H 2 O
Qabul qilish usullari
1. Galoalkanlarning ammiak bilan o'zaro ta'siri
CH 3 Br + 2NH 3 → CH 3 NH 2 + NH 4 Br

2. Spirtlarning ammiak bilan o'zaro ta'siri
(Amalda bu reaksiyalar birlamchi, ikkilamchi, uchinchi darajali aminlar va toʻrtlamchi ammoniy asosli tuz aralashmasini hosil qiladi.)
Aminlar bizning hayotimizga mutlaqo kutilmaganda kirib keldi. Yaqin vaqtgacha bular edi zaharli moddalar, o'limga olib kelishi mumkin bo'lgan to'qnashuv. Va endi, bir yarim asr o'tgach, biz sintetik tolalar, matolar, qurilish materiallari va aminlar asosidagi bo'yoqlardan faol foydalanamiz. Yo'q, ular xavfsizroq bo'lishmadi, odamlar shunchaki ularni "o'ylash" va bo'ysundirish, o'zlari uchun ma'lum foyda olish imkoniyatiga ega bo'lishdi. Qaysi biri haqida yana gaplashamiz.
Ta'rif
Eritmalarda yoki birikmalarda anilinni sifat va miqdoriy aniqlash uchun reaksiyadan foydalaniladi, uning oxirida probirka tubiga 2,4,6-tribromoanilin ko`rinishidagi oq cho`kma tushadi.
Tabiatdagi aminlar
Ominlar tabiatning hamma joylarida vitaminlar, gormonlar va oraliq metabolik mahsulotlar shaklida mavjud bo'lib, ular hayvonlarning tanasida ham, o'simliklarda ham mavjud. Bundan tashqari, tirik organizmlarning parchalanishi suyuq holatda seld sho'rligining yoqimsiz hidini chiqaradigan o'rta aminlarni ham hosil qiladi. Adabiyotda keng tavsiflangan "kadavra zahari" aniq aminlarning o'ziga xos amberi tufayli paydo bo'ldi.
Uzoq vaqt davomida biz ko'rib chiqayotgan moddalar o'xshash hid tufayli ammiak bilan aralashib ketgan. Ammo XIX asr o'rtalarida frantsuz kimyogari Vurtz metilamin va etilaminni sintez qila oldi va yondirilganda uglevodorodlar ajralib chiqishini isbotladi. Bu aytib o'tilgan birikmalar va ammiak o'rtasidagi asosiy farq edi.
Sanoat sharoitida aminlarni ishlab chiqarish
Aminlardagi azot atomi eng past oksidlanish darajasida bo'lganligi sababli, azot o'z ichiga olgan birikmalarning qaytarilishi ularni olishning eng oddiy va eng qulay usuli hisoblanadi. Aynan shu tur arzonligi tufayli sanoat amaliyotida keng qo'llaniladi.
Birinchi usul - nitro birikmalarini kamaytirish. Anilin hosil bo'ladigan reaktsiya olim Zinin tomonidan nomlangan va birinchi marta XIX asr o'rtalarida amalga oshirilgan. Ikkinchi usul lityum alyuminiy gidrid yordamida amidlarni kamaytirishdir. Birlamchi aminlarni nitrillardan ham olish mumkin. Uchinchi variant - alkillanish reaktsiyalari, ya'ni ammiak molekulalariga alkil guruhlarini kiritish.
Aminlarni qo'llash

O'z-o'zidan, shaklda toza moddalar, aminlar kamdan kam qo'llaniladi. Noyob misollardan biri - polietilen poliamin (PEPA), uy sharoitida epoksi qatronining qattiqlashishini osonlashtiradi. Asosan birlamchi, uchinchi yoki ikkilamchi aminlar turli xil organik moddalar ishlab chiqarishda oraliq mahsulotdir. Eng mashhuri anilindir. Bu anilin bo'yoqlarining katta palitrasining asosidir. Oxirida olingan rang to'g'ridan-to'g'ri tanlangan xom ashyoga bog'liq. Sof anilin ko'k rang hosil qiladi, ammo anilin, orto- va para-toluidin aralashmasi qizil bo'ladi.
Alifatik aminlar poliamidlar, masalan, neylon va boshqalarni olish uchun kerak.Ular mashinasozlikda, shuningdek, arqonlar, gazlamalar va plyonkalar ishlab chiqarishda qo'llaniladi. Bundan tashqari, poliuretan ishlab chiqarishda alifatik diizosiyanatlar qo'llaniladi. Istisno xossalari (engilligi, mustahkamligi, elastikligi va har qanday sirtga yopishtirish qobiliyati) tufayli ular qurilishda (ko‘pik, elim) va poyabzal sanoatida (slipga qarshi taglik) talabga ega.
Tibbiyot aminlar qo'llaniladigan yana bir sohadir. Kimyo ulardan sulfanilamid guruhidan antibiotiklarni sintez qilishga yordam beradi, ular ikkinchi darajali dorilar, ya'ni zaxira sifatida muvaffaqiyatli qo'llaniladi. Bakteriyalar muhim dorilarga qarshilik ko'rsatsa.
Inson tanasiga zararli ta'sir
Ma'lumki, aminlar juda zaharli moddalardir. Ular bilan har qanday o'zaro ta'sir sog'likka zarar etkazishi mumkin: bug'larni inhalatsiyalash, ochiq teri bilan aloqa qilish yoki birikmalarni tanaga kiritish. O'lim kislorod etishmasligidan kelib chiqadi, chunki aminlar (xususan, anilin) qondagi gemoglobin bilan bog'lanadi va uning kislorod molekulalarini ushlashiga to'sqinlik qiladi. Xavotir beruvchi alomatlar nafas qisilishi, nazolabial uchburchak va barmoq uchlarining ko'k rangi o'zgarishi, taxipnea (tez nafas olish), taxikardiya, ongni yo'qotishdir.
Agar bu moddalar tananing yalang'och joylariga tushsa, ularni oldindan spirtga namlangan paxta bilan tezda olib tashlashingiz kerak. Bu ifloslanish maydonini ko'paytirmaslik uchun iloji boricha ehtiyotkorlik bilan bajarilishi kerak. Agar zaharlanish belgilari paydo bo'lsa, albatta shifokorga murojaat qilishingiz kerak.
Alifatik aminlar asab va yurak-qon tomir tizimlari uchun zahardir. Ular jigar funktsiyasining tushkunligiga, jigar distrofiyasiga va hatto siydik pufagi saratoniga olib kelishi mumkin.