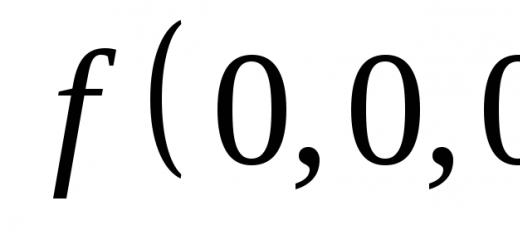Savol bo'limida anilin aminlar, tuzilishi, funktsional guruhi vakili!? muallif tomonidan berilgan Soch eng yaxshi javob Anilin (fenilamin) - organik birikma C6H5NH2 formulasi bilan, eng oddiy aromatik amin. Tarkibida NH2 amino guruhi mavjud. Bu rangsiz yog'li suyuqlik, o'ziga xos hidli, suvdan bir oz og'irroq va unda yomon eriydi, organik erituvchilarda eriydi. Havoda u tezda oksidlanadi va qizil-jigarrang rangga ega bo'ladi. Zaharli.
Anilin ham aminokislotadagi, ham aromatik halqadagi reaksiyalar bilan tavsiflanadi. Bu reaktsiyalarning xususiyatlari atomlarning o'zaro ta'siri bilan bog'liq. Bir tomondan, benzol halqasi alifatik aminlar va hatto ammiak bilan solishtirganda aminokislotalarning asosiy xususiyatlarini zaiflashtiradi. Boshqa tomondan, aminokislotalar ta'sirida benzol halqasi benzolga qaraganda almashtirish reaktsiyalarida faolroq bo'ladi. Masalan, anilin bromli suv bilan kuchli reaksiyaga kirishib, 2,4,6-tribromoanilin (oq cho`kma) hosil qiladi.
Asosiy anilin-katalitik hosil qilish usuli. nitrobenzolni vodorod bilan gaz yoki suyuq fazada kamaytirish. Gaz fazasi jarayoni nikel yoki mis o'z ichiga olgan mushukda 250-350 ° S haroratda quvurli aloqa apparatida amalga oshiriladi.
S6N5NO2 + 3H2 = C6H5NH2 + 2H2O + 443,8 kJ/mol
Anilin suvdan ajratish yo'li bilan ajratiladi va distillash orqali tozalanadi; reaktsiya suv biokimyoviy neytrallanadi. 1 t anilin olish uchun 1,35 t nitrobenzol, 800 m3 H2 va 1 kg katalizator sarflanadi.
Suyuq fazada yuqori haroratda anilin olinadi. bosim H2 (1,1 MPa gacha) va nikel yoki palladiy mushukida 160-170 ° S. bir vaqtda bilan eritmaning issiqligi tufayli suv va anilinni distillash.
Dars turi: mavjud bilimlar asosida yangi materialni o'rganish darsi
Darsning maqsadi: O'rganilayotgan "Aminlar" bo'limida talabalarning bilim va tushunchalarini umumlashtirish, kengaytirish va tizimlashtirish. "Anilin" mavzusining asosiy tushunchalariga e'tibor qarating.
Bashoratli natija: bilimlar umumlashtiriladi va maqsadga muvofiq tizimlashtiriladi.
Dars maqsadlari:
Tarbiyaviy:
O'rgangan bo'lim bo'yicha bilimingizni sinab ko'ring va uni mustahkamlang yangi material, mavzu bo'yicha bilimlarni chuqurlashtirish; o'rganilgan materialni umumlashtirish; ijodiy topshiriqlar asosida materialning o‘zlashtirilganligini tekshirish; mashqlar bajarish va masalalarni yechishda olingan bilimlarni amaliyotda qo‘llash qobiliyatini rivojlantirish;
Tarbiyaviy:
Do'stni va o'zini baholash qobiliyatini rivojlantirishga yordam berish; o'z nuqtai nazarini ifoda etish, asosli suhbat o'tkazish va tahlil asosida xulosa chiqarish qobiliyatini rivojlantirish; talabalarga o'z ishlarining natijalarini ko'rishga yordam berish; o'quvchilarda asosiy narsani ajratib ko'rsatish qobiliyatini rivojlantirish; rivojlantirish kognitiv faoliyat Va Ijodiy qobiliyatlar.
Tarbiyaviy:
Faol hayotiy pozitsiya, halollik va insoniy odob-axloqni tarbiyalash; darslar orqali o‘quvchilarda o‘ziga bo‘lgan ishonchni shakllantirish; o'quvchilarni insoniy fazilatlarning ichki qadriyati to'g'risida xulosa chiqarishga olib keladi.
Darslar davomida
I Tashkiliy va motivatsion bosqich (1 daqiqa)
Bosqichning maqsadi (kutilgan natija): talabalarni faol ishlashga undash
Bosqichning vazifalari: Talabalarni darsning yuqori sur'atiga moslashtirish
Talabalarni sinfga salomlash. Bugun darsimiz juda qizg'in bo'ladi va oldimizda bir qator vazifalar turibdi.
Lekin birinchi navbatda, D-Z Slide 2 uy vazifasini yozing
(kundalik yozuvi)
1. § 52, § 51 takrorlash.
2. 52-§, No 4-6 yozma, 1-3 og'zaki
I I Maqsadni belgilash (1,5 daqiqa)
Maqsad: To'ldirilgan "Aminlar" bo'limi bo'yicha bilimlarni umumlashtirish, dars mavzusi bo'yicha bilimlarni egallash, anilinni aromatik va alifatik aminlarning boshqa vakillari bilan taqqoslash.
Maqsadlar: 3-slayd Dars maqsadlari
Ominlarning fizik va kimyoviy xossalarini eslang; aminlarning xossalarini xarakterlovchi reaksiya tenglamalarini tuzish qobiliyatini rivojlantirishni davom ettirish; "Anilin" bo'limida kimyoviy jarayonlarning xususiyatlari bilan tanishish; kimyoviy moddalar oqimining sababini ko'rishni o'rganishni davom eting. molekula tuzilishiga qarab reaksiyalar; sinfda ishingizni baholang.
III Asosiy qism. Ma'lum faktlar asosida yangi narsalarni o'rganish
Aminlar va anilinlarning tuzilishi
Mavjud bilimlar asosida yangi materialni o'rganish
Ominlar organik hosilalar bo'lib, ularda bitta, ikkita yoki uchta atom uglevodorod qoldig'i bilan almashtiriladi.
Shunga ko'ra, aminlarning uch turi odatda ajralib turadi:
birlamchi amin metilamin
CH3CH2—NH—CH2CH3
ikkilamchi amin dietilamin
H3CH2—N—CH2CH3
uchinchi darajali amin trietilamin
Ominlar strukturaviy izomeriya bilan tavsiflanadi:
Uglerod skeletining izomeriyasi
Funktsional guruh pozitsiyasi izomeriyasi
Birlamchi, ikkilamchi va uchinchi darajali aminlar bir-biriga izomerdir (sinflararo izomeriya).
Izomeriya va amin nomenklaturasi bo'yicha trening
Yangi materialni o'rganish
Anilinning elektron tuzilishi
Aminoguruhi to'g'ridan-to'g'ri aromatik halqa bilan bog'langan aminlar aromatik aminlar deyiladi.
Bu birikmalarning eng oddiy vakili aminobenzol yoki anilindir.
Asosiy o'ziga xos xususiyat Aminlarning elektron tuzilishi - bu funktsional guruhga kiruvchi atomda yolg'iz elektron juftining mavjudligi. Bu aminlarning asoslar xossalarini namoyon etishiga olib keladi.
Ammoniy ionidagi barcha vodorod atomlarini uglevodorod radikali bilan rasmiy almashtirish mahsuloti bo'lgan ionlar mavjud.
Bu ionlar ammoniy tuzlariga o'xshash tuzlarda uchraydi. Ular to'rtlamchi tuzlar deb ataladi.
Aromatik aminlarning izomeriyasi va nomenklaturasi bo'yicha trening
Anilinning fizik xossalarini aminlarning fizik xossalari bilan taqqoslab o'rganish
Amin va anilinning fizik xossalari
Eng oddiy aminlar (metilamin, dimetilamin, trimetilamin) gazsimon moddalardir. Qolgan quyi aminlar suvda yaxshi eriydigan suyuqliklardir. Ular ammiakni eslatuvchi xarakterli hidga ega.
Birlamchi va ikkilamchi aminlar vodorod aloqalarini hosil qilish qobiliyatiga ega. Bu ularning qaynash nuqtalarining bir xil bo'lgan birikmalarga nisbatan sezilarli o'sishiga olib keladi molekulyar og'irlik, lekin vodorod aloqalarini hosil qila olmaydi.
Anilin - yog'li suyuqlik, suvda kam eriydi, 184 ° C haroratda qaynatiladi.
Rus organik kimyogari, akademik.
aromatik nitro birikmalarning qaytarilish reaksiyasini kashf etdi (1842) va anilin olindi. Ominlar turli kislotalar bilan tuzlar hosil qila oladigan asoslar ekanligi isbotlangan. Anilin shu qadar katta sanoat ahamiyatiga egaki, faqat bitta reaktsiya bilan bu olimning nomi kimyo tarixiga "oltin harflar" bilan yozilishi mumkin.
Amin va anilinning kimyoviy xossalari
Aminlarning kimyoviy xossalari asosan azot atomida yolg'iz elektron juftning mavjudligi bilan aniqlanadi.
1. Asos sifatida aminlar. Aminoguruhning azot atomi ammiak molekulasidagi azot atomi kabi yakka elektron juftligi tufayli donor-akseptor mexanizmiga ko'ra kovalent bog' hosil qilishi mumkin, donor vazifasini bajaradi. Shu munosabat bilan aminlar, ammiak kabi, vodorod kationini biriktirishga qodir, ya'ni asos sifatida ishlaydi.
Kursdan allaqachon bilganingizdek, ammiakning suv bilan reaktsiyasi gidroksid ionlarining hosil bo'lishiga olib keladi. Ammiakning suvdagi eritmasi mavjud ishqoriy reaktsiya. Aminlarning suvdagi eritmalari ham ishqoriy reaksiya beradi. Ammo anilin zaifroq asos bo'lib, istaksiz reaksiyaga kirishadi.
Ammiak kislotalar bilan reaksiyaga kirishib ammoniy tuzlarini hosil qiladi. Ominlar kislotalar bilan ham reaksiyaga kirishishga qodir.
Alifatik aminlarning asosiy xossalari ammiaknikiga qaraganda ancha aniq. Bu bir yoki bir nechta donor alkil o'rnini bosuvchi moddalar mavjudligi bilan bog'liq bo'lib, ularning ijobiy induktiv ta'siri azot atomidagi elektron zichligini oshiradi. Elektron zichligi ortishi azotni kuchliroq elektron juft donorga aylantiradi, bu esa uning asosiy xususiyatlarini yaxshilaydi.
Anilin kislotalar bilan reaksiyalarda ham asosiy xususiyatlarga ega, ammo ular alifatik aminlarnikiga qaraganda kamroq aniqlanadi.
Aromatik aminlar holatida aminokislota va benzol halqasi bir-biriga sezilarli ta'sir ko'rsatadi.
Aminoguruh birinchi turdagi yo'naltiruvchi vositadir. Aminoguruh salbiy induktiv ta'sirga va aniq ijobiy mezomer ta'sirga ega. Shunday qilib, elektrofil almashtirish reaktsiyalari (bromlash, nitrlash) orto- va para-almashtirilgan mahsulotlarga olib keladi.
E'tibor bering, faqat katalizator - temir (III) xlorid ishtirokida bromlanadigan benzoldan farqli o'laroq, anilin bromli suv bilan reaksiyaga kirisha oladi. Bu amino guruhining benzol halqasidagi elektron zichligini oshirish (toluol va fenol molekulalaridagi o'rinbosarlarning o'xshash ta'sirini eslang) elektrofil almashtirish reaktsiyalarida aromatik tizimni faollashtirishi bilan izohlanadi. Bundan tashqari, anilin, benzoldan farqli o'laroq, suvda ozgina eriydi.
P-tizim interfeysi benzol halqasi aminokislotalarning yolg'iz elektron jufti bilan anilin alifatik aminlarga qaraganda sezilarli darajada zaifroq asos bo'lishiga olib keladi.
Amin va anilinning to'liq va to'liq bo'lmagan oksidlanish reaktsiyalarining xususiyatlari, oksidlanish va qaytarilish reaktsiyalarining o'zaro o'tishlari ko'rsatilgan.
HRMNING BARCHA NAMALLARI YOZILGAN, MAHSULOTLARGA NOMI BERILADI (tushuntirish evristik suhbat shaklida beriladi)
Ominlar va anilinlarni tayyorlash
1. Galogen hosilalaridan aminlar olish
CH3CH2Br + NH3 -> CH3CH2NH2 C6H5Br + NH3 -> C6H5NH2
2. Nitrobirikmalarni - alifatik va aromatiklarni qaytarish yo'li bilan birlamchi aminlarni olish. Qaytaruvchi vosita "chiqarilish vaqtida" vodorod bo'lib, masalan, ruxning gidroksidi yoki temirning xlorid kislotasi bilan o'zaro ta'siri natijasida hosil bo'ladi.
Amin va anilinni qo'llash
Ominlar dori vositalari va polimer materiallar ishlab chiqarish uchun keng qo'llaniladi. Anilin eng muhim birikma hisoblanadi bu sinfdan(diagramma), bu anilin bo'yoqlari, dorilar (sulfanilamid preparatlari), polimer materiallar (anilin formaldegid smolalari), portlovchi moddalar, raketa yoqilg'isi va pestitsidlar ishlab chiqarish uchun ishlatiladi.
"Reaktiv" yoki "reaktiv" bo'yoqlar bugungi kunda bozorda anilin bo'yoqlarining eng yaxshi tanlovidir. Ushbu bo'yoqlar guruhi o'simlik tolalaridan (paxta, zig'ir, viskoza, kanop, bambuk, qog'oz, jut va boshqalar) tayyorlangan matolar uchun juda yaxshi ekanligini isbotladi.
IV O'rganilgan materialni mustahkamlash
1. Metil-fenilamin molekulasidagi y-bog'lar sonini ko'rsating:
a) 6; b) 5; 7 da; d) 4.
2. Aminoguruhga fenil radikalining ta'siri anilinning qanday xossalari bilan izohlanadi?
a) anilin benzolga nisbatan almashtirish reaksiyalariga osonroq kiradi;
b) aromatik halqadagi elektron zichligi notekis taqsimlangan;
v) ammiakdan farqli ravishda anilinning suvdagi eritmasi lakmus rangini o'zgartirmaydi;
d) anilin qanday asosda ammiakdan kuchsizroq?
3. Umumiy bilan izomer aminlarning grafik formulalarini yozing molekulyar formula C4H11N. Ushbu moddalarni nomlang.
4. a) noorganik xom ashyodan ammoniy fenilxloridni oling.
HC1 + KOH spirti + HI + NH3 + HC1
b) Propanol-2 → ? → ? → ? → ? → ?
5. 11,2 litr metilamin (n.s.) bilan reaksiyaga kirishib, oʻrtacha tuz hosil qila oladigan 19,6% li sulfat kislota eritmasining massasini toping.
6. Fenol va anilin aralashmasi w (Br2) = 3% bo'lgan 480 g bromli suv bilan to'liq reaksiyaga kirishdi. Reaksiya mahsulotlarini zararsizlantirish uchun 36,4 sm3 NaOH eritmasi sarflandi (w = 10%, p = 1,2 g / sm3). Aniqlash massa ulushlari asl aralashmadagi moddalar.
7. 30 g benzol, fenol va anilin aralashmasini neytrallash uchun 49,7 ml 17% HC1 kerak (p = 1,0 g/ml). Aralashmaning bir xil miqdori bromli suv bilan reaksiyaga kirishganda 99,05 g cho`kma hosil bo`ladi. Asl aralashmadagi komponentlarning massa ulushlarini toping.
V Sinf faoliyatini baholash. Reflektsiya.
Anilinning asosiy xususiyatlari:
a) aromatik amin - anilin katta amaliy ahamiyatga ega;
b) anilin C 6 H 5 NH 2 suvda yomon eriydigan rangsiz suyuqlik;
v) havoda qisman oksidlanganda och jigarrang rangga ega;
d) anilin juda zaharli.
Anilinning asosiy xossalari ammiak va cheklovchi aminlarga qaraganda kuchsizroqdir.
1. Anilin lakmus rangini o'zgartirmaydi, lekin kislotalar bilan o'zaro ta'sirlashganda tuzlar hosil qiladi.
2. Agar anilinga konsentrlangan xlorid kislota qo'shilsa, ekzotermik reaksiya sodir bo'ladi va aralashmani sovutgandan so'ng tuz kristallari hosil bo'lishini kuzatish mumkin: + Cl - – fenilammoniy xlorid.
3. Fenilammoniy xlorid eritmasi ishqor eritmasi bilan ishlansa, u holda yana anilin ajralib chiqadi: [C 6 H 5 NH 3 ] + + Cl - + Na + + OH - → H 2 O + C 6 H 5 NH. 2 + Na + + CI -. Aromatik fenil radikalining ta'siri - C 6 H 5 - bu erda ifodalangan.
4. Anilin C 6 H 5 NH 2 da benzol halqasi aminokislotalar azotining yolg‘iz elektron juftini o‘ziga qarab siljitadi. Shu bilan birga, azotdagi elektron zichligi pasayadi va u vodorod ionini zaifroq bog'laydi, ya'ni moddaning asos sifatidagi xususiyatlari kamroq darajada namoyon bo'ladi.
5. Amino guruhi benzol halqasiga ta'sir qiladi.
6. Brom tarkibida suvli eritma benzol bilan reaksiyaga kirishmaydi.
Anilindan foydalanish usullari:
1) anilin– kimyo sanoatining eng muhim mahsulotlaridan biri;
2) ko'plab anilin bo'yoqlarini ishlab chiqarish uchun boshlang'ich materialdir;
3) anilin dorivor moddalar, masalan, sulfanilamid preparatlari, portlovchi moddalar, yuqori molekulyar birikmalar va boshqalarni ishlab chiqarishda qo'llaniladi Qozon universiteti professori N.N. Zinin (1842) anilin olishning qulay usuliga ega edi katta ahamiyatga ega kimyo va kimyo sanoatini rivojlantirish uchun.
1. Organik sintez sanoati bo'yoqlar ishlab chiqarishdan boshlandi.
2. Bu ishlab chiqarishning keng miqyosda rivojlanishi kimyoda hozirda ma'lum bo'lgan anilinni olish reaksiyasidan foydalanish asosida mumkin bo'ldi. Zinin reaktsiyalari.
Zinin reaktsiyasining xususiyatlari:
1) bu reaksiya nitrobenzolning qaytarilishidan iborat va quyidagi tenglama bilan ifodalanadi:
C 6 H 5 -NO 2 + 6H → C 6 H 5 -NH 2 + 2H 2 O;
2) anilin ishlab chiqarishning keng tarqalgan sanoat usuli - kislotali muhitda nitrobenzolni metallar, masalan, temir (cho'yan) bilan qaytarish;
3) tegishli tuzilishdagi nitrobirikmalarni tiklash hisoblanadi umumiy usul aminlarni olish.
74. Aminokislotalar
Tuzilishi va jismoniy xususiyatlar.
1.Aminokislotalar- bular molekulalarida NH 2 amino guruhi va karboksil guruhi - COOH bo'lgan moddalar.
Masalan: NH 2 -CH 2 -COOH aminosirka kislota, CH 3 -CH(NH 2)-COOH aminopropion kislota.
2. Aminokislotalar- Bular suvda eriydigan rangsiz kristall moddalardir.
3. Ko'pgina aminokislotalar shirin ta'mga ega.
4. Aminokislotalarni karboksilik kislotalar deb hisoblash mumkin, ularning molekulalarida radikaldagi vodorod atomi aminokislotalar bilan almashtiriladi. Bunday holda, aminokislotalar izomeriyasining turlaridan birini keltirib chiqaradigan aminokislotalar turli xil uglerod atomlarida joylashgan bo'lishi mumkin.
Aminokislotalarning ba'zi vakillari:
1) aminoasetik kislota H 2 N-CH 2 -COOH;
2) aminopropion kislota H 2 N-CH 2 -CH 2 -COOH;
3) aminobutirik kislota H 2 N-CH 2 -CH 2 -CH 2 -COOH;
4) aminovaler kislota H 2 N-(CH 2) 4 -COOH;
5) aminokaproik kislota H 2 N-(CH 2) 5 -COOH.
5. Aminokislotalar molekulasida uglerod atomlari qancha ko'p bo'lsa, karboksil guruhiga nisbatan aminokislotalarning turli pozitsiyalari bilan ko'proq izomerlar mavjud bo'lishi mumkin.
6. Izomerlarning nomi guruhning karboksilga nisbatan NH 2 o'rnini ko'rsatishi uchun aminokislotalar molekulasidagi uglerod atomlari ketma-ket yunon alifbosi harflari bilan belgilanadi: a) a-aminokaproik kislota. ; b) b-aminokaproik kislota.
Aminokislotalarning tuzilishi xususiyatlari izomeriyadan iborat bo'lib, bu uglerod skeletining shoxlanishi, shuningdek, uning uglerod zanjirining tuzilishi bilan ham bog'liq bo'lishi mumkin.
Aminokislotalarni qo'llash usullari:
1) aminokislotalar tabiatda keng tarqalgan;
2) aminokislotalar molekulalari barcha o'simlik va hayvon oqsillari qurilgan qurilish bloklari; tana oqsillarini yaratish uchun zarur bo'lgan aminokislotalar odamlar va hayvonlar tomonidan oziq-ovqat oqsillarining bir qismi sifatida olinadi;
3) aminokislotalar og'ir charchoq uchun, og'ir operatsiyalardan keyin buyuriladi;
4) ular oshqozon-ichak traktini chetlab o'tib, bemorlarni ovqatlantirish uchun ishlatiladi;
5) aminokislotalar ma'lum kasalliklarga davo sifatida zarur (masalan, glutamin kislotasi asab kasalliklarida, histidin oshqozon yarasi uchun ishlatiladi);
6) ba'zi aminokislotalar qishloq xo'jaligida hayvonlarni boqish uchun ishlatiladi, bu ularning o'sishiga ijobiy ta'sir qiladi;
7) texnik ahamiyatga ega: aminokaproik va aminoantik kislotalar sintetik tolalar - kapron va enant hosil qiladi.
Dars maqsadlari: haqida talabalar bilimini mustahkamlash uchun tahlil misolidan foydalaning kimyoviy xossalari ah aminlar; aromatik aminlar haqida tushuncha berish; ko'rsatish amaliy ahamiyati anilin kimyo sanoatining eng muhim mahsuloti sifatida.
Uskunalar: ko'rgazmali stolda - anilin, suv, fenolftalein, xlorid kislotasi, ishqor eritmasi, probirkalar.
Aniqlash maqsadida anilin o'rganilmoqda umumiy tushuncha aminlar haqida va bu birikmalar sinfining eng muhim vakili sifatida.
Shu munosabat bilan, dars vazifa va savollarni muhokama qilish uchun talabalarni maksimal darajada jalb qilgan holda hikoya shaklida o'tkazilishi mumkin:
Uglevodorodlarning gomologik qatorlarini ayting va ularning tuzilishi xususiyatlarini ko'rsating.
Ominlar qanday moddalardir?
Aromatik aminning formulasi qanday?
Anilinning asosiy xossalarini namoyon etishini qanday isbotlash mumkin? Kimyoviy reaksiya tenglamasini yozing.
Keyinchalik, talabalar e'tibori anilin va brom o'rtasidagi reaksiyaga qaratiladi, aminokislotalarning benzol halqasiga ta'siri haqida to'xtalmasdan, faqat anilin molekulasining strukturaviy xususiyatlari bu reaktsiyani amalga oshirishga imkon berishini ko'rsatadi.
Bo'yoqlar, turli farmatsevtika preparatlari, fotoreagentlar, portlovchi moddalar, plastmassalar va boshqalarni ishlab chiqarish uchun anilin ishlab chiqarish va ulardan foydalanish bo'yicha. - deydi o'qituvchi.
Ushbu darsda, bizning fikrimizcha, anilinni ishlab chiqarish va ishlatish haqidagi hikoyada aminokislotalarni qo'llashda ham ishlab chiqarishdan, ham qo'shimcha mahsulotlardan chiqindilarning toksik ta'sirini qayd etish maqsadga muvofiqdir.
Batafsil dars rejasi
Ushbu mavzuni o'rganishda rivojlanish haqidagi asosiy fikrni mustahkamlash kerak organik moddalar va ularning xilma-xilligini keltirib chiqaradigan sabablar; tushunchasini chuqurlashtirish kovalent bog'lanish aminlarga misollar yordamida; haqidagi bilimlarni kengaytirish vodorod aloqalari va amfoter birikmalar.
Mavzuni ko'rib chiqishni boshlashda talabalardan qaysi azotli birikmalarni bilishlarini eslab qolishlari so'raladi. Talabalar nitrobenzol, nitrogliserin, trinitrotsellyuloza nomlarini aytadilar. Nitrobenzolning xossalari va laboratoriya sharoitida olinishi haqidagi ma’lumotlarni qisqacha takrorlang. Shu bilan birga, doskada reaksiya tenglamasini tuzadilar, uning turini (almashtirish) qayd qiladilar va unga nom beradilar (nitrlanish reaktsiyasi). Nitrlash reaksiyalarini olib borish mumkinmi degan savolga to'yingan uglevodorodlar, talabalar ijobiy javob beradilar. Shundan so'ng, beshinchi gomologgacha bo'lgan nitrlanish reaktsiyalari tenglamalarini yozing. O'qituvchi bu reaksiyalarni birinchi bo'lib rus olimi M.I. Konovalov 1886. Nitrobenzolga oʻxshatib, yangi olingan azotli moddalarga – nitrometan, nitroetan va boshqalarga nom beradi. Keyin o'qituvchi talabalarni olingan gomologlarning fizik xususiyatlari bilan qisqacha tanishtiradi. Nitrobirikmalarning kimyoviy xossalari orasida ularning vodorod bilan kamaytirilish qobiliyatini ta'kidlash kerak. Talabalar yangi azot o'z ichiga olgan moddalarning gomologik qatori hosil bo'lishiga ishonch hosil qilishlari va ularni mustaqil ravishda nomlashlari uchun ular reaktsiya tenglamalarini tuzadilar:
CH 3 NO 2 + 3H 2 2H 2 O + CH 3 NH 2
C 2 H 5 NO 2 + 3 H 2 2 H 2 O + C 2 H 5 NH 2
C 3 H 7 NO 2 + 3 H 2 2 H 2 O + C 3 H 7 NH 2 va boshqalar.
Atomlarning yangi funktsional guruhi - NH 2 - aminokislotalarning shakllanishiga e'tibor bering. Bu erda shuni ta'kidlash kerakki, ular "amin" so'zini qo'shgan holda molekulaning bir qismi bo'lgan radikallar tomonidan aminlar deb ataladi. Shundan so‘ng o‘quvchilar hosil bo‘ladigan moddalarni bemalol nomlashlari mumkin: metilamin, etilamin va boshqalar.Nitratlanish reaksiyalari uchun avval yozilgan tenglamalarni qaytarilish reaksiyalari bilan solishtirib, ular o‘rtasida genetik bog‘liqlik bor degan xulosaga keladilar. gomologik qator organik moddalar: uglevodorodlar nitro birikmalarga, nitro birikmalar esa aminlarga aylanishi mumkin:
CH 4 + HNO 3 H 2 O + CH 3 NO 2;
CH 3 NO 2 + 3H 2 2H 2 O + CH 3 NH 2.
Bu birikmalar yog'li aminlardir, chunki ular to'yingan uglevodorodlardan olinadi. Keyin amin seriyasining birinchi a'zolarining fizik xususiyatlari tasvirlanadi. Ularning kimyoviy xususiyatlarini o'rganishga o'tishdan oldin, funktsional guruhning tarkibiga e'tibor bering. Aminoguruh - bu ammiak qoldig'i bo'lib, unda bitta vodorod atomi uglevodorod radikali bilan almashtiriladi. Keyinchalik ular aminlarni ammiakning hosilalari sifatida ko'rib chiqishni taklif qilishadi. Talabalar yana ikkita vodorod atomi ammiakda uglevodorod radikallari bilan almashtirilishi mumkinligini ta'kidlaydilar. Keyin, molekulaga kiritilgan uglevodorod qoldiqlari soniga qarab, aminlar bo'lishi mumkin
CH 3 NH 2, C 2 H 5 NH 2
asosiy
ikkinchi darajali
uchinchi darajali
Tabiatda aminlar oqsil birikmalarining parchalanishi paytida topiladi; masalan, seld sho'ri tarkibida metilamin, dimetilamin, tri-metilamin mavjud. Barcha aminlar ammiakning hosilalaridir, shuning uchun ular ham unga o'xshash bo'lishi kerak. Talabalar bu savolni mustaqil ravishda hal qilishlari mumkin (bu dars uchun ular ammiakning xususiyatlarini ko'rib chiqishlari kerak). Masalan, talabalardan biri doskaning chap tomoniga ammiakning kimyoviy xossalarini tavsiflovchi reaksiyalar tenglamalarini (suv bilan, kislotalar bilan reaksiya, kislorod oqimida yonish) yozadi. Bu tajribalar, ayniqsa, ammiak qobiliyatini ta'kidlab, bu erda ko'rsatilgan faqat kislorod oqimida yonadi.
Keyin shunga o'xshash tajribalar aminlar bilan amalga oshiriladi (1.1.3.1-bandga qarang). Tajribalar asosida aminlarning xossalari haqida xulosalar chiqariladi.
Ammiakdan farqli o'laroq, aminlar havoda yonadi. Ular shunday xulosaga kelishadi: aminlar kimyoviy xossalari bo'yicha ammiakga o'xshaydi, lekin undan farqli o'laroq, ular havoda yonadi. Bu xususiyat olim Vurtsni 1848 yilda aminlarni kashf etishga olib keldi. Tushuntirish jarayonida ammiakning xossalari bilan parallel ravishda doskaning o'ng tomoniga aminlar bilan reaksiya tenglamalari yoziladi. Ammiak va aminlarning xossalarini solishtirish natijasida o`quvchilar organik moddalar orasida asos xossalariga ega bo`lgan moddalar - organik asoslar borligiga ishonch hosil qiladilar. Bu ammoniy ionining hosil bo'lishi misolidan foydalanib, elektron tuzilishga asoslangan holda tushuntiriladi. Sizga shuni eslatib o'tamizki, azot atomining beshta valentlik elektronidan uchta juftlashtirilmagan elektron vodorod atomlari bilan kovalent bog'lanish hosil qilish uchun boradi va ammiak molekulasini hosil qiladi va ikkita juftlashgan elektron bo'linmagan va erkin qoladi. Ular tufayli azot atomida suv yoki kislotaning vodorod ioni (proton) bilan kovalent bog'lanish o'rnatiladi. Bunday holda, birinchi holda, asoslarning xususiyatlarini aniqlaydigan gidroksil ionlari, ikkinchisida - kislotali qoldiqning ionlari chiqariladi. Ko'rib chiqmoqdalar elektron tuzilma aminlar:
Alohida e'tibor ammiakdagi kabi vodorod protoni bilan kovalent bog'lanish hosil qilish uchun ketadigan azotning yolg'iz elektron juftligiga qaratiladi. Bu holda, agar vodorod proton (ion) kislotadan bo'lsa, asos (1) yoki tuz (2) xususiyatlariga ega organik birikma hosil bo'ladi:


Tuz formulasi boshqacha yozilishi mumkin:
CH 3. NH 2. HC1
Metilamin gidroxlorid
Talabalar moddalarning xossalari tuzilishiga qarab belgilanishini biladilar. Ammoniy gidroksid va metilammoniyning elektron tuzilishini solishtirish. ular qaysi moddalar - aminlar yoki ammiak - kuchliroq asoslar ekanligini aniqlashlari mumkin.
Metil radikali elektron zichligini siqib chiqarishga qodir ekanligini eslash tavsiya etiladi. Keyin azotda ortib borayotgan elektron zichligi paydo bo'ladi va u molekulada vodorod protonini mustahkamroq ushlab turadi. Gidroksil ioni ajralib chiqadi, uning eritmadagi konsentratsiyasi ortadi, shuning uchun yog'li aminlar ammiakdan ko'ra kuchliroq asoslardir. Materialni mustahkamlash uchun o'qituvchi savol beradi: dimetilamin va trimetilamin asosiy xususiyatlarni kuchaytirishi yoki zaiflashishi kutiladimi? Talabalar radikal elektron zichlikni siqib chiqarishga qodir ekanligini bilishadi, shuning uchun ular mustaqil ravishda ikki va uch o'rinli aminlar mono almashtirilganlarga nisbatan kuchliroq asoslar bo'lishi kerak degan xulosaga kelishadi. Ikki radikal azotdagi elektron zichligini ko'proq oshiradi va shuning uchun azot vodorod ionini kuchliroq ushlab turadi va gidroksil ionlari eritmaga kira boshlaydi, ya'ni. aminlarning asosiy xossalarining kuchi azot atomidagi manfiy zaryadning kattaligiga bog'liq: u qanchalik katta bo'lsa, asoslarning kuchi shunchalik katta bo'ladi. Uchinchi darajali amin eng kuchli asos bo'lishi kerakdek tuyuladi, ammo tajriba buning aksini ko'rsatadi. Ko'rinib turibdiki, uchta metil radikali azot elektronlarining yolg'iz juftligini himoya qiladi, vodorod ionlarining erkin qo'shilishiga xalaqit beradi va shuning uchun eritmaga ozgina gidroksil ionlari kiradi, shuning uchun muhit zaif asosli hisoblanadi.
Talabalar organik moddalar sinflari o'rtasidagi genetik aloqani yaxshiroq tushunishlari uchun ular barcha "ajdodlar" dan aromatik aminlarning hosil bo'lishini tahlil qiladilar. aromatik uglevodorodlar- nitro birikmalar orqali benzol. Avvalo, ular to'yingan uglevodorodlardan yog'li aminlarni olish usullarini qisqacha eslashadi, so'ngra ular benzolning avval o'rganilgan xususiyatlarini esga olishni va ularni benzolning elektron tuzilishiga asoslanib tushuntirishni taklif qilishadi. Buning uchun benzolning elektron tuzilishi jadvalini joylashtirish va uning molekulasi modelini tayyorlash maqsadga muvofiqdir. Shunday qilib, talabalarning o'zlari nitrobenzol orqali benzoldan fenilamingacha "ipni cho'zadilar" va mos keladigan reaktsiya tenglamalarini osongina yozadilar.
Bu yerda ular nitrobenzolni qayta oqim kondensatorli kolbada olish tajribasini namoyish etadilar. Tegishli reaksiya tenglamasini doskaga yozing. Keyin hosil bo'lgan nitrobenzolni anilinga qaytarish uchun tajriba o'tkaziladi. Bu tajriba davomida talabalarga N.N.ning reaksiyasi haqida ma’lumot beriladi. Zinin va uning xalq xo'jaligi uchun ahamiyati.
Keyin ular sof anilinni (agar u maktabda mavjud bo'lsa), uning toksikligi va uni ehtiyotkorlik bilan ishlatish haqida gapirib berishadi. Ba'zi jismoniy xususiyatlarni ko'rsating: agregatsiya holati, rangi, hidi, suvda eruvchanligi.
Keyin ular anilinning kimyoviy xossalarini o'rganishga o'tadilar. Yog'li aminlarga o'xshab, anilin asosiy xususiyatlarga ega deb taxmin qilinadi. Buning uchun anilinning suvda eruvchanligi tekshirilgan stakanga bir necha tomchi fenolftalein qo'shing. Eritmaning rangi o'zgarmaydi. Anilinning konsentrlangan xlorid va sulfat kislotalar bilan o'zaro ta'sirini tekshiring. Aralashmani sovutgandan so'ng, talabalar tuzlarning kristallanishini kuzatadilar, shuning uchun anilin yog'li aminlardan zaif bo'lmagan asoslar xossalarini namoyon qiladi. Ushbu tajribalarni muhokama qilish jarayonida reaksiya tenglamalari tuziladi va hosil bo'lgan moddalarga nomlar beriladi.
Keyinchalik, ular anilin tuzlarining gidroksidi bilan o'zaro ta'sirini ko'rsatadilar (biz ammoniy tuzlari bilan o'xshashlikni chizamiz). Shu o‘rinda savol tug‘iladi: agar seld sho‘r suvi ishqor bilan reaksiyaga kirishib, aminlar hosil qilsa, yog‘li aminlar qanday birikmalar ko‘rinishida topiladi? (Qoida tariqasida, talabalar javob berishadi: tuzlar shaklida). Ularning suvda eruvchanligi va anilin tuzlarining oksidlovchi moddalar bilan, masalan, kaliy bixromati bilan o'zaro ta'siri tekshiriladi. Bu reaksiya turli rangdagi moddalarni aniqlaydi. Talabalarga ko'plab anilin bo'yoqlari (jumladan, sintetik indigo kabi qimmatli bo'yoqlar), dorivor moddalar, plastmassalar ishlab chiqarish anilinning xususiyatlariga asoslanganligi haqida ma'lumot beriladi. Xulosa qilib aytganda, ular anilinning oqartiruvchi bilan o'zaro ta'sir qilish tajribasini namoyish etadilar. Bu reaksiya anilinga xos ekanligi qayd etilgan. Sinov uchun nitrobenzolni metallar bilan qaytarish bo'yicha tajriba davomida olingan moddalar aralashmasida anilinni aniqlash taklif etiladi. Talabalar sinflar o'rtasida genetik bog'liqlik mavjudligiga yana bir bor ishonch hosil qilishdi. O'rganilgan narsalarni mustahkamlash uchun quyidagi o'zgarishlarni amalga oshirish imkoniyatini tasdiqlovchi reaktsiya tenglamalarini tuzish taklif etiladi:
Talabalar buni tajriba orqali ko'rishadi anilinning asosiy xossalari chegaralovchi qator aminlari bilan solishtirganda zaiflashadi. Bu aromatik fenil radikalining C 6 H 5 ta'siri bilan izohlanadi. Aniqlik uchun benzolning elektron tuzilishini yana bir bor ko'rib chiqamiz. Talabalar benzol yadrosining harakatlanuvchi elektron buluti oltita elektrondan hosil bo'lishini eslashadi (molekulaning modeli yoki benzol molekulasining yaxshi chizilgani yaxshi). Shuni ta'kidlash kerakki, benzol halqasida bitta vodorod atomi o'rniga aminokislotalar mavjud bo'lib, amin molekulasining elektron tuzilishini chizib oling va yana bir bor aminokislotadagi azot atomining erkin yolg'iz elektron juftligiga e'tibor bering. benzol halqasining -elektronlari bilan o'zaro ta'sir qiladi. Natijada, azotdagi elektron zichligi kamayadi, elektronlarning erkin juftligi vodorod protonini kamroq kuch bilan ushlab turadi va eritmaga oz miqdorda gidroksil ionlari kiradi. Bularning barchasi indikatorlar bilan reaksiyaga kirishganda kuzatilgan anilinning zaif asosiy xususiyatlarini aniqlaydi.
Aminoguruhning azot elektronlarining yolg'iz juftligi benzol halqasining -elektronlari bilan o'zaro ta'sirlashib, elektron zichligini orto va para pozitsiyalariga siljitadi, bu joylarda benzol halqasini kimyoviy jihatdan faolroq qiladi. Bu anilinning bromli suv bilan o'zaro ta'siri tajribasi bilan osongina tasdiqlanadi, bu darhol ko'rsatiladi:


Xulosa qilib aytganda, o`quvchilar tabiatda mavjud bo`lgan moddalar o`rtasidagi bog`lanishga, ularning oddiydan murakkabgacha rivojlanishiga e`tibor berishlari kerak.
Aminlar bizning hayotimizga mutlaqo kutilmaganda kirib keldi. Yaqin vaqtgacha bular edi zaharli moddalar, o'limga olib kelishi mumkin bo'lgan to'qnashuv. Va endi, bir yarim asr o'tgach, biz sintetik tolalar, matolar, qurilish materiallari va aminlar asosidagi bo'yoqlardan faol foydalanamiz. Yo'q, ular xavfsizroq bo'lishmadi, odamlar shunchaki ularni "o'ylash" va bo'ysundirish, o'zlari uchun ma'lum foyda olish imkoniyatiga ega bo'lishdi. Qaysi biri haqida yana gaplashamiz.
Ta'rif
Eritmalarda yoki birikmalarda anilinni sifat va miqdoriy aniqlash uchun reaksiyadan foydalaniladi, uning oxirida probirka tubiga 2,4,6-tribromoanilin ko`rinishidagi oq cho`kma tushadi.
Tabiatdagi aminlar
Ominlar tabiatning hamma joylarida vitaminlar, gormonlar va oraliq metabolik mahsulotlar shaklida mavjud bo'lib, ular hayvonlarning tanasida ham, o'simliklarda ham mavjud. Bundan tashqari, tirik organizmlarning parchalanishi suyuq holatda seld sho'rligining yoqimsiz hidini chiqaradigan o'rta aminlarni ham hosil qiladi. Adabiyotda keng tavsiflangan "kadavra zahari" aniq aminlarning o'ziga xos amberi tufayli paydo bo'ldi.
Uzoq vaqt davomida biz ko'rib chiqayotgan moddalar o'xshash hid tufayli ammiak bilan aralashib ketgan. Ammo XIX asr o'rtalarida frantsuz kimyogari Vurtz metilamin va etilaminni sintez qila oldi va yondirilganda uglevodorodlar ajralib chiqishini isbotladi. Bu aytib o'tilgan birikmalar va ammiak o'rtasidagi asosiy farq edi.
Sanoat sharoitida aminlarni ishlab chiqarish
Aminlardagi azot atomi eng past oksidlanish darajasida bo'lganligi sababli, azot o'z ichiga olgan birikmalarning qaytarilishi ularni olishning eng oddiy va eng qulay usuli hisoblanadi. Aynan shu tur arzonligi tufayli sanoat amaliyotida keng qo'llaniladi.
Birinchi usul - nitro birikmalarini kamaytirish. Anilin hosil bo'ladigan reaktsiya olim Zinin tomonidan nomlangan va birinchi marta XIX asr o'rtalarida amalga oshirilgan. Ikkinchi usul lityum alyuminiy gidrid yordamida amidlarni kamaytirishdir. Birlamchi aminlarni nitrillardan ham olish mumkin. Uchinchi variant - alkillanish reaktsiyalari, ya'ni ammiak molekulalariga alkil guruhlarini kiritish.
Aminlarni qo'llash

O'z-o'zidan, shaklda toza moddalar, aminlar kamdan kam qo'llaniladi. Noyob misollardan biri - polietilen poliamin (PEPA), uy sharoitida epoksi qatronining qattiqlashishini osonlashtiradi. Asosan birlamchi, uchinchi yoki ikkilamchi aminlar turli xil organik moddalar ishlab chiqarishda oraliq mahsulotdir. Eng mashhuri anilindir. Bu anilin bo'yoqlarining katta palitrasining asosidir. Oxirida olingan rang to'g'ridan-to'g'ri tanlangan xom ashyoga bog'liq. Sof anilin beradi Moviy rang, va anilin, orto- va para-toluidin aralashmasi qizil bo'ladi.
Alifatik aminlar poliamidlar, masalan, neylon va boshqalarni olish uchun kerak.Ular mashinasozlikda, shuningdek, arqonlar, gazlamalar va plyonkalar ishlab chiqarishda qo'llaniladi. Bundan tashqari, poliuretan ishlab chiqarishda alifatik diizosiyanatlar qo'llaniladi. Istisno xossalari (engilligi, mustahkamligi, elastikligi va har qanday sirtga yopishtirish qobiliyati) tufayli ular qurilishda (ko‘pik, elim) va poyabzal sanoatida (slipga qarshi taglik) talabga ega.
Tibbiyot aminlar qo'llaniladigan yana bir sohadir. Kimyo ulardan sulfanilamid guruhidan antibiotiklarni sintez qilishga yordam beradi, ular ikkinchi darajali dorilar, ya'ni zaxira sifatida muvaffaqiyatli qo'llaniladi. Bakteriyalar muhim dorilarga qarshilik ko'rsatsa.
Inson tanasiga zararli ta'sir
Ma'lumki, aminlar juda zaharli moddalardir. Ular bilan har qanday o'zaro ta'sir sog'likka zarar etkazishi mumkin: bug'larni inhalatsiyalash, ochiq teri bilan aloqa qilish yoki birikmalarni tanaga kiritish. O'lim kislorod etishmasligidan kelib chiqadi, chunki aminlar (xususan, anilin) qondagi gemoglobin bilan bog'lanadi va uning kislorod molekulalarini ushlashiga to'sqinlik qiladi. Xavotir beruvchi alomatlar nafas qisilishi, nazolabial uchburchak va barmoq uchlarining ko'k rangi o'zgarishi, taxipnea (tez nafas olish), taxikardiya, ongni yo'qotishdir.
Agar bu moddalar tananing yalang'och joylariga tushsa, ularni oldindan spirtga namlangan paxta bilan tezda olib tashlashingiz kerak. Bu ifloslanish maydonini ko'paytirmaslik uchun iloji boricha ehtiyotkorlik bilan bajarilishi kerak. Agar zaharlanish belgilari paydo bo'lsa, albatta shifokorga murojaat qilishingiz kerak.
Alifatik aminlar asab va yurak-qon tomir tizimlari uchun zahardir. Ular jigar funktsiyasining tushkunligiga, jigar distrofiyasiga va hatto siydik pufagi saratoniga olib kelishi mumkin.