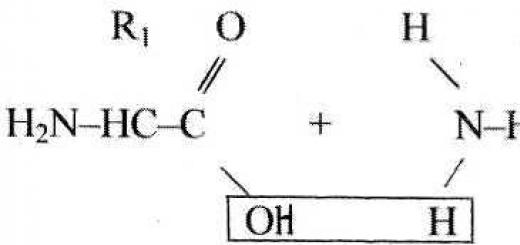
Kémiai tulajdonságok a-aminosavak határozzák meg leginkább általános eset, karboxil- és amincsoportok jelenléte ugyanazon a szénatomon. Az aminosavak mellékfunkciós csoportjainak specifitása meghatározza reaktivitásuk különbségeit és az egyes aminosavak egyéniségét. A polipeptidek és fehérjék molekuláiban az oldalfunkciós csoportok tulajdonságai kerülnek előtérbe, i. miután az amin- és karboxilcsoportok elvégezték a dolgukat - poliamid láncot alkotnak.
Tehát magának az aminosav-fragmensnek a kémiai tulajdonságai aminreakciókra, reakciókra oszlanak karbonsavakés a tulajdonságok kölcsönös hatásuk miatt.
A karboxilcsoport lúgokkal való reakciókban nyilvánul meg - karboxilátokat képezve, alkoholokkal - észtereket képezve, ammóniával és aminokkal - savamidokat képezve, az a-aminosavak hevítésre és enzimek hatására meglehetősen könnyen dekarboxileződnek (4.2.1. ábra). .
Ennek a reakciónak fontos élettani jelentősége van, mivel in vivo végrehajtása megfelelő biogén aminok képződéséhez vezet, amelyek számos funkciót látnak el: konkrét funkciókatélő szervezetekben. A hisztidin dekarboxilezésekor hisztamin képződik, aminek hormonális hatása van. Az emberi szervezetben kötött formában, gyulladásos és allergiás reakciók, anafilaxiás sokk során szabadul fel, hajszálerek tágulását, simaizmok összehúzódását okozza, élesen növeli a szekréciót. sósavból a gyomorban.
Ezenkívül a dekarboxilezési reakcióval az aromás gyűrű hidroxilezési reakciójával együtt egy másik biogén amin, a szerotonin képződik a triptofánból. Emberben megtalálható a bélsejtekben a vérlemezkékben, a coelenterates, puhatestűek, ízeltlábúak és kétéltűek mérgében, és megtalálható a növényekben (banán, kávé, homoktövis). A szerotonin közvetítő funkciókat lát el a központi és a perifériás területen idegrendszerek, befolyásolja az erek tónusát, növeli a hajszálerek ellenállását, és növeli a vérlemezkék számát (4.2.2. diagram).
Az aminosavak aminocsoportja savakkal való reakciókban nyilvánul meg, ammóniumsókat képezve és acilezve
4.2.1
4.2.2

és savhalogenidekkel és alkilhalogenidekkel reagálva alkilez, aldehidekkel Schiff-bázisokat képez, salétromsavval pedig a közönséges primer aminokhoz hasonlóan a megfelelő hidroxiszármazékokat, jelen esetben hidroxisavakat képez (4.2.3. ábra).
4.2.3

Az aminocsoport és a karboxil funkció egyidejű részvétele kémiai reakciók elég változatos. Az a-aminosavak sok kétértékű fém ionjaival alkotnak komplexeket - ezek a komplexek fémiononként két aminosavmolekula részvételével épülnek fel, míg a fém ligandumokkal kétféle kötést hoz létre: a karboxilcsoport a fémmel alakul ki. ionos kötés, és az aminocsoport a fém szabad pályáihoz koordinálva magányos elektronpárjával vesz részt (donor-akceptor kötés), ún. kelát komplexeket adva (4.2.4. ábra, a fémek a stabilitás szerint sorba rendeződnek a komplexek közül).
Mivel egy aminosav molekula savas és bázikus funkciót is tartalmaz, a köztük lévő kölcsönhatás mindenképpen elkerülhetetlen - belső só (ikerion) képződéséhez vezet. Mivel ez egy gyenge sav és egy gyenge bázis sója, ez vizesoldat könnyen hidrolizál, pl. a rendszer egyensúlyi. BAN BEN kristályos állapot az aminosavak tisztán ikerionos szerkezetűek, ezért ezeknek az anyagoknak a tartalma magas (4.2.5. ábra).
4.2.4

4.2.5

A ninhidrin reakciónak van nagyon fontos aminosavak kimutatására azok minőségi és mennyiségi elemzés. A legtöbb aminosav reakcióba lép a ninhidrinnel, felszabadítva a megfelelő aldehidet, és az oldat intenzív kék-lila színűvé válik (nm), oldatok narancsszín(nm) csak prolint és hidroxiprolint adnak. A reakcióséma meglehetősen bonyolult, közbenső szakaszai nem teljesen egyértelműek, a színezett reakcióterméket „Ruemann-ibolyának” nevezik (4.2.6. ábra).
A diketopiperazinok szabad aminosavak melegítésével, vagy még jobb esetben észtereik melegítésével keletkeznek.
4.2.6

A reakciótermék szerkezete alapján - pirazin heterociklus származékaként, és a reakcióvázlat alapján - ciklusos kettős amidként határozható meg, mivel aminocsoportok karboxil funkciós csoportjainak kölcsönhatásából jön létre a nukleofil szubsztitúciós séma szerint ( 4.2.7. séma).
Az α-aminosav-poliamidok képződése a diepiperazinok képződésének fentebb leírt reakciója, és
4.2.7

4.2.8

egy olyan fajta, amelyhez a természet valószínűleg ezt a vegyületosztályt alkotta. A reakció lényege, hogy az egyik α-aminosav amincsoportjának nukleofil támadása a második α-aminosav karboxilcsoportja ellen, míg a második aminosav amincsoportja egymás után támadja meg a harmadik aminosav karboxilcsoportját. stb. (4.2.8. diagram).
A reakció eredménye egy poliamid vagy (a fehérjék és fehérjeszerű vegyületek kémiájával kapcsolatban nevezett) polipeptid. Ennek megfelelően a -CO-NH- fragmentumot peptidegységnek vagy peptidkötésnek nevezzük.
Az aminosavak minden élő szervezet fő építőanyagai. Természetüknél fogva a növények elsődleges nitrogéntartalmú anyagai, amelyek a talajból szintetizálódnak. Az aminosavak szerkezete összetételüktől függ.
Aminosav szerkezet
Mindegyik molekulája tartalmaz karboxil- és amincsoportokat, amelyek egy-egy gyökhöz kapcsolódnak. Ha egy aminosav 1 karboxil- és 1 aminocsoportot tartalmaz, szerkezetét az alábbi képlettel jelezhetjük.

Azokat az aminosavakat, amelyekben 1 sav és 1 lúgos csoport van, monoamino-monokarbonsavaknak nevezzük. Az organizmusokban 2 karboxilcsoport vagy 2 amincsoport is szintetizálódik, és ezek funkciói meghatározásra kerülnek. A 2 karboxil- és 1 amincsoportot tartalmazó aminosavakat monoamino-dikarbonsavnak, a 2 amint és 1 karboxilcsoportot tartalmazó aminosavakat diamino-monokarbonsavnak nevezzük.
Az R szerves gyök szerkezetében is különböznek egymástól. Mindegyiknek megvan a maga neve és szerkezete. Ennélfogva különféle funkciókat aminosavak. A savas és lúgos csoportok jelenléte biztosítja a magas reakcióképességet. Ezek a csoportok összekapcsolják az aminosavakat, és polimert - fehérjét képeznek. A fehérjéket szerkezetük miatt polipeptideknek is nevezik.
Aminosavak, mint építőanyagok
A fehérje molekula több tíz vagy száz aminosavból álló lánc. A fehérjék összetételében, mennyiségében és az aminosavak sorrendjében különböznek, mivel a 20 komponens kombinációinak száma szinte végtelen. Némelyikük az esszenciális aminosavak teljes összetételét tartalmazza, mások nélkülözik egyet vagy többet. Az egyes aminosavakat, amelyek funkciója hasonló az emberi szervezet fehérjéihez, nem használják élelmiszerként, mivel rosszul oldódnak, és a gyomor-bél traktus nem bontja le őket. Ide tartoznak a köröm, a haj, a szőr vagy a toll fehérjéi.
Az aminosavak funkcióit nehéz túlbecsülni. Ezek az anyagok az emberi étrend fő táplálékai. Milyen funkciót töltenek be az aminosavak? Növelik az izomtömeg növekedését, segítik az ízületek és szalagok erősítését, helyreállítják a sérült testszöveteket és részt vesznek az emberi szervezetben végbemenő összes folyamatban.

Esszenciális aminosavak
Csak adalékanyagokból ill élelmiszer termékek beszerezhető Funkciók az egészséges ízületek, erős izmok, szép haj kialakulásának folyamatában nagyon jelentősek. Ezek az aminosavak a következők:
- fenilalanin;
- lizin;
- treonin;
- metionin;
- valin;
- leucin;
- triptofán;
- hisztidin;
- izoleucin.
Az esszenciális aminosavak funkciói
Ezek a téglák alapvető funkciókat látnak el az emberi test minden sejtjének működésében. Mindaddig láthatatlanok, amíg kellő mennyiségben bejutnak a szervezetbe, de hiányuk jelentősen rontja az egész szervezet működését.
- A valin megújítja az izmokat, és kiváló energiaforrásként szolgál.
- A hisztidin javítja a vér összetételét, elősegíti az izmok regenerálódását és növekedését, valamint javítja az ízületek működését.
- Az izoleucin segíti a hemoglobin termelődését. Szabályozza a cukor mennyiségét a vérben, növeli az ember energiáját és állóképességét.
- A leucin erősíti az immunrendszert, figyeli a vércukor- és leukociták szintjét. Ha a leukociták szintje túl magas: csökkenti azokat, és aktiválja a szervezet tartalékait a gyulladás megszüntetésére.
- A lizin elősegíti a kalcium felszívódását, amely építi és erősíti a csontokat. Segíti a kollagéntermelést, javítja a haj szerkezetét. Férfiak számára ez egy kiváló anabolikus szteroid, mivel izmot épít és növeli a férfi erőt.
- A metionin normalizálja az emésztőrendszer és a máj működését. Részt vesz a zsírok lebontásában, megszünteti a toxikózist terhes nőknél, jótékony hatással van a hajra.
- A treonin javítja a gyomor-bél traktus működését. Növeli az immunitást, részt vesz az elasztin és a kollagén képződésében. A treonin megakadályozza a zsír lerakódását a májban.
- A triptofán felelős az emberi érzelmekért. Szerotonint termel - a boldogság hormonját, ezáltal normalizálja az alvást és javítja a hangulatot. Csillapítja az étvágyat, jótékony hatással van a szívizomra és az artériákra.
- A fenilalanin az idegsejtektől a fej agyába irányuló jelek továbbítójaként szolgál. Javítja a hangulatot, elnyomja az egészségtelen étvágyat, javítja a memóriát, növeli az érzékenységet, csökkenti a fájdalmat.
Az esszenciális aminosavak hiánya növekedési visszamaradáshoz, anyagcserezavarokhoz és izomtömeg csökkenéshez vezet.

Nem esszenciális aminosavak
Ezek olyan aminosavak, amelyek szerkezetét és funkcióit a szervezet termeli:
- arginin;
- alanin;
- aszparagin;
- glicin;
- prolin;
- taurin;
- tirozin;
- glutamát;
- szerin;
- glutamin;
- ornitin;
- cisztein;
- karnitin
A nem esszenciális aminosavak funkciói
- A cisztein eltávolítja a mérgező anyagokat, részt vesz a bőr- és izomszövetek létrehozásában, valamint természetes antioxidáns.
- A tirozin csökkenti a fizikai fáradtságot, felgyorsítja az anyagcserét, megszünteti a stresszt és a depressziót.
- Az alanin az izomnövekedést szolgálja, és energiaforrás.
- fokozza az anyagcserét és csökkenti az ammóniaképződést erős edzés során.
- A cisztin megszünteti a fájdalmat, ha a szalagok és az ízületek megsérülnek.
- Felelős érte agyi tevékenység, hosszan tartó fizikai aktivitás során glükózzá alakul, energiát termelve.
- A glutamin helyreállítja az izmokat, javítja az immunitást, felgyorsítja az anyagcserét, javítja az agyműködést és növekedési hormont termel.
- A glicin szükséges az izomműködéshez, a zsírlebontáshoz, a vérnyomás és a vércukorszint stabilizálásához.
- A karnitin a zsírsavakat a sejtekbe mozgatja, ahol azok lebomlanak, és energiát szabadítanak fel, ami a felesleges zsír elégetését és energiatermelést eredményez.
- Az ornitin növekedési hormont termel, részt vesz a vizelet képződésében, lebontja a zsírsavakat és segíti az inzulintermelést.
- A prolin biztosítja a kollagén termelődését, szükséges a szalagokhoz és az ízületekhez.
- A szerin javítja az immunitást és energiát termel, ami a gyors anyagcseréhez szükséges zsírsavakés izomnövekedést.
- A taurin lebontja a zsírt, növeli a szervezet ellenálló képességét, és epesókat szintetizál.
A fehérje és tulajdonságai
A fehérjék vagy fehérjék nitrogént tartalmazó, nagy molekulájú vegyületek. A „fehérje” fogalma, amelyet először Berzelius nevezett meg 1838-ban, a görög szóból származik, és jelentése „elsődleges”, ami a fehérjék természetben betöltött vezető szerepét tükrözi. A fehérjék sokfélesége teszi lehetővé a létezést Hatalmas mennyiségűélőlények: a baktériumoktól az emberi szervezetig. Lényegesen több van belőlük, mint más makromolekulákból, mivel a fehérjék az élő sejt alapját képezik. Az emberi test tömegének körülbelül 20%-át, a sejt száraz tömegének több mint 50%-át teszik ki. Ez a sokféle fehérje húsz különböző aminosav tulajdonságaival magyarázható, amelyek kölcsönhatásba lépnek egymással és polimer molekulákat hoznak létre.

A fehérjék kiemelkedő tulajdonsága, hogy képesek önállóan létrehozni egy bizonyos fehérjére jellemző térbeli struktúrát. A fehérjék peptidkötéseket tartalmazó biopolimerek. Mert kémiai összetétel a fehérjék állandó átlagos nitrogéntartalma körülbelül 16%.
Az élet, valamint a test növekedése és fejlődése lehetetlen a fehérje aminosavak új sejteket építő funkciója nélkül. A fehérjék más elemekkel nem helyettesíthetők, szerepük az emberi szervezetben rendkívül fontos.
A fehérjék funkciói
A fehérjék iránti igény a következő funkciókban rejlik:
- szükséges a növekedéshez és fejlődéshez, mivel ez a fő építőanyag az új sejtek létrehozásához;
- szabályozza az anyagcserét, melynek során energia szabadul fel. Az étel elfogyasztása után az anyagcsere sebessége megnövekszik, például ha az étel szénhidrátból áll, az anyagcsere 4% -kal, ha fehérjékből áll - 30% -kal gyorsul;
- szabályozza a szervezetben annak hidrofilitása miatt - a víz vonzásának képessége;
- erősíti az immunrendszert olyan antitestek szintetizálásával, amelyek védenek a fertőzésektől és megszüntetik a betegségek veszélyét.

Termékek - fehérjeforrások
Az emberi izomzat és csontváz élő szövetekből áll, amelyek nemcsak működnek, hanem az élet során megújulnak is. Felépülnek a sérülésekből, és megőrzik erejüket és tartósságukat. Ehhez nagyon speciális tápanyagokra van szükségük. Az élelmiszer biztosítja a szervezet számára az összes folyamathoz szükséges energiát, beleértve az izomműködést, a szövetek növekedését és helyreállítását. A szervezetben lévő fehérjét pedig energiaforrásként és építőanyagként is használják.

Ezért nagyon fontos megfigyelni az élelmiszerekben való napi felhasználását. Fehérjében gazdag ételek: csirke, pulyka, sovány sonka, sertés, marha, hal, garnélarák, bab, lencse, szalonna, tojás, dió. Mindezek a termékek ellátják a szervezetet fehérjével és biztosítják az élethez szükséges energiát.
Az aminosavak szerves amfoter vegyületek. Két ellentétes természetű funkciós csoportot tartalmaznak a molekulában: egy bázikus tulajdonságú aminocsoportot és egy savas tulajdonságú karboxilcsoportot. Az aminosavak savakkal és bázisokkal egyaránt reagálnak:
H2N-CH2-COOH + HCl → Cl [H3N-CH2-COOH],
H 2 N -CH 2 -COOH + NaOH → H 2 N-CH 2 -COONa + H 2 O.
Amikor az aminosavakat vízben oldjuk, a karboxilcsoport eltávolít egy hidrogéniont, amely kapcsolódhat az aminocsoporthoz. Ebben az esetben belső só képződik, amelynek molekulája egy bipoláris ion:
H2N-CH2-COOH + H3N-CH2-COO-.
Az aminosavak sav-bázis átalakulása a különböző környezetekben a következő általános diagrammal ábrázolható:

Az aminosavak vizes oldatai a funkciós csoportok számától függően semleges, lúgos vagy savas környezettel rendelkeznek. Így a glutaminsav savas oldatot képez (két -COOH csoport, egy -NH 2), a lizin lúgos oldatot (egy -COOH csoport, kettő -NH 2).
A primer aminokhoz hasonlóan az aminosavak salétromsavval reagálnak, az aminocsoport hidroxocsoporttá, az aminosav pedig hidroxisavvá alakul:
H 2N-CH(R)-COOH + HNO 2 → HO-CH(R)-COOH + N 2 + H 2 O
A felszabaduló nitrogén mennyiségének mérése lehetővé teszi az aminosav mennyiségének meghatározását ( Van Slyke módszer).
Az aminosavak hidrogén-klorid gáz jelenlétében reagálhatnak alkoholokkal, átalakulva észter(pontosabban az éter hidroklorid sójába):
H 2 N-CH(R)-COOH + R’OH H 2 N-CH(R)-COOR’ + H 2 O.
Az aminosav-észterek nem rendelkeznek bipoláris szerkezettel, és illékony vegyületek.
Az aminosavak legfontosabb tulajdonsága, hogy képesek kondenzálódni peptidekké.
Kvalitatív reakciók.
1) Minden aminosavat ninhidrin oxidál

kék-lila színű termékek képződésével. A prolin iminosav sárga színt ad a ninhidrinnel. Ez a reakció felhasználható aminosavak mennyiségi meghatározására spektrofotometriával.
2) Ha az aromás aminosavakat tömény salétromsavval hevítjük, nitrálódik benzolgyűrűés vegyületek keletkeznek, amelyek színeződnek sárga. Ezt a reakciót nevezik xantoprotein(a görög xanthos szóból - sárga).
Az aminosavak sav-bázis tulajdonságai két ionizálható csoport - karboxil- és aminocsoport - jelenlétével függnek össze, ezért az aminosavak mind a savak, mind a bázisok tulajdonságait mutathatják, pl. amfoter vegyületek. Kristályos állapotban és vizes oldatokban az α-aminosavak bipoláris ionok, más néven ikerionok formájában léteznek. Az ionos szerkezet meghatározza az α-aminosavak néhány tulajdonságát: magas olvadáspont (200-300°C), nem illékonyság, vízben való oldhatóság és nem poláros szerves oldószerekben való oldhatatlanság. Az aminosavak vízben való oldhatósága összefügg a szervezetben való felszívódásukkal és szállításukkal. Az aminosavmolekulák ionizációja az oldat pH-jától függ. A monoamino-monokarbonsavak esetében a disszociációs folyamat a következő formában történik:
Az erősen savas oldatokban az aminosavak pozitív, a lúgos oldatokban negatív ionokként vannak jelen.
Az aminosavak sav-bázis tulajdonságai a Brønsted-Lowry savak és bázisok elmélete alapján magyarázhatók. A teljesen protonált -aminosav (kationos forma) a Brønsted-elmélet szemszögéből egy kétbázisú sav, amely két savcsoportot tartalmaz: egy disszociálatlan karboxilcsoportot (–COOH) és egy protonált aminocsoportot (NH 3), amelyek jellemzői. pK 1 és pK 2 megfelelő értékeivel.
Az aminosavak pK-értékeit a titrálási görbékből határozzuk meg. Tekintsük az alanin titrálási görbéjét (1. ábra).

Rizs. 1 – 0,1 M alanin oldat 0,1 M HCl-oldattal (a) és 0,1 M NaOH-oldattal (b) történő titrálásával kapott görbék.
Az alanin titrálási görbéjéből az következik, hogy a karboxilcsoport pK 1 = 2,34, a protonált aminocsoport pK 2 = 9,69. pH = 6,02-nél az alanin bipoláris ionként létezik, amikor a részecske teljes elektromos töltése 0. Ezen a pH-értéken az alanin molekula elektromosan semleges. Ezt a pH-értéket izoelektromos pontnak nevezzük, és pH et vagy pI jelöléssel. A monoamino-monokarbonsavak esetében az izoelektromos pontot két pK érték számtani átlagaként számítjuk ki. Például az alanin esetében ez egyenlő:
рI= ½(рК 1 + рК 2) = ½(2,34 + 9,69) = 6,02
Az izoelektromos pont feletti pH-értéknél az aminosav negatív töltésű, a pI alatti pH-értéknél pedig az aminosav nettó pozitív töltést hordoz. Például pH = 1,0 esetén az összes alanin molekula ionok formájában létezik

+1 teljes díjjal. pH = 2,34-nél, amikor egyenlő mennyiségű ion keveréke van

teljes töltés = +0,5. Hasonlóképpen megjósolhatja bármely más aminosav teljes töltésének előjelét és nagyságát bármely pH-értéknél.
A gyökben ionizálható csoporttal rendelkező aminosavak összetettebb titrálási görbékkel rendelkeznek, amelyek három szakaszból állnak, amelyek az ionizáció három lehetséges szakaszának felelnek meg, és ezért három pK értékük van (pK 1, pK 2 és pK R). A savas aminosavak, például az aszparaginsav ionizálása a következő egymást követő szakaszokból áll:

Az ilyen aminosavak izoelektromos pontjait is meghatározza a gyök ionizálható csoportjának jelenléte a -amino- és -karboxilcsoportokkal együtt. A monoamino-dikarbonsavak esetében az izoelektromos pontok a savas pH-tartomány felé tolódnak el, és két karboxilcsoport pK-értékei közötti számtani átlagként határozzák meg (pIaszparaginsav = 2,97). Bázikus aminosavak esetén a pI a lúgos régióba tolódik, és két protonált aminocsoport pK-értékei közötti számtani átlagként számítják ki (pIlizin = 9,74).
Az aminosavak sav-bázis tulajdonságait az aminosavak elektroforézissel és ioncserélő kromatográfiával történő elválasztására, majd azonosítására használják. Mindkét módszer a teljes elektromos töltés előjelében és nagyságában mutatkozó különbségeken alapul egy adott pH-érték mellett.
A nitrogéntartalmúak között szerves anyag kettős funkciójú kapcsolatok vannak. Különösen fontosak közülük aminosavak.
Körülbelül 300 különböző aminosav található az élő szervezetek sejtjeiben és szöveteiben, de csak 20 ( α-aminosavak ) egységként (monomerként) szolgálnak, amelyekből minden élőlény peptidjei és fehérjéi épülnek fel (ezért fehérje aminosavak). Ezen aminosavak elhelyezkedésének szekvenciáját a fehérjékben a megfelelő gének nukleotidszekvenciája kódolja. A fennmaradó aminosavak szabad molekulák és kötött formában egyaránt megtalálhatók. Az aminosavak közül sok csak bizonyos szervezetekben található meg, és vannak olyanok is, amelyek csak az egyikben találhatók meg a sokféle leírt organizmus közül. A legtöbb mikroorganizmus és növény szintetizálja a szükséges aminosavakat; Az állatok és az emberek nem képesek előállítani az élelmiszerből nyert, úgynevezett esszenciális aminosavakat. Az aminosavak részt vesznek a fehérjék és szénhidrátok anyagcseréjében, az élőlények számára fontos vegyületek (például a nukleinsavak szerves részét képező purin- és pirimidinbázisok) képzésében, hormonok, vitaminok, alkaloidok, pigmentek részét képezik. , toxinok, antibiotikumok stb.; Egyes aminosavak közvetítőként szolgálnak az idegimpulzusok továbbításában.
Aminosavak- szerves amfoter vegyületek, amelyek karboxilcsoportokat tartalmaznak - COOH és aminocsoportok -NH 2 .
Aminosavak karbonsavnak tekinthetők, amelyek molekuláiban a hidrogénatomot a gyökben aminocsoport helyettesíti.
OSZTÁLYOZÁS
Az aminosavakat szerkezeti jellemzőik szerint osztályozzák.1. Attól függően relatív pozíció amino- és karboxilcsoportok, aminosavak vannak osztva α-, β-, γ-, δ-, ε- stb.
2. A funkciós csoportok számától függően savas, semleges és bázikus csoportokat különböztetünk meg.
3. A szénhidrogén gyök természete alapján megkülönböztetik alifás(zsír), aromás, kéntartalmúÉs heterociklusos aminosavak. A fenti aminosavak a zsíros sorozatba tartoznak.
Az aromás aminosavra példa a para-amino-benzoesav:
A heterociklusos aminosavra példa a triptofán, amely esszenciális α-aminosav.
ELNEVEZÉSTAN
A szisztematikus nómenklatúra szerint az aminosavak neveit a megfelelő savak nevéből alakítják ki az előtag hozzáadásával. aminoés jelzi az aminocsoport elhelyezkedését a karboxilcsoporthoz viszonyítva. A szénlánc számozása a karboxilcsoport szénatomjától.
Például:
Gyakran alkalmaznak egy másik módszert is az aminosavak nevének megalkotására, amely szerint az előtagot hozzáadják a karbonsav triviális nevéhez amino az aminocsoport helyzetét a görög ábécé betűivel jelölve.
Példa:
α-aminosavak esetébenR-CH(NH2)COOH
Amelyek rendkívül fontos szerepet játszanak az állatok és növények életfolyamataiban, triviális elnevezéseket használnak.
Asztal.
|
Aminosav |
Rövidítve kijelölés |
A gyök szerkezete (R) |
|
glicin |
Gly |
H- |
|
Alanin |
Ala (Ala) |
CH 3 - |
|
Valin |
Val |
(CH3)2CH- |
|
Leucin |
lej (lej) |
(CH 3) 2 CH - CH 2 - |
|
Serin |
Ser |
OH-CH2- |
|
Tirozin |
Tyr (lőtér) |
HO – C 6 H 4 – CH 2 – |
|
Aszparaginsav |
Áspiskígyó |
HOOC – CH 2 – |
|
Glutaminsav |
Glu |
HOOC – CH 2 – CH 2 – |
|
cisztein |
Cys (cisz) |
HS – CH 2 – |
|
Aszparagin |
Asn (Asn) |
O = C – CH 2 – │ NH 2 |
|
Lizin |
Lys (Liz) |
NH 2 - CH 2 - CH 2 - CH 2 - |
|
Fenilalanin |
Phen |
C 6 H 5 – CH 2 – |
Ha egy aminosavmolekula két aminocsoportot tartalmaz, akkor az előtagot használják a nevébendiamino-, három NH 2 csoport – triamino- stb.
Példa:
Két vagy három karboxilcsoport jelenlétét az utótag tükrözi a névben -diovy vagy -triinsav:
ISOMERIA
1. A szénváz izomerizmusa
2. A funkciós csoportok helyzetének izomerizmusa
3. Optikai izoméria
α-aminosavak, kivéve a glicin NH 2-CH2-COOH.
FIZIKAI TULAJDONSÁGOK
Az aminosavak magas (250°C feletti) olvadáspontú kristályos anyagok, amelyek az egyes aminosavak között alig különböznek, ezért nem jellemzőek. Az olvadást az anyag bomlása kíséri. Az aminosavak vízben nagyon jól oldódnak, szerves oldószerekben pedig nem oldódnak, ezért hasonlóak a nem aminosavakhoz. szerves vegyületek. Sok aminosav édes ízű.
FOGADÁS
3. Mikrobiológiai szintézis. Ismeretes, hogy a mikroorganizmusok életfolyamataik során a fehérjék α - aminosavait termelik.
KÉMIAI TULAJDONSÁGOK
Az aminosavak amfoter szerves vegyületek, sav-bázis tulajdonságok jellemzik őket.
én . Általános tulajdonságok
1. Intramolekuláris semlegesítés → bipoláris ikerion képződik:
A vizes oldatok elektromosan vezetőképesek. Ezeket a tulajdonságokat az magyarázza, hogy az aminosavmolekulák belső sók formájában léteznek, amelyek egy protonnak a karboxilcsoportból az aminocsoportba való átvitelével jönnek létre:
ikerion
Az aminosavak vizes oldatai a funkciós csoportok számától függően semleges, savas vagy lúgos környezettel rendelkeznek.
ALKALMAZÁS
1) az aminosavak széles körben elterjedtek a természetben;
2) az aminosavmolekulák azok az építőelemek, amelyekből minden növényi és állati fehérje épül; a testfehérjék felépítéséhez szükséges aminosavakat az emberek és az állatok élelmiszerfehérjék részeként nyerik;
3) aminosavakat írnak fel súlyos kimerültségre, súlyos műtétek után;
4) betegek táplálására használják;
5) az aminosavak bizonyos betegségek gyógymódjaként szükségesek (például a glutaminsavat idegbetegségekre, a hisztidint gyomorfekélyre használják);
6) bizonyos aminosavakat használnak fel mezőgazdaságállatok etetésére, amely pozitív hatással van a növekedésükre;
7) technikai jelentőséggel bírnak: az aminokapronsav és az aminoenantsav szintetikus rostokat képez - kapron és enant.
AZ AMINOSAVAK SZEREPÉRŐL
Az aminosavak előfordulása a természetben és biológiai szerepe
A természetben való megtalálás és az aminosavak biológiai szerepe