Halogènes– Éléments du groupe VII – fluor, chlore, brome, iode, astatine (l'astatine a été peu étudiée en raison de sa radioactivité). Les halogènes sont des non-métaux distincts. Seul l'iode présente dans de rares cas des propriétés similaires à celles des métaux.
A l'état non excité, les atomes d'halogène ont une configuration électronique commune : ns2np5. Cela signifie que les halogènes ont 7 électrons de valence, à l'exception du fluor.
Propriétés physiques des halogènes : F2 – gaz incolore et difficile à liquéfier ; Le Cl2 est un gaz jaune-vert, facilement liquéfiable, avec une odeur âcre et suffocante ; Br2 – liquide rouge-brun ; I2 est une substance cristalline violette.

Les solutions aqueuses d'halogénures d'hydrogène forment des acides. HF – fluorure d’hydrogène (fluorure) ; HCl – chlorhydrique (sel); НBr—bromure d'hydrogène ; HI – iodure d’hydrogène. La force des acides diminue de haut en bas. L'acide fluorhydrique est le plus faible de la série des acides halogénés et l'acide iodhydrique est le plus fort. Cela s'explique par le fait que l'énergie de liaison du Hg diminue d'en haut. La force de la molécule NG diminue dans le même sens, ce qui est associé à une augmentation de la distance internucléaire. La solubilité des sels légèrement solubles dans l'eau diminue également :
De gauche à droite, la solubilité des halogénures diminue. AgF est hautement soluble dans l’eau. Tous les halogènes à l'état libre sont des agents oxydants. Leur force en tant qu'agents oxydants diminue du fluor à l'iode. À l’état cristallin, liquide et gazeux, tous les halogènes existent sous forme de molécules individuelles. Les rayons atomiques augmentent dans la même direction, ce qui entraîne une augmentation des points de fusion et d'ébullition. Le fluor se dissocie mieux en atomes que l'iode. Les potentiels des électrodes diminuent lorsque l'on descend dans le sous-groupe halogène. Le fluor a le potentiel d'électrode le plus élevé. Le fluor est l'agent oxydant le plus puissant. Tout halogène libre supérieur déplacera l'halogène inférieur, qui est dans l'état d'un ion négatif à charge unique en solution.
20. Chlore. Chlorure d'hydrogène et acide chlorhydrique
Chlore (Cl) – se situe en 3ème période, dans le groupe VII du sous-groupe principal du système périodique, numéro d'ordre 17, masse atomique 35.453 ; fait référence aux halogènes.
Propriétés physiques: gaz jaune-vert avec une odeur âcre. Densité 3,214 g/l ; point de fusion -101 °C ; point d'ébullition -33,97 °C. À température ordinaire, il se liquéfie facilement sous une pression de 0,6 MPa. En se dissolvant dans l'eau, il forme une eau chlorée jaunâtre. Il est très soluble dans les solvants organiques, notamment l'hexane (C6H14) et le tétrachlorure de carbone.
Propriétés chimiques du chlore : configuration électronique : 1s22s22p63s22p5. Il y a 7 électrons dans le niveau externe. Pour terminer le niveau, vous avez besoin d'un électron, que le chlore accepte, présentant un état d'oxydation de -1. Il existe également des états d'oxydation positifs du chlore jusqu'à + 7. Les oxydes de chlore suivants sont connus : Cl2O, ClO2, Cl2O6 et Cl2O7. Ils sont tous instables. Le chlore est un puissant agent oxydant. Il réagit directement avec les métaux et les non-métaux :
Réagit avec l'hydrogène. Dans des conditions normales, la réaction se déroule lentement, avec un fort échauffement ou un éclairage - avec une explosion, selon un mécanisme en chaîne :
![]()
Le chlore interagit avec les solutions alcalines, formant des sels - hypochlorites et chlorures :
Lorsque le chlore passe dans une solution alcaline, un mélange de solutions de chlorure et d'hypochlorite se forme :
Le chlore est un agent réducteur : Cl2 + 3F2 = 2ClF3.
Interaction avec l'eau :
Le chlore ne réagit pas directement avec le carbone, l'azote et l'oxygène.
Reçu: 2NaCl + F2 = 2NaF + Cl2.
Électrolyse: 2NaCl + 2H2O = Cl2 + H2 + 2NaOH.
Trouver dans la nature : contenu dans les minéraux suivants : halite (sel gemme), sylvite, bischofite ; l'eau de mer contient des chlorures de sodium, de potassium, de magnésium et d'autres éléments.
Chlorure d'hydrogène HCl. Propriétés physiques: gaz incolore, plus lourd que l'air, très soluble dans l'eau pour former d'acide chlorhydrique.
Reçu: dans le laboratoire:
Dans l'industrie : l'hydrogène est brûlé dans un flux de chlore. Ensuite, le chlorure d'hydrogène est dissous dans l'eau pour former de l'acide chlorhydrique (voir ci-dessus).
Propriétés chimiques: l'acide chlorhydrique est fort, monobasique, interagit avec les métaux dans la série de tension jusqu'à l'hydrogène : Zn + 2HCl = ZnCl2 + H2.
En tant qu'agent réducteur, il réagit avec les oxydes et les hydroxydes de nombreux métaux.
DÉFINITION
Halogènes– éléments du groupe VII A – fluor (F), chlore (Cl), brome (Br) et iode (I).
Configuration électronique du niveau d'énergie externe des halogènes ns 2 np 5. Étant donné qu'il ne manque qu'un seul électron aux halogènes avant d'atteindre le niveau d'énergie, ils présentent le plus souvent en ORR les propriétés d'agents oxydants. États d'oxydation des halogènes : de « -1 » à « +7 ». Le seul élément du groupe halogène, le fluor, ne présente qu'un seul état d'oxydation « -1 » et est l'élément le plus électronégatif. Les molécules halogènes sont diatomiques : F 2, Cl 2, Br 2, I 2.
Propriétés chimiques des halogènes
Avec une charge croissante du noyau d'un atome d'un élément chimique, c'est-à-dire lors du passage du fluor à l'iode, la capacité oxydante des halogènes diminue, ce qui est confirmé par la capacité de déplacer les halogènes inférieurs par des halogènes supérieurs à partir des acides halohydriques et de leurs sels :
Br 2 + 2HI = I 2 + 2HBr;
Cl 2 + 2KBr = Br 2 + 2KCl.
Le fluor a la plus grande activité chimique. Majorité éléments chimiques même à température ambiante, interagit avec le fluor, libérant un grand nombre de chaleur. Même l’eau brûle dans le fluor :
2H 2 O + 2F 2 = 4HF + O 2.
Le chlore libre est moins réactif que le fluor. Il ne réagit pas directement avec l'oxygène, l'azote et les gaz rares. Il interagit avec toutes les autres substances comme le fluor :
2Fe + Cl2 = 2FeCl3;
2P + 5Cl 2 = 2PCl 5.
Lorsque le chlore interagit avec l'eau froide, une réaction réversible se produit :
Cl 2 + H 2 O↔HCl + HClO.
Le mélange de produits de réaction est appelé eau chlorée.
Lorsque le chlore interagit avec les alcalis à froid, des mélanges de chlorures et d'hypochlorites se forment :
Cl 2 + Ca(OH) 2 = Ca(Cl)OCl + H 2 O.
Lorsque le chlore est dissous dans une solution alcaline chaude, la réaction suivante se produit :
3Cl 2 + 6KOH = 5KCl + KClO 3 + 3H 2 O.
Le brome, comme le chlore, se dissout dans l'eau et, réagissant partiellement avec lui, forme ce qu'on appelle « l'eau bromée », tandis que l'iode est pratiquement insoluble dans l'eau.
L'activité chimique de l'iode diffère considérablement de celle des autres halogènes. Il ne réagit pas avec la plupart des non-métaux et réagit lentement avec les métaux uniquement lorsqu'ils sont chauffés. L'interaction de l'iode avec l'hydrogène ne se produit qu'avec un fort chauffage ; la réaction est endothermique et hautement réversible :
H 2 + I 2 = 2HI - 53 kJ.
Propriétés physiques des halogènes
Au non. Le fluor est un gaz jaune clair avec une odeur âcre. Toxique. Le chlore est un gaz vert clair, tout comme le fluor, il a une odeur âcre. Très toxique. À pression élevée et à température ambiante, il se transforme facilement en état liquide. Le brome est un liquide lourd de couleur rouge-brun avec une odeur piquante désagréable caractéristique. Le brome liquide, ainsi que ses vapeurs, sont hautement toxiques. Le brome est peu soluble dans l’eau et bien dans les solvants non polaires. L'iode est un solide gris foncé avec un éclat métallique. La vapeur d'iode a violet. L'iode se sublime facilement, c'est-à-dire entre dans état gazeuxà partir d'un solide, tout en contournant l'état liquide.
Production d'halogènes
Les halogènes peuvent être obtenus par électrolyse de solutions ou de fusions d'halogénures :
MgCl 2 = Mg + Cl 2 (fondre).
Le plus souvent, les halogènes sont obtenus par la réaction d'oxydation des acides halohydriques :
MnO 2 + 4HCl = MnCl 2 + Cl 2 + 2H 2 O;
K 2 Cr 2 O 7 + 14HCl = 3Cl 2 + 2KCl + 2CrCl 3 + 7H 2 O ;
2KMnO 4 +16HCl = 2MnCl 2 +5Cl 2 +8H 2 O +2KCl.
Application d'halogènes
Les halogènes sont utilisés comme matières premières pour fabriquer divers produits. Ainsi, le fluor et le chlore sont utilisés pour la synthèse de divers matériaux polymères ; le chlore est également une matière première dans la production d'acide chlorhydrique. Brome et iode trouvés large application en médecine, le brome est également utilisé par l’industrie des peintures et vernis.
Exemples de résolution de problèmes
EXEMPLE 1
| Exercice | Calculer le volume de chlore (n°) qui a réagi avec l'iodure de potassium si de l'iode pesant 508 g s'est formé | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solution | Écrivons l'équation de la réaction entre le chlore et l'iodure de potassium : Cl 2 + 2KI = I 2 + 2KCl Masse molaire de l'iode, calculée à l'aide du tableau des éléments chimiques de D.I. Mendeleev, égal à – 254 g/mol. Trouvons la quantité d'iode formée : v(Je 2) = m(Je 2)/M(Je 2) À, ouvert en 1940
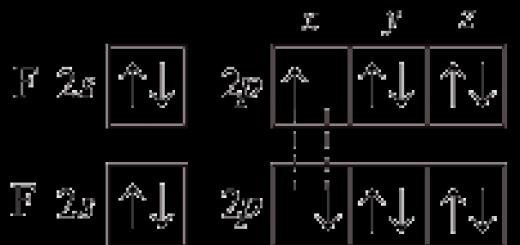
La distribution des orbitales électroniques dans la couche électronique externe de tous les halogènes est du même type
Ils ont beaucoup de points communs dans la structure des atomes et des molécules. Ils terminent la construction R.-coquilles de la couche externe, elles appartiennent donc toutes au nombre d'éléments p. Il manque un électron à la couche électronique externe des atomes d'halogène, de sorte que l'électronégativité de ces éléments est prononcée et, dans les réactions redox, ils se comportent principalement comme des agents oxydants. ■ 1. Comment le rayon atomique change-t-il en fonction de l'augmentation de la charge du noyau atomique ?
Propriétés physiques des halogènesToutes les propriétés des halogènes, tant physiques que chimiques, dépendent de la structure des atomes de l’élément. Ces propriétés des différents halogènes sont largement similaires, mais en même temps, chaque halogène possède un certain nombre de caractéristiques. ■ 7. Comment l'intensité de la couleur des halogènes change-t-elle avec l'augmentation des charges nucléaires ?
10. Compilez et remplissez le tableau « Propriétés physiques des halogènes » selon le modèle suivant :
Effet physiologique des halogènesTous sont toxiques par leurs effets physiologiques. Le fluorure est particulièrement toxique : lorsqu'il est inhalé en petites quantités, il provoque un œdème pulmonaire, et en grande quantité, il provoque la destruction du tissu pulmonaire et la mort. Iode Le moins toxique de tous les halogènes. L'inhalation de vapeurs d'iode lorsqu'elles sont chauffées peut provoquer une intoxication, mais il est rare de travailler avec de l'iode sous forme de vapeur, par exemple pour le purifier par sublimation. L'iode cristallin ne doit pas être pris avec les mains, car s'il entre en contact avec la peau, il provoque l'apparition de taches jaunes caractéristiques. Tous les travaux avec des halogènes doivent être effectués sous une sorbonne. Notez dans votre cahier les précautions de sécurité pour travailler avec des halogènes et les premiers secours en cas d'empoisonnement. Propriétés chimiques des halogènes
De par la nature de leurs propriétés chimiques, comme indiqué ci-dessus, tous les halogènes sont des non-métaux typiques dotés d'une électronégativité significative. L'élément le plus électronégatif avec la plus grande activité non métallique est le fluor, le moins actif est l'iode. Riz. 21. Combustion de l'hydrogène dans le chlore. 1- chlore 2- Interaction des halogènes avec des substances simples. Vous pouvez retracer la diminution de l'activité chimique du fluor au chlore à l'aide d'exemples de différentes réactions. L'interaction de divers halogènes avec l'hydrogène est particulièrement intéressante. Leurs conditions de réaction sont différentes. Le fluorure est le composé le plus durable parmi les halogénures d'hydrogène. Avec l'hydrogène, le brome forme du bromure d'hydrogène.
Les halogènes présentent également des propriétés oxydantes lorsqu’ils interagissent avec les métaux, qui sont généralement très actifs. Riz. 22. Par exemple. Cu + Cl2 = CuСl2 Ici, en réaction avec le chlore, il présente un état d'oxydation égal à +3 - Fe +3, et égal à +2 - Cu +2. Dans tous les cas ci-dessus, le chlore se comporte comme. Chimie des éléments Non-métaux du sous-groupe VIIA Les éléments du sous-groupe VIIA sont des non-métaux typiques à haute teneur électronégativité, ils ont un nom de groupe - « halogènes ». Principales questions abordées lors de la conférence Caractéristiques générales des non-métaux du sous-groupe VIIA. Structure électronique, les caractéristiques les plus importantes des atomes. L'étape la plus caractéristique pénalités d’oxydation. Caractéristiques de la chimie des halogènes. Substances simples. Composés naturels. Composés halogènes Acides halohydriques et leurs sels. Sel et acide fluorhydrique créneaux horaires, reçu et demande. Complexes halogénures. Binaire composés d'oxygène halogènes. Instabilité env. Propriétés redox des substances simples et co- unités. Réactions de disproportion. Diagrammes de Latimer.
Chimie des éléments du sous-groupe VIIA caractéristiques générales
Le groupe VIIA est formé d'éléments p : fluor F, chlore Cl, brome Br, iode I et astate At. La formule générale des électrons de valence est ns 2 np 5. Tous les éléments du groupe VIIA sont des non-métaux typiques.
pour la formation d'une coque stable à huit électrons des boîtes, c'est pourquoi ils ont il y a une forte tendance à ajout d'un électron. Tous les éléments forment facilement une simple charge unique ny anions G – . Sous forme d'anions simples, les éléments du groupe VIIA se trouvent dans l'eau naturelle et dans les cristaux de sels naturels, par exemple l'halite NaCl, la sylvite KCl, la fluorite. CaF2. Nom général du groupe des éléments VIIA- Le groupe « halogènes », c'est-à-dire « donnant naissance à des sels », est dû au fait que la plupart de leurs composés avec des métaux sont pré- constitue sels typiques(CaF2, NaCl, MgBr2, KI), co- qui peut être obtenu par interaction directe interaction du métal avec l'halogène. Les halogènes libres sont obtenus à partir de sels naturels, c'est pourquoi le nom « halogènes » est également traduit par « nés de sels ».
L'état d'oxydation minimum (–1) est le plus stable pour tous les halogènes. Certaines caractéristiques des atomes des éléments du groupe VIIA sont données dans Les caractéristiques les plus importantes des atomes des éléments du groupe VIIA
Les halogènes ont une affinité électronique élevée (maximum à Cl) et une énergie d'ionisation très élevée (maximale à F) et maximale électronégativité possible à chaque période. Le fluor est le plus électronégatif de tous les éléments chimiques. La présence d'un électron non apparié dans les atomes d'halogène détermine représente l'union des atomes de substances simples en molécules diatomiques Г2. Pour les substances simples, les halogènes, les agents oxydants les plus caractéristiques sont propriétés, qui sont les plus fortes en F2 et s’affaiblissent lors du passage à I2. Les halogènes se caractérisent par la plus grande réactivité de tous les éléments non métalliques. Le fluor, même parmi les halogènes, se démarque a une activité extrêmement élevée. L'élément de la deuxième période, le fluor, diffère le plus fortement des autres autres éléments du sous-groupe. Il s’agit d’un modèle général pour tous les non-métaux.
Le fluor, élément le plus électronégatif, ne montre pas de sexe états d'oxydation résidents. Dans tous les cas, y compris avec le ki- l'oxygène, le fluor est à l'état d'oxydation (-1). Tous les autres halogènes présentent des degrés d'oxydation positifs leniya jusqu'à un maximum de +7. Les états d'oxydation les plus caractéristiques des halogènes : F : -1, 0 ; Cl, Br, I : -1, 0, +1, +3, +5, +7. Cl possède des oxydes connus dans lesquels il se trouve dans des états d'oxydation : +4 et +6. Les composés halogènes les plus importants, dans les états positifs, Les pénalités d'oxydation sont les acides contenant de l'oxygène et leurs sels. Tous les composés halogènes dans des états d'oxydation positifs sont sont des agents oxydants puissants. terrible degré d'oxydation. La disproportion est favorisée par un environnement alcalin. Application pratique de substances simples et de composés oxygénés La réduction des halogènes est principalement due à leur effet oxydant. Le plus large utilisation pratique trouver des substances simples Cl2 et F2. La plus grande quantité le chlore et le fluor sont consommés dans l'industrie synthèse organique : dans la production de plastiques, de réfrigérants, de solvants, pesticides, médicaments. Des quantités importantes de chlore et d'iode sont utilisées pour obtenir des métaux et pour leur raffinage. Le chlore est également utilisé pour blanchir la cellulose, pour la désinfection boire de l'eau et en production eau de Javel et acide chlorhydrique. Les sels d'oxoacides sont utilisés dans la production d'explosifs.
Les acides – acides chlorhydrique et fondu – sont largement utilisés dans la pratique. Le fluor et le chlore font partie des vingt éléments les plus courants là-bas, il y a beaucoup moins de brome et d’iode dans la nature. Tous les halogènes se trouvent dans la nature dans des états d'oxydation(-1). Seul l'iode se présente sous forme de sel KIO3, qui est inclus comme impureté dans le salpêtre chilien (KNO3). L'astatine est un élément radioactif produit artificiellement (il n'existe pas dans la nature). L'instabilité de At se reflète dans le nom, qui vient du grec. "astatos" - "instable". L'astate est un émetteur pratique pour la radiothérapie des tumeurs cancéreuses. Substances simples Les substances simples des halogènes sont formées de molécules diatomiques G2. Dans les substances simples, lors du passage de F2 à I2 avec augmentation du nombre d'électrons couches de trône et augmentation de la polarisabilité des atomes, il y a une augmentation interaction intermoléculaire, conduisant à un changement dans la co- debout dans des conditions standard. Le fluor (dans des conditions normales) est un gaz jaune, à –181°C il se transforme en état liquide. Le chlore est un gaz jaune-vert qui se transforme en liquide à –34°C. De couleur ha- Le nom Cl lui est associé, il vient du grec « chloros » - « jaune- vert". Une forte augmentation du point d'ébullition du Cl2 par rapport au F2, indique une interaction intermoléculaire accrue. Le brome est un liquide rouge foncé très volatil qui bout à 58,8°C. le nom de l'élément est associé à l'odeur forte et désagréable du gaz et est dérivé de "bromos" - "malodorant". Iode – cristaux violet foncé, avec un léger « métallique » des grumeaux qui, lorsqu'ils sont chauffés, se subliment facilement en formant des vapeurs violettes ;
Le point d'ébullition de l'iode est de 183°C. Son nom vient de la couleur de la vapeur d'iode - "iodos" - "violet". Toutes les substances simples ont une odeur âcre et sont toxiques. L'inhalation de leurs vapeurs provoque une irritation des muqueuses et des organes respiratoires, et à des concentrations élevées, une suffocation. Durant la Première Guerre mondiale, le chlore était utilisé comme agent toxique. Le fluor gazeux et le brome liquide provoquent des brûlures cutanées. Travailler avec ha- logens, des précautions doivent être prises. Puisque les substances simples des halogènes sont formées de molécules non polaires refroidit, ils se dissolvent bien dans les solvants organiques non polaires : alcool, benzène, tétrachlorure de carbone, etc. Le chlore, le brome et l'iode sont peu solubles dans l'eau ; leurs solutions aqueuses sont appelées eau de chlore, de brome et d'iode. Br2 se dissout mieux que les autres, concentration de brome en sat. La solution atteint 0,2 mol/l et le chlore – 0,1 mol/l. Le fluorure décompose l'eau : 2F2 + 2H2O = O2 + 4HF Les halogènes présentent une activité et une transition oxydatives élevées en anions halogénures. Г2 + 2e– 2Г– Le fluor a une activité oxydante particulièrement élevée. Le fluor oxyde les métaux nobles (Au, Pt). Pt + 3F2 = PtF6 Il interagit même avec certains gaz inertes (krypton, xénon et radon), par exemple, Xe + 2F2 = XeF4 Dans l'ambiance F2, beaucoup de très connexions stables, Par exemple, eau, quartz (SiO2). SiO2 + 2F2 = SiF4 + O2
Dans les réactions avec le fluor, même des agents oxydants aussi puissants que l'azote et le soufre l'acide nique, agissent comme agents réducteurs, tandis que le fluor oxyde l'entrée contenant O(–2) dans leur composition. 2HNO3 + 4F2 = 2NF3 + 2HF + 3O2 H2 SO4 + 4F2 = SF6 + 2HF + 2O2 La grande réactivité de F2 crée des difficultés dans le choix des composants. matériaux de structure pour travailler avec. Habituellement, à ces fins, nous utilisons Il existe du nickel et du cuivre qui, une fois oxydés, forment à leur surface des films protecteurs denses de fluorures. Le nom F est dû à son action agressive. Je mange, ça vient du grec. "fluoros" – "destructeur". Dans la série F2, Cl2, Br2, I2, le pouvoir oxydant s'affaiblit en raison d'une augmentation augmenter la taille des atomes et diminuer l’électronégativité. DANS solutions aqueuses propriétés oxydantes et réductrices du ver- Les substances sont généralement caractérisées à l'aide de potentiels d'électrode. Le tableau montre les potentiels d'électrode standard (Eo, V) pour les demi-réactions de réduction formation d'halogènes. A titre de comparaison, la valeur Eo pour ki- le carbone est l’agent oxydant le plus courant. Potentiels d'électrode standard pour les substances halogènes simples
Activité oxydative réduite Comme le montre le tableau, F2 est un agent oxydant beaucoup plus puissant, que l'O2, donc F2 n'existe pas dans les solutions aqueuses , il oxyde l'eau, revenir à F–. A en juger par la valeur E®, le pouvoir oxydant du Cl2
également supérieure à celle de l'O2. En effet, lors du stockage à long terme de l’eau chlorée, celle-ci se décompose avec dégagement d’oxygène et formation de HCl. Mais la réaction est lente (la molécule Cl2 est sensiblement plus forte que la molécule F2 et l'énergie d'activation pour les réactions avec le chlore est plus élevée), la dispro- portionnement : Cl2 + H2 O HCl + HOCl Dans l'eau, il n'atteint pas la fin (K = 3,9, 10–4), donc le Cl2 existe dans les solutions aqueuses. Br2 et I2 se caractérisent par une stabilité encore plus grande dans l'eau. La dismutation est une oxydation très caractéristique. réaction de réduction des halogènes. Disproportion de l'amplification se verse dans un environnement alcalin. La dismutation du Cl2 dans les alcalis conduit à la formation d'anions Cl– et ClO–. La constante de disproportion est de 7,5. 1015. Cl2 + 2NaOH = NaCl + NaClO + H2O Lorsque l'iode est disproportionné dans l'alcali, I– et IO3– se forment. Ana- Logiquement, Br2 disproportionne l'iode. Le changement de produit est disproportionné nation est due au fait que les anions GO– et GO2– dans Br et I sont instables. La réaction de dismutation du chlore est utilisée dans l'industrie capacité à obtenir un oxydant hypochlorite puissant et à action rapide, chaux décolorante, sel de bertholet. 3Cl2 + 6 KOH = 5KCl + KClO3 + 3H2 O
Interaction des halogènes avec les métaux Les halogènes réagissent vigoureusement avec de nombreux métaux, par exemple : Mg + Cl2 = MgCl2 Ti + 2I2 TiI4 Halogénures Na +, dans lesquels le métal a un faible état d'oxydation (+1, +2), - Ce sont des composés de type sel avec des liaisons principalement ioniques. Comment voilà, les halogénures ioniques sont des solides avec un point de fusion élevé Halogénures métalliques, dans lesquels le métal a haut degré oxydation Les composés sont des composés avec des liaisons principalement covalentes. Beaucoup d'entre eux sont des gaz, des liquides ou sont fusibles dans des conditions normales. solides. Par exemple, WF6 est un gaz, MoF6 est un liquide, TiCl4 est liquide. Interaction des halogènes avec les non-métaux Les halogènes interagissent directement avec de nombreux non-métaux : hydrogène, phosphore, soufre, etc. Par exemple : H2 + Cl2 = 2HCl 2P + 3Br2 = 2PBr3 S + 3F2 = SF6 La liaison dans les halogénures non métalliques est principalement covalente. Généralement, ces composés ont des points de fusion et d’ébullition bas. Lors du passage du fluor à l'iode, le caractère covalent des halogénures augmente. Les halogénures covalents des non-métaux typiques sont composés acides; lorsqu'ils interagissent avec l'eau, ils s'hydrolysent pour former des acides. Par exemple: PBr3 + 3H2 O = 3HBr + H3 PO3 PI3 + 3H2O = 3HI + H3 PO3 PCl5 + 4H2O = 5HCl + H3 PO4
Les deux premières réactions sont utilisées pour produire du brome et de l'iodure d'hydrogène. acide noique. Interhalogénures. Les halogènes, se combinant les uns avec les autres, forment des interg- conduit. Dans ces composés, l’halogène le plus léger et le plus électronégatif est à l’état d’oxydation (-1), et le plus lourd est à l’état positif. pénalités d’oxydation. En raison de l'interaction directe des halogènes lors du chauffage, on obtient : ClF, BrF, BrCl, ICl. Il existe également des interhalogénures plus complexes : ClF3, BrF3, BrF5, IF5, IF7, ICl3. Tous les interhalogénures dans des conditions normales sont des substances liquides avec basses températuresébullition. Les interhalogénures ont une activité oxydante élevée activité. Par exemple, des substances chimiquement stables telles que SiO2, Al2 O3, MgO, etc. brûlent dans les vapeurs de ClF3. 2Al2 O3 + 4ClF3 = 4 AlF3 + 3O2 + 2Cl2 Le Fluorure ClF 3 est un réactif fluoré agressif qui agit rapidement cour F2. Il est utilisé dans synthèses organiques et pour obtenir des films protecteurs à la surface des équipements en nickel pour travailler avec du fluor. Dans l'eau, les interhalogénures s'hydrolysent pour former des acides. Par exemple, ClF5 + 3H2O = HClO3 + 5HF Halogènes dans la nature. Obtention de substances simples Dans l'industrie, les halogènes sont obtenus à partir de leurs composés naturels. Tous les procédés d'obtention d'halogènes libres sont basés sur l'oxydation de l'halogène Ions Nid. 2Г – Г2 + 2e– Une quantité importante d'halogènes se trouve dans eaux naturelles sous forme d'anions : Cl–, F–, Br–, I–. DANS eau de mer peut contenir jusqu'à 2,5 % de NaCl. Le brome et l'iode sont obtenus à partir de l'eau puits de pétrole et l'eau de mer.
Structure et propriétés des atomes. Éléments du sous-groupe principal du groupe VII Tableau périodique D.I. Mendeleev, réunis sous le nom général d'halogènes - fluor F, chlore Cl, brome Br, iode I, astate At (rarement trouvé dans la nature) - sont des non-métaux typiques. Cela est compréhensible, car leurs atomes contiennent à l'extérieur niveau d'énergie sept électrons et ils n’ont besoin que d’un seul électron pour le compléter. Les atomes d'halogène, lorsqu'ils interagissent avec les métaux, acceptent un électron des atomes métalliques. Dans ce cas, il se pose liaison ionique et des sels se forment. C'est de là que ça vient Nom commun sous-groupes « halogènes », c'est-à-dire « donnant naissance à des sels ». Les halogènes sont des agents oxydants très puissants. Fluorure dans réactions chimiques ne présente que des propriétés oxydantes et se caractérise uniquement par l'état d'oxydation -1 des composés. Les halogènes restants présentent également des propriétés réductrices lorsqu'ils interagissent avec des éléments plus électronégatifs - fluor, oxygène, azote. Leurs états d'oxydation peuvent prendre les valeurs +1, +3, +5, +7. Les propriétés réductrices des halogènes augmentent du chlore à l'iode, ce qui est associé à une augmentation des rayons de leurs atomes : les atomes de chlore sont environ une fois et demie plus petits que l'iode. Les halogènes sont des substances simples. Tous les halogènes existent à l'état libre sous forme de molécules diatomiques avec une liaison covalente non polaire. liaison chimique entre les atomes. A l'état solide, F 2, Cl 2, Br 2, I 2 ont des molécules réseaux cristallins, ce que confirme leur propriétés physiques(Tableau 7). Tableau 7
Comme on peut le constater, avec l'augmentation masse moléculaire les halogènes, leurs points de fusion et d'ébullition augmentent (Fig. 88), la densité augmente : le fluor et le chlore sont des gaz, le brome est un liquide, l'iode est un solide.
Riz. 88. Cela est dû au fait qu'à mesure que la taille des atomes et des molécules d'halogène augmente (Fig. 89), les forces d'interaction intermoléculaire entre eux augmentent également.
Riz. 89. De F 2 à I 2, l'intensité de la couleur des halogènes augmente. Les cristaux d'iode ont un éclat métallique. L'activité chimique des halogènes, comme celle des non-métaux, s'affaiblit du fluor à l'iode. Chaque halogène est l'agent oxydant le plus puissant de sa période. Les propriétés oxydantes des halogènes se manifestent clairement lorsqu'ils interagissent avec les métaux. Dans ce cas, comme vous le savez déjà, des sels se forment. Ainsi, le fluor réagit déjà dans des conditions normales avec la plupart des métaux et, lorsqu'il est chauffé, il réagit également avec l'or, l'argent et le platine, connus pour leur passivité chimique. L'aluminium et le zinc s'enflamment dans une atmosphère de fluor :
Les halogènes restants réagissent avec les métaux principalement lorsqu'ils sont chauffés. Ainsi, dans un ballon rempli de chlore, des cristaux d'antimoine broyés s'enflamment et brûlent magnifiquement (Fig. 90), formant un mélange de deux chlorures d'antimoine (III) et (V) :
Riz. 90. La poudre de fer chauffée s'enflamme également lorsqu'elle réagit avec le chlore. L'expérience peut également être réalisée avec de l'antimoine, mais seule la limaille de fer doit d'abord être chauffée dans une cuillère en fer, puis versée par petites portions dans un ballon contenant du chlore. Le chlore étant un oxydant puissant, la réaction entraîne la formation de chlorure de fer (III) (Fig. 91) :
Riz. 91. Un fil de cuivre chauffé au rouge brûle dans des vapeurs de brome :
L'iode oxyde les métaux plus lentement, mais en présence d'eau, qui est un catalyseur, la réaction de l'iode avec la poudre d'aluminium se déroule très violemment :
La réaction s'accompagne du dégagement de vapeurs d'iode violettes (pourquoi ?). La diminution des propriétés oxydantes et l'augmentation des propriétés de réduction des halogènes du fluor à l'iode peuvent également être jugées par leur capacité à se déplacer les uns les autres des solutions salines.
Riz. 92. Le brome libre déplace l'iode des sels :
Cette réaction n'est pas typique du fluor, car elle se produit en solution et le fluor interagit avec l'eau, en déplaçant l'oxygène :
L'oxygène joue ici le rôle inhabituel d'agent réducteur. C'est peut-être le seul cas où l'oxygène dans une réaction de combustion n'est pas l'une des substances de départ, mais son produit. L'affaiblissement des propriétés oxydantes des halogènes du fluor à l'iode se manifeste clairement lorsqu'ils interagissent avec l'hydrogène. L’équation de cette réaction peut s’écrire sous la forme générale : N 2 + G 2 = 2NG (G - conditionnel désignation chimique halogènes). Si le fluor réagit avec l'hydrogène dans n'importe quelles conditions avec une explosion, alors un mélange de chlore et d'hydrogène ne réagit avec une explosion que lorsqu'il est enflammé ou directement irradié. lumière du soleil, le brome réagit avec l'hydrogène lorsqu'il est chauffé et sans explosion. Ces réactions sont exothermiques. La réaction du composé d'iode cristallin avec l'hydrogène est faiblement endothermique ; elle se déroule lentement même lorsqu'elle est chauffée. À la suite de ces réactions, il se forme respectivement du fluorure d'hydrogène HF, du chlorure d'hydrogène HCl, du bromure d'hydrogène HBr et de l'iodure d'hydrogène HI. Découverte des halogènes. Le fluor sous forme libre a été obtenu pour la première fois en 1886 par le chimiste français A. Moissan, qui a été récompensé pour cette prix Nobel. L'élément tire son nom du grec fluoros - « destructeur ». Le chlore a été découvert par le chimiste suédois K. Scheele en 1774. L'élément doit son nom à sa couleur. substance simple(du grec chloros - jaune-vert). Le brome a été découvert en 1826 par le chimiste français A. Balard. L'élément doit son nom à l'odeur d'une substance simple (du grec bromos - fétide). L'iode a été obtenu en 1811 par le scientifique français B. Courtois et tire son nom de la couleur des vapeurs d'une substance simple (du grec iodes - violet). Nouveaux mots et concepts
Missions pour travail indépendant
Lire aussi : | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||