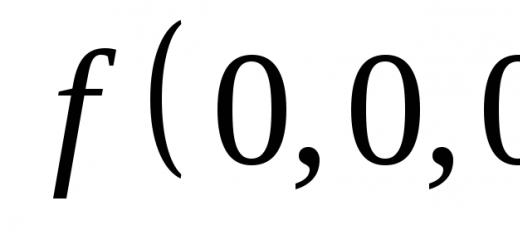کلمه "شیمی" چه ارتباط مثبت و منفی را در شما برمی انگیزد؟
تو چی میدونی
در مورد شیمی؟
مثبت
منفی
آیا می توان لیست "منفی ها" را کاهش داد؟

آیا شما شخصا نیاز به مطالعه شیمی دارید؟
آیا انسان امروز می تواند بدون دانش شیمی کار کند؟



در درس های شیمی یاد خواهید گرفت
- واکنش های شیمیایی چیست؟
- انواع واکنش های شیمیایی چیست؟
- چه چیزی سرعت یک واکنش شیمیایی را تعیین می کند؟
- و خیلی بیشتر …

ما در احاطه بدن فیزیکی زندگی می کنیم.
اجسام فیزیکی از چه چیزی ساخته شده اند؟
هر ماده ای خواص مشخصه خود را دارد.
خواص ماده –
ویژگی هایی که با آن یک ماده با ماده دیگر متفاوت است.
هر مورد، هر موجود زندهدانشمندان آن را جسم می نامند.

تمرین 1 (دو نفره کار کنید)
آلومینیوم
ناخن - میخ
جام
زنجیر
دانه برف
کارامل
سیم
کوه یخ

وظیفه 2
از لیست ارائه شده، مواد و اجسام فیزیکی را به طور جداگانه انتخاب کنید:
اکسیژن، آجر، آب، خط کش، سکه، شیشه، جیوه، سیم، آهن، هیزم، گوگرد، شکر، قلم.

بدن چه نام دارد؟
تفاوت جسم و ماده چیست؟
اجسام چه خواصی دارند؟
مواد چه خواصی دارند؟
مواد چیست؟

یاد آوردن
هر چیزی که ما را احاطه کرده است
این بدن های فیزیکی ,
و اجسام فیزیکی از چه چیزهایی تشکیل شده اند -
این مواد

خواص مواد
فیزیکی
شیمیایی
واکنش های یک ماده معین با مواد دیگر
- وضعیت تجمع
- رنگ
- طعم و مزه
- بو
- درخشش
- رسانایی حرارتی و الکتریکی
- انحلال پذیری در آب
- تراکم
- جوش، نقطه ذوب

وظیفه 3 (دو نفره کار کنید)
"ماده را حدس بزنید و خواص آن را توصیف کنید."
4-البته خیلی نیاز دارم. شما نمی توانید بدون من شام بپزید، خیار ترشی نمیشه کرد شما نمی توانید گوشت ژله ای را مزه دار کنید. اما نه تنها در غذا - من در آب دریا زندگی می کنم. اگر اشکی از چشمت جاری شد، شما فوراً سلیقه من را به یاد خواهید آورد. زودباورها می گویند: ...
5. معمولاً مانند آرد سفید است ید مرا آبی می کند. اما چقدر از آب جوش می ترسم! در آن من بلافاصله ... چسب خواهم شد
6. من پودر خاکستری هستم، در حال حاضر خانه من یک کیف است. کمی آب می خورم و در همان لحظه من فورا سفت خواهم شد. من - …
1. من به شما اطلاع می دهم: من عجله دارم! من زندگی می کنم در حالی که می نویسم. کل تخته را سفید کرد
2. من می روم برای یک سکه کوچک من عاشق زنگ زدن هستم، برای این کار یادبودی برای من برپا می کنند، و آنها می دانند: نام من ...
3. من از خاک رس معمولی ساخته شده ام، اما من فوق العاده مدرن هستم. من از برق گرفتگی نمی ترسم بی باک در هوا پرواز می کنم؛ من در آشپزخانه بدون مهلت خدمت می کنم - من می توانم از عهده تمام وظایف برآیم. من به نام خودم افتخار می کنم: اسم من هست...
من در حال ناپدید شدن هستم. من بودم...

امروزه تعداد مواد از 18 میلیون فراتر رفته است.
در فرآیند دگرگونی ها (در آینده آنها را واکنش های شیمیایی می نامیم)، برخی از مواد قادر به تبدیل شدن به مواد دیگر هستند.



شیمی است
چرا باید خواص برخی مواد را بدانید؟
علم مواد، خواص آنها، تبدیل مواد و پدیده های همراه با این دگرگونی ها
شیمی چیست؟
خواص
ترکیب
کاربرد
یاد آوردن


مبنای مطالعه درس شیمی می باشد
مواد از چه چیزی تشکیل شده اند؟
اتمی - نظریه مولکولی
ماده - مولکول - اتم

اتم -
کوچکترین ذره غیر قابل تقسیم شیمیایی
نوع خاصی از اتم نامیده می شود
عنصر شیمیایی
بیش از 118 نوع اتم وجود دارد که مواد را تشکیل می دهند
بیشتر شناخته شده است 118 نوع اتم بنابراین وجود دارد و بیشتر 118 عنصر شیمیایی

اشکال وجود یک عنصر شیمیایی
عنصر شیمیایی
ساده
مجتمع
در دسترس
اتم ها
مواد
مواد
اتم های هیدروژن
مولکول های هیدروژن
اتم های هیدروژن در یک مولکول آب

مواد
ساده
مجتمع
مواد
مواد
موادی که توسط اتم های یک عنصر شیمیایی تشکیل می شوند
موادی که توسط اتم های مختلف تشکیل می شوند عناصر شیمیایی

سوالات:
شیمی چه چیزی را مطالعه می کند؟
بدن فیزیکی چیست؟
ماده چیست؟
امروز در کلاس چه چیز جدیدی یاد گرفتید؟
موادی را که می شناسید نام ببرید.
چند مثال از اجسام فیزیکی بیاورید.

به بیانیه گوش دهید و مطرح کنید دست راست، اگر صحبت می کنیم موضوع سادهو سمت چپ - اگر در مورد یک عنصر باشد:
هوا حاوی 21 درصد اکسیژن (حجمی) است.
یک مولکول آمونیاک از نیتروژن و هیدروژن تشکیل شده است
آهن قابلیت مغناطیسی شدن را دارد
اکسیژن از احتراق پشتیبانی می کند
آهن بخشی از هموگلوبین است
گوگرد زرد
شیمیایی
ساده
عنصر
ماده

مشق شب
درس شیمی پایه هشتم
(درس مقدماتی)
ملاقات: شیمی!
"شیمی جذابیت مقاومت ناپذیری دارد
به لطف قدرت عظیم و نامحدودی که
به کسانی که آن را می دانند عطا می کند.»
دبلیو کالینز هدف: توسعه دهید علاقه شناختیبرای دانش آموزان پایه هشتم درس شیمی.وظایف:
آشنایی دانش آموزان با تاریخچه توسعه شیمی، ارائه اولین ایده ها در مورد این علم؛
برای به روز رسانی دانش دانش آموزان در مورد مواد، شروع به ایجاد ایده در مورد خواص مواد و تبدیل آنها.
توسعه دهید مهارت های تحلیلیدانش آموزان.
تجهیزات.روزنامه دیواری موضوعی، کارت هایی با فرمول مواد و واکنش های شیمیایی، بشر، فلاسک های ته صاف، یک پارچ شیشه ای تیره، کبریت، سوخت خشک، میز نمایش، انبر بوته، دستمال، بوته چینی، مجموعه ای از فلزات و پلاستیک ها.مواد: محلول های تازه تهیه شده از یدید پتاسیم و استات سرب، فنل فتالئین، خاکستر سودا، هیدروژن سولفات سدیم، اتانول، قرص نورسولفازول، دی کرومات آمونیوم.
در طول کلاس هامن . سخنرانی افتتاحیه معلم
در جهان علم وجود دارد که بدون آن امروزه تحقق خارق العاده ترین پروژه ها و رویاهای افسانه ای غیرممکن است. این- علم شیمی. او معجزات زیادی در مجموعهاش دارد که خیالپردازیهای بهترین داستاننویسان جهان را در مقایسه کمرنگ میکند: انگار سیندرلا را به یک شاهزاده خانم تبدیل میکند، گرافیت را به الماس درخشان تبدیل میکند، به کاغذ استحکام فلز میدهد و حافظه فلزی میبخشد. بیهوده نیست که آنها او را جادوگر و زن شگفت انگیز می نامند: او تغذیه می کند، آب می دهد، لباس می پوشد، شفا می دهد، می شویید، مواد معدنی را استخراج می کند، به شما اجازه می دهد به فضا برید و در ته اقیانوس غرق شوید.
هر یک از شما بدون اینکه بدانید هر روز بدون اینکه از خانه خارج شوید واکنش های شیمیایی انجام می دهید: روشن کردن کبریت و گاز، تهیه غذا. و بدن انسان خود یک کارخانه شیمیایی بزرگ است که در آن واکنش های شیمیایی زیادی رخ می دهد.
امروز اولین آشنایی شما با این علم شگفت انگیز است. این سخنرانی توسط دانش آموزان پایه نهم ارائه خواهد شد. آنها در مورد تاریخچه توسعه علم شیمی به شما خواهند گفت، چیزهای زیادی به شما نشان می دهند آزمایش های جالبو در پایان درس، با پاسخ به سوالات مسابقه، می توانید بلیط قطار سریع السیر را خریداری کنید که شما را به پهنه های وسیع سیاره می برد.شیمی - 8.
II. یادگیری مطالب جدید. نمایش آزمایشات اولین مجریدر کلاس هشتم شروع به مطالعه یک موضوع جدید برای خود می کنید.علم شیمی -علم مواد و تبدیل آنهاهمه مواد اطراف ما از عناصر شیمیایی تشکیل شده اند که در حال حاضر بیش از 110 مورد از آنها وجود دارد. وقتی با هم ترکیب شوند، اتم های عناصر مختلف بیش از بیست میلیون ماده را تشکیل می دهند.
شناخت خواص مواد برای یافتن کاربرد آنها ضروری است. بله، مال ماست اجداد دور، از سختی فوق العاده سیلیکون قدردانی کرد و از آن برای ساخت سلاح و ابزار استفاده کرد. شما قبلاً برخی از مواد را می شناسید: آهن، آلومینیوم، آب، گچ، شکر، اکسیژن، دی اکسید کربن، پلاستیک و غیره (نمایش مجموعه ای از فلزات، پلاستیک). نه تنها مواد روی زمین، بلکه کل جهان از همان عناصری تشکیل شده است که دانشمندان یکی پس از دیگری در سیاره ما کشف کردند.
در درس های شیمی چیزهای جالب زیادی در مورد عناصر شیمیایی خواهید آموخت. و امروز می خواهیم شما را به طور خلاصه با تاریخچه پیشرفت علم شیمی آشنا کنیم.
دانش آموزانبه عنوان یک قاعده، اکثر مورخان شیمی مراحل اصلی توسعه آن را شناسایی می کنند:
1. دوره پیش از کیمیاگری: تا قرن سوم. آگهی
در دوره پیش از کیمیاگری، جنبه های نظری و عملی دانش در مورد ماده به طور نسبی مستقل از یکدیگر توسعه یافت. منشأ خواص ماده توسط فلسفه طبیعی باستان مورد توجه قرار گرفت؛ عملیات عملی با ماده در انحصار شیمی صنایع دستی بود.
2. دوره کیمیاگری: قرن III - XVII.
دوره کیمیاگری به نوبه خود به سه زیر دوره تقسیم می شود -اسکندریه(یونانی-مصری)،عربی و اروپایی کیمیاگری دوره کیمیاگری زمان جستجوی سنگ فیلسوفی بود که برای تبدیل فلزات ضروری تلقی می شد. در این دوره، پیدایش شیمی تجربی و انباشت دانش در مورد ماده رخ داد; نظریه کیمیاگری که بر اساس ایده های فلسفی باستانی در مورد عناصر بود، ارتباط تنگاتنگی با طالع بینی و عرفان داشت. در کنار "طلاسازی" شیمیایی و فنی، دوره کیمیاگری نیز به دلیل ایجاد یک سیستم منحصر به فرد از فلسفه عرفانی قابل توجه است.
3. دوره شکل گیری (اتحاد): قرن XVII - XVIII.
در جریان شکل گیری شیمی به عنوان یک علم، عقلانی شدن کامل آن صورت گرفت. شیمی خود را از دیدگاه های فلسفی و کیمیاگری طبیعی در مورد عناصر به عنوان حامل کیفیت های معین رها کرد. همراه با گسترش دانش عملی در مورد ماده، یک دیدگاه واحد از فرآیندهای شیمیایی شروع به توسعه و استفاده کامل کرد. روش تجربی. انقلاب شیمیایی که این دوره را تکمیل کرد، سرانجام شیمی را به شکل علمی مستقل (اگرچه با سایر شاخههای علوم طبیعی مرتبط است)، که به مطالعه تجربی ترکیب اجسام مشغول بود، ظاهر کرد.
4. دوره قوانین کمی (نظریه اتمی-مولکولی): 1789 - 1860.
دوره قوانین کمی که با کشف قوانین کمی اصلی شیمی - قوانین استوکیومتری و شکل گیری نظریه اتمی - مولکولی مشخص شد، سرانجام تبدیل شیمی به علم دقیق، نه تنها بر اساس مشاهده، بلکه بر اساس اندازه گیری است.
5. دوره شیمی کلاسیک: 1860 - پایان قرن 19.
دوره شیمی کلاسیک با پیشرفت سریع علم مشخص می شود: جدول تناوبیعناصر، نظریه ظرفیت و ساختار شیمیاییمولکول ها، استریوشیمی، ترمودینامیک شیمیاییو سینتیک شیمیایی; برنامه های کاربردی به موفقیت های درخشانی دست یافته اند شیمی معدنیو سنتز آلی. در ارتباط با حجم فزاینده دانش در مورد ماده و خواص آن، تمایز شیمی آغاز شد - جداسازی شاخه های فردی آن، به دست آوردن ویژگی های علوم مستقل.
6. دوره مدرن: از آغاز قرن بیستم تا به امروز.
در آغاز قرن بیستم، انقلابی در فیزیک رخ داد: سیستم دانش در مورد ماده بر اساس مکانیک نیوتنی جایگزین شد. نظریه کوانتومو نظریه نسبیت ایجاد تقسیم پذیری اتم و ایجاد مکانیک کوانتومیمحتوای جدید را در مفاهیم اولیه شیمی قرار دهید. پیشرفتهای فیزیک در آغاز قرن بیستم، درک دلایل تناوب ویژگیهای عناصر و ترکیبات آنها، توضیح ماهیت نیروهای ظرفیت و ایجاد نظریهها را ممکن ساخت. پیوند شیمیاییبین اتم ها ظهور اساسا جدید روش های فیزیکیتحقیقات فرصتهای بیسابقهای برای مطالعه ترکیب، ساختار و واکنشپذیری یک ماده برای شیمیدانان فراهم کرد. همه اینها با هم منجر به، از جمله دستاوردهای دیگر، موفقیت های درخشان شیمی بیولوژیکی در نیمه دوم قرن بیستم شد - ایجاد ساختار پروتئین ها و DNA، دانش مکانیزم های عملکرد سلول های یک موجود زنده.
مجری دوم
شیمی در مصر به وجود آمد. نام« علم شیمی » از کلمه همی یا هما (سیاه) گرفته شده است که مصریان باستان آن را کشور خود می نامیدند. بنابراین، کلمه "شیمی" به هنر مصری اشاره دارد که با مواد معدنی و فلزات مختلف سروکار داشت. شیمی یک علم الهی محسوب می شد، در دست کشیشان بود و از ناآگاهان پنهان بود. اعراب به کلمه «شیمی» یک ویژگی اضافه کردند عربیپیشوند "ال". اصطلاح "کیمیاگری" و "کیمیاگر" ظاهر شد. اکنون کیمیا نامی است که به دوره توسعه شیمی باقرن چهارم تا شانزدهم. آگهی
هدف تحقیقات کیمیاگران جستجوی "سنگ فیلسوف" بود که ظاهراً قادر به تبدیل هر فلزی به طلا است. پادشاهان و پادشاهان کیمیاگران را در کاخ های خود نگه می داشتند تا بتوانند برای آنها طلا بدست آورند. ببینید کیمیاگران چگونه کار می کردند.
کیمیاگر
- من آزمایش "تبدیل آب به طلا" را به شما نشان خواهم داد.
یک لیوان حاوی محلول تازه تهیه شده از یدید پتاسیم و دیگری حاوی محلولی از استات سرب است. هر دو محلول در یک لیوان با ظرفیت بزرگتر ریخته می شوند. یک رسوب زرد روشن از یدید سرب رخ می دهد (کارتی را با یک واکنش شیمیایی نشان دهید).
2 KI + سرب ( CH 3 COO )2 = PbI 2 + 2 KCH 3 COO
در درس های بعدی یاد خواهیم گرفت که چنین نمادهایی از معادلات واکنش شیمیایی به چه معناست.
مجری سوم
اما کیمیاگران هرگز نتوانستند فلزات را به طلا تبدیل کنند. کیمیاگری در بسیاری از کشورها ممنوع بود. افرادی که به تحقیقات کیمیاگری مشغول بودند به جادوگری متهم شدند و در آتش سوزانده شدند. اما علم را نمی توان ممنوع کرد. دانشمندان پیشوند "ال" را از کلمه "کیمیاگری" حذف کردند و نام جدیدی - شیمی به دست آوردند. الان اسمش همینهعلمی که مواد اطراف ما و همچنین خواص و دگرگونی های آنها را مطالعه می کند.
امروزه محصولات شیمیایی جایگاه غالبی را در ما به خود اختصاص داده اند زندگی روزمره. تحقیقات شیمیایی در آزمایشگاه های پژوهشکده، کارخانه ها، کارخانه ها و غیره انجام می شود. هر مدرسه دارای یک اتاق شیمی و یک آزمایشگاه شیمی است.
حال با چند ماده و دگرگونی های شیمیایی آشنا می شویم.
دستیار اول آزمایشگاه- من آزمایش "تبدیل آب به شربت تمشک" را به شما نشان خواهم داد.
برای انجام آزمایش از چهار بشر و یک پارچ شیشه ای تیره استفاده شده است. لیوان اول حاوی فنل فتالئین، دومی حاوی کربنات سدیم، چهارمی حاوی هیدروژن سولفات سدیم و کوزه حاوی آب است. لیوان سوم هیچ چیزی ندارد.
در یک کوزه شیشه ای تیره آب معمولی وجود دارد، آن را در چهار لیوان بریزید. سپس آب لیوان ها را به جز لیوان آخری دوباره داخل کوزه بریزید و لیوان آخر را به عنوان کنترل باقی بگذارید. دوباره از کوزه آب داخل لیوان بریزیم. نگاه کنید: محلول به رنگ زرشکی روشن مانند شربت تبدیل شده است! "شربت" را در یک کوزه بریزید، از آخرین لیوان با "آب" رقیق کنید. آخرین بارآب از کوزه داخل لیوان ها بریزید. ببینید، "شربت" دوباره به آب تبدیل شده است.
انگار یک معجزه است! نه، در یک لیوان فقط فنل فتالئین و در شیشه دیگر یک محلول قلیایی وجود داشت. هنگامی که آنها مخلوط می شوند، محلولی به رنگ زرشکی تشکیل می شود. یاد آوردن:فنل فتالئین در محلول های قلیایی همیشه زرشکی برای از بین رفتن رنگ، کمی محلول اسیدی اضافه کردم. اسید قلیایی را خنثی کرد و محلول تغییر رنگ داد.
مواد شیمیایی مورد استفاده در این آزمایش را نام ببرید.
دستیار آزمایشگاه دوم
- بسیاری از شما عاشق افسانه ها و داستان های علمی تخیلی هستید. اکنون خواهید دید که چگونه بیگانه یا به سادگی مار گورینیچ از پیله متولد می شود.
(موسیقی پخش می شود، آزمایش "مارهای فرعون" نشان داده می شود)
شرح تجربه
یک قرص سوخت خشک را آسیاب کنید و آن را در یک پشته روی پایه قرار دهید. سه قرص نورسولفازول را روی سوخت قرار دهید. سوخت خشک سبک از یک میله فلزی برای اصلاح "مارها" در حال خزنده استفاده کنید. پس از اتمام آزمایش، آتش را با درپوش پلاستیکی خاموش کنید.
دستیار اول آزمایشگاه
- حالا دستمال را در دستانم می گیرم، ابتدا آن را با آب کلید خیس می کنم و با شعله کبریت آتش می زنم.
(آزمایش "روسری نسوز" نشان داده شده است)
شرح تجربه
دستمال را در آب بشویید، سپس آن را به آرامی فشار دهید و به خوبی در الکل خیس کنید. دستمال را با انبرهای بوته ای از یکی از انتهای آن بگیرید و در حالی که آنها را درازای بازو نگه دارید، یک ترکش بلند به پارچه بیاورید. الکل بلافاصله شعله ور می شود - به نظر می رسد که دستمال آتش گرفته است. اما سوختن متوقف می شود و روسری آسیبی نمی بیند، زیرا دمای اشتعال پارچه مرطوب بسیار بالاتر از الکل است.
سی 2 اچ 5 اوه + 3 O 2 = 2 CO 2 + 3 اچ 2 O
ماده ای را نام ببرید که از فرآیندهای احتراق و تنفس پشتیبانی می کند. از خواص این ماده چه می دانید؟
دستیار آزمایشگاه دوم
- در پایان جلسه ما آزمایشی به نام "آتشفشان" را نشان خواهم داد. شما، البته، می دانید که چه منظره باشکوهی است - یک فوران آتشفشانی. در دوران باستان، آتشفشان وزوویوس شهر پمپئی را مدفون کرد.
(بازی های موسیقی و تجربه نشان داده می شود.)
شرح تجربه
یک بوته یا فنجان چینی را در گردن فلاسک مخروطی قرار دهید. فلاسک را می توان با پلاستیلین پوشانده و به آن شکل کوهی داد و یا می توان مدلی از تپه ساخت. یک ورق کاغذ بزرگ را زیر فلاسک یا ماکت قرار دهید تا اکسید کروم جمع شود. III ). دی کرومات آمونیوم را داخل یک بوته بریزید و آن را با الکل در مرکز تپه مرطوب کنید. آتشفشان توسط یک ترکش در حال سوختن مشتعل می شود. واکنش گرمازا است، به شدت ادامه مییابد و ذرات داغ اکسید کروم همراه با نیتروژن به بیرون پرتاب میشوند. III ). اگر نور را خاموش کنید، تصور یک آتشفشان در حال فوران را خواهید داشت که از دهانه آن توده های داغ بیرون می ریزد (نشان دادن کارتی با واکنش شیمیایی).
( N.H. 4)2 Cr 2 O 7 = ن 2 + Cr 2 O 3 + 4 اچ 2 O
(اکسید کروم (III). ) جمع آوری و برای آزمایش های دیگر ذخیره کنید).
معلم
این همان تعداد دگرگونی های شیمیایی جالبی است که امروز باید در کلاس مشاهده می کردید.
یک واکنش شیمیایی را می توان با علائم آن - تغییر رنگ مواد، ظاهر شدن بو، تشکیل رسوب، انتشار نور و گرما و تشکیل یک ماده گازی - قضاوت کرد.
- در آزمایش های نشان داده شده چه نشانه هایی از واکنش های شیمیایی را می توانید نام ببرید؟
III. آزمون برای دانش آموزان معلم- خوب، بچه ها، آیا شیمی شما را با شگفتی های خود مجذوب خود کرده است؟ و اکنون سعی می کنید به سوالات مسابقه پاسخ دهید که مانند بلیط ورودی برای شما خواهد بود دنیای شگفت انگیزمواد و دگرگونی ها
سوالات امتحانیرایج ترین ماده روی زمین (اب)
در آب فرو نمی رود، در آتش نمی سوزد و فقط در دمای زیر صفر درجه وجود دارد.(یخ)
فلزی را نام ببرید که در دمای اتاق مایع است. (سیاره تیر)
بدون این گاز در دنیا
حیوانات و مردم زنده نخواهند شد.
بچه ها می توانند آن را برای شما نام گذاری کنند
بالاخره به او می گویند -….اکسیژن
5) من در جهان شناخته شده زندگی می کنم، در آپارتمان سیزدهم. من نرم، سبک، چکش خوار هستم، در بسته بندی می درخشم. (آلومینیوم )
6) این گاز در هنگام تخلیه صاعقه تشکیل می شود. آنجا در یک جنگل کاج است، جایی که می توانید به راحتی نفس بکشید.
و هیچ مزه ای در آب باقی نمی گذارد و به خوبی آن را ضد عفونی می کند. (ازن )
آفرین به همه سوالات درست جواب دادی
حالا چه مواد شیمیایی را می توانید نام ببرید؟
IV. جمع بندی درس معلم:آیا دستیاران من به شما ثابت کرده اند که شیمی علم جالبی است؟ چه چیزی به شما کمک کرد تا خودتان را در این مورد متقاعد کنید؟ چه آزمایش هایی را می توانید در خانه تکرار کنید تا عزیزان خود را شگفت زده کنید؟ اما نکات ایمنی را فراموش نکنید.
اما شیمی یکی از علوم پیچیده است که در بخش علوم طبیعی گنجانده شده است. میلیون ها ماده و در نتیجه میلیون ها فرمول های شیمیایی، واکنش های شیمیایی، بسیاری از قوانین و الگوها. و شما باید این قوانین، قوانین شیمی، قوانین جهان را مطالعه کنید. هرکسی که خود را وقف این علم کند، می تواند در کشف اسرار طبیعت، ایجاد مواد و مواد جدیدی که در طبیعت وجود ندارند، کمک کند.
در حین سال تحصیلی، از درس به درس، من و شما به تدریج سیاره را فتح خواهیم کرد - شیمی 8 که فقط با کمک دانش خود می توانیم آن را تصاحب کنیم.
برای شما در این کار دشوار آرزوی موفقیت دارم اما مسیر جالب! موفق باشید!
V. مشق شبطبق کتاب درسی: پیشگفتار. معرفی. فصل 1.§1 موضوع شیمی. مواد. تبدیل مواد.
تهیه گزارش (اختیاری) در مورد تاریخ شیمی: "دانش شیمیایی مردمان باستان"، "کیمیاگری"، "شیمی عملی در روسیه باستان".
مسأله 82عنصر هیدروژن
پروفسور دیمیتری ایوانوویچ در درس ویدیویی شیمی جدید خود به بینندگان کنجکاو تلویزیون درباره عنصر هیدروژن خواهد گفت.
دیمیتری ایوانوویچ در پاسخ به سؤالی از بیننده تلویزیونی وسوولود ماکاروف توضیح می دهد که چرا عنصر هیدروژن را می توان در دو سلول جدول D.I. به طور همزمان یافت. مندلیف. معلوم می شود که تمام نکته در توانایی او برای قرار گرفتن در حالات مختلف است. اما برای اینکه همه چیز را به درستی درک کنید، البته، ابتدا باید اصل ساختار خود جدول تناوبی و تفاوت بین گروه های عناصر این جدول را به خاطر بسپارید. سپس همه چیز بلافاصله روشن می شود.
همچنین از این درس شیمی ویدیویی، بینندگان تلویزیون خواهند آموخت که عنصر هیدروژن رایج ترین عنصر در جهان است. او کجا نیست! حتی خورشید نیز از سه چهارم آن تشکیل شده است!
استفاده از عنصر هیدروژن به عنوان سوخت، چشم اندازهای هیجان انگیزی را در اختیار شما قرار می دهد! پس از همه، عواقب مضر سوزاندن چنین سوختی برای محیطحداقل، اگر وجود نداشته باشد. بنابراین استفاده از چنین سوختی در مقیاس وسیع می تواند کمک قابل توجهی به بشریت در حل مشکلات زیست محیطی کند.
هنگامی که کودک به دبیرستان می رسد، موضوعاتی دارد که اکثر والدین دیگر نمی توانند به آنها کمک کنند، به خصوص اگر دانش آموز تعدادی از کلاس های مدرسه را از دست داده باشد و اکنون شکاف های قابل مشاهده ای در دانش داشته باشد. یکی از این رشته های سخت، شیمی است. به لطف فراوانی فرمول ها و عناصر شیمیایی، کنار آمدن با آن همیشه بسیار دشوار است. اما وضعیت را می توان اصلاح کرد و دروس ویدیویی جالب و آموزنده در مورد شیمی به این امر کمک می کند.مطالعه با آکادمی مجازی آسان است
این سایت حدود صد درس آنلاین شیمی را ارائه می دهد که اکثر آنها بر اساس کتاب های درسی مدرن گابریلیان هستند. مطالبی برای نمرات 8،9،10 و 11 وجود دارد که همه را پوشش می دهد ویژگی های سنیاین گروه از دانش آموزان تمامی کلاس ها توسط اساتید مجرب تدریس می شود که نه تنها مطالب را آموزش می دهند، بلکه آن را نیز توضیح می دهند مثال های ساده. مزیت درس های ویدیویی در شیمی این است که می توانید تمام فرآیندها و واکنش ها را به وضوح نشان دهید و آزمایش ها را انجام دهید.یادگیری شیمی از ساده به پیچیده
برای تسلط کامل بر موضوع، باید از شیمی عناصر شروع کنید. آنها اساس این رشته هستند. سپس می توانید به ساختار اتم، اسیدها، نمک ها، مواد و فلزات بروید. با مطالعه دقیق این مطالب، می توانید شروع به آشنایی با درس های ویدیویی کنید معادلات شیمیاییو واکنش های مبادله ای مرحله نهاییتبدیل به شیمی آلی خواهد شد.دروس ویدیویی از آکادمی مجازی به شما کمک می کند تا به طور معنی داری برای آزمون دولتی واحد و آزمون دولتی واحد آماده شوید، زیرا با کمک آنها می توانید به راحتی آنچه را که در آن مطالعه کرده اید تکرار کنید. دوره مدرسهمواد، و همچنین اصلاح تمام مشکلات موجود.
موضوع درس:"اسیدها، ترکیب، طبقه بندی و اهمیت آنها."
اهداف درس:
آموزشی:
ترکیب و طبقه بندی اسیدها را در نظر بگیرید.
به توسعه توانایی نوشتن فرمول مواد طبقات اصلی ادامه دهید ترکیبات معدنی;
به توسعه مهارت ها برای تعیین درجه اکسیداسیون عناصر شیمیایی در ترکیبات ادامه دهید.
آموزشی:
توسعه مهارت های تفکر دانش آموزان را ادامه دهید: مقایسه، تجزیه و تحلیل، نتیجه گیری.
به توسعه مهارت های کار تجربی ادامه دهید.
ادامه توسعه مهارت های آموزشی عمومی؛
علاقه به موضوع را توسعه دهید.
آموزشی:
پرورش فرهنگ کار دانش و همکاری؛
پرورش احساس مسئولیت و دقت؛
کمک به ایجاد یک جو روانی-عاطفی مطلوب در کلاس درس.
نوع درس: ترکیب شده
روش های تدریس: کلامی (داستان، توضیح، گفتگو)؛
گویا؛
تظاهرات؛
جستجوی جزئی، مبتنی بر مشکل، تحقیق.
تجهیزات و معرف ها: لپ تاپ، پروژکتور، تابلوی تعاملی، ارائه، نمونه اسیدها: کلریدریک، سولفوریک، اسکوربیک، استیک، سیتریک، لوله آزمایش، قفسه لوله آزمایش، اندیکاتور، دفترچه، برگه، جداول با فرمول اسید.
در طول کلاس ها:
سازمان لحظه
به روز رسانی دانش.
? بچه ها، ما شروع به مطالعه کلاس های ترکیبات معدنی کرده ایم. قبلاً با چه دسته ای از مواد آشنا شده ایم؟(اکسیدها، هیدریدها و فرار ترکیبات هیدروژنی، زمینه).
CaO، SO 2 ، Fe 2 در باره 3 ، نا 2 اوه، کل 2 در باره 7 (اسلاید 1).
? چه فرمول هایی می بینید؟
? به چه موادی اکسید می گویند؟
? مواد زیر به کدام دسته تعلق دارند: KOH، Al(OH) 3 ، Ba(OH) 2 مس (OH) 2 ?
? چه موادی پایه محسوب می شوند؟
? چه چیزی تعداد گروه های هیدروکسیل در پایه را تعیین می کند؟(بسته به حالت اکسیداسیون فلز.)
(اسلاید 2). تیک تاک پا "پایه ها"
مسیر برنده متشکل از فرمول های پایه را پیدا کنید.
زمین بازی شماره 1 زمین بازی شماره 2
این دلایل را نام ببرید.? فونداسیون ها در اولین زمین بازی چه مشترکاتی دارند و چه تفاوتی با پایه های واقع در زمین بازی شماره 2 دارند؟(در زمین بازی اول - پایه های محلول، در دوم - نامحلول.)
مثال بزن
? پایه های محلول چه ویژگی هایی دارند؟ هنگام استفاده از مواد قلیایی چه اقدامات احتیاطی باید رعایت شود؟
وظیفه طبقه بندی مرکب(اسلاید 3)
مواد زیر را به سه گروه طبقه بندی کنید. این گروه ها را نام ببرید
CaO، Al(OH) 3 ، CuO، HCl، H 2 اوه، کل 2 در باره 7 ، Fe(OH) 2 , NO 3 ، NaOH، H 2 بنابراین 4 .
یادگیری مطالب جدید
در گروه سوم شما موادی را قرار دادید که هنوز برای شما ناآشنا هستند که متعلق به کلاس اسیدها هستند. امروز با موادی از این کلاس آشنا خواهیم شد. بنابراین، موضوع درس ما "اسیدها: ترکیب، طبقه بندی و معنی" است.موضوع درس را در آن بنویسید کتاب کار. (اسلاید 4).
? در مورد اسیدها چه چیزهایی باید بدانیم؟(ترکیب، فرمول ها، نام ها، طبقه بندی ها، معنی، مقررات ایمنی).
انواع اسیدها (اسلاید 5).
طرح مطالعه اسید (اسلاید 6).
ترکیب.
طبقه بندی.
نامگذاری و اکسیدهای مربوطه
معنی و کاربرد.
قوانین ایمنی هنگام کار با اسیدها
ترکیب اسیدها (اسلاید 7).
فرمول سه اسید را مشاهده می کنید: کلریدریکHCl ، بابونهن 2 بنابراین 4 و اسیدهای فسفریکن 3 RO 4 . چه وجه مشترکی با هم دارند؟
بله، این وجود اتم های هیدروژن در ترکیب آنهاست که هر سه فرمول با آن شروع می شود. بقیه را باقیمانده اسید می نامند.
اسیدها – مواد پیچیده ای که مولکول های آنها از اتم های هیدروژن و یک باقی مانده اسید تشکیل شده است.
طبقه بندی اسیدها
الف) با وجود اکسیژن . (اسلاید 8)
? به تفاوت باقیمانده اسیدهای دو گروه اسید روی تخته توجه کنید. این تفاوت چیست؟
درست است، بقایای اسیدی اسیدهای سولفوریک، نیتریک، فسفریک و پرکلریک حاوی اکسیژن هستند و بقایای اسیدی اسیدهای هیدروکلریک، هیدروبرومیک، هیدروسولفوریک و هیدروفلوریک حاوی اکسیژن نیستند.
وجود اکسیژن یا عدم وجود آن یکی از نشانه های طبقه بندی اسیدها است. با توجه به این معیار، اسیدها به دو گروه تقسیم می شوند:بدون اکسیژن وحاوی اکسیژن از جدول مثال هایی از اسیدهای بدون اکسیژن و حاوی اکسیژن بیاورید.
ب) طبقه بندی اسیدها بر اساس بازی . (اسلاید 9).
? به فرمول های اسید روی تخته نگاه کنید. آنها بر اساس معیارهای خاصی به سه گروه تقسیم می شوند. به نظر شما این علامت چیست؟
پایه - تعداد اتم های هیدروژن در اسید
از جدول نمونه هایی از اسیدهای مونوبازیک، دوبازیک و تری بازیک بیاورید.
با تعداد اتم های هیدروژن، می توانید بار کل باقی مانده اسید را تعیین کنید، که وقتی در آب حل می شود، یک یون با بار منفی تشکیل می دهد.
هنگامی که هیدروژن حل می شود، یک یون با بار مثبت تشکیل می دهد که بار آن +1 است. تعیین بار یون ویژگی های خاص خود را دارد.
ب) طبقه بندی اسیدها بر اساس حلالیت در آب (اسلاید 10).
به هر حال، توانایی حل شدن در آب نشانه دیگری از طبقه بندی اسیدها است. بر این اساس تمام اسیدها به دو گروه محلول و نامحلول تقسیم می شوند. بیایید با استفاده از جدول حلالیت مثال هایی بزنیم.
درجه اکسیداسیون عناصر در اسیدها و اکسیدهای مربوط به اسیدها. (اسلاید 11).
1 −1 +1 − 2 +1 ایکس − 2 +5 − 2
HCl H 2 اس اچ 3 RO 4 → پ 2 در باره 5 - اسید فسفریک
(+1) 3 +x + (-2) · 4 = 0
x − 5 = 0
ایکس = + 5
1 + 3 − 2 +3 − 2
ن 3 RO 3 → پ 2 در باره 3 - اسید فسفر
اکسیدهای مربوط به اسیدها را شناسایی کنید.(اسلاید 12).
ن 2 بنابراین 4 → SO 3 نه 3 → ن 2 در باره 5
ن 2 بنابراین 3 → SO 2 نه 2 → ن 2 در باره 3
نامگذاری اسیدها
اسیدهای آنوکسیک:
یک واکه به نام عنصر اسیدساز اضافه می شود"O"
و کلمات "هیدروژن اسید"
HCl- اسید هیدروکلریکن 2 S – هیدروسولفید اسید
اسیدهای حاوی اکسیژن:
پسوند به نام روسی عنصر تشکیل دهنده اسید اضافه شده است:
اگر عنصر نمایش داده شودبالاتر CO(برابر با شماره گروه)
+6
– "-n" و پایان "-aya":اچ 2 بنابراین 4
اگر عنصر CO زیر بالاترین +4
– "-ist" و پایان "-aya":اچ 2 بنابراین 3
اسید گوگرد
اهمیت اسیدها در طبیعت و زندگی انسان (اسلاید 13-14).
اسیدهای موجود در طبیعت
اسیدها در زندگی انسان
در بدن انسان
در پخت غذا
در پزشکی
که در اقتصاد ملی
باران اسیدی
قوانین ایمنی هنگام کار با اسیدها (اسلاید 15-16).
در قرن نوزدهم، دانشمند Justus Liebig در آلمان زندگی و کار می کرد. او یک آزمایشگر از جانب خدا بود، از کودکی مشتاقانه به پدرش در تهیه لاک، رنگ و دارو کمک می کرد. یک روز، در خلال یک درس یونانی، کوله پشتی لیبیگ با فولمینات جیوه منفجر شد. پدر، مطمئن شد که پسر برای ورزشگاه بریده نشده است، او را نزد یک داروساز شاگرد کرد. چند ماه بعد، شیمیدان سیزده ساله بهتر از معلم می دانست که چگونه داروها را ترکیب کند. پس از یک انفجار دیگر او را بیرون انداختند، اما تحصیلات خود را در شیمی رها نکرد و در سن 23 سالگی استاد دانشگاه گیسن شد. کارل وگت، شیمیدانی که با لیبیگ کار می کرد، یک مورد را اینگونه توصیف می کند. لیبیگ با در دست داشتن یک بطری با درپوش زمینی وارد می شود. او به وگت میگوید: «بیا، دستت را خالی کن» و با چوب پنبهای خیس دستش را لمس میکند. «این درست نیست، می سوزد؟ – لیبیگ با خونسردی می پرسد. من تازه اسید فرمیک بی آب دریافت کردم. به نظر شما آیا لیبیگ اسیدها را به درستی مدیریت می کند؟
(خیر. هنگام کار با مواد شیمیاییباید مراقب باشید: موهای خود را بردارید، آستین های خود را بالا بزنید، بیش از 1-2 میلی لیتر محلول بریزید، شیشه را با برچسب رو به بالا نگه دارید.)
? چگونه می توان اسید را بدون توسل به روش های افراطی تعیین کرد؟
تثبیت دانش
تجربه آزمایشگاهی
کارت راهنمایی:
شکل کار: اتاق بخار.
زمان عملیات - 8-10 دقیقه.
ورزش:
مطالعه رنگ شاخص ها در محیط های اسیدی.
تجهیزات و معرف ها:
3 لوله آزمایش با اسید هیدروکلریک و 3 لوله آزمایش با اسید سیتریک، نشانگرهای مایع: تورنسل، فنل فتالئین و متیل اورانژ، میله های شیشه ای.
مقررات ایمنی:
توجه! لازم است با دقت با اسیدها کار کنید، زیرا ممکن است دچار سوختگی یا مسمومیت شوید. اگر اسید روی پوست تان رفت، آن را با جریان آب بشویید.
انجام آزمایش و گزارش نتایج:
گروه 1:
در لوله آزمایش با اسید هیدروکلریکیک قطره فنل فتالئین اضافه کنید. با میله شیشه ای هم بزنید. نتایج مشاهدات را در جدول ثبت کنید.
یک قطره متیل اورانژ به لوله آزمایش دوم با اسید هیدروکلریک اضافه کنید. با میله شیشه ای هم بزنید. نتایج مشاهدات را در جدول ثبت کنید.
یک قطره تورنسل به لوله آزمایش سوم با اسید کلریدریک اضافه کنید. با میله شیشه ای هم بزنید. نتایج مشاهدات را در جدول ثبت کنید.
گروه 2:
یک قطره فنل فتالئین را به یک لوله آزمایش حاوی اسید سیتریک اضافه کنید. با میله شیشه ای هم بزنید. نتایج مشاهدات را در جدول ثبت کنید.
یک قطره متیل اورانژ به لوله آزمایش دوم با اسید سیتریک اضافه کنید. با میله شیشه ای هم بزنید. نتایج مشاهدات را در جدول ثبت کنید.
یک قطره تورنسل به لوله آزمایش سوم با اسید سیتریک اضافه کنید. با میله شیشه ای هم بزنید. نتایج مشاهدات را در جدول ثبت کنید.
تاثیر اسیدها بر شاخص ها
بحث در مورد نتایج و فرمول نتیجه گیری:چه شاخص هایی رنگ خود را در اسیدها تغییر دادند؟(لیتموس و متیل اورانژ).
? آیا تغییرات رنگی یکسان این شاخص ها را در هر دو اسید مشاهده کردید؟(آره).
? تورنسل و متیل اورانژ در هر دو اسید کلریدریک و سیتریک چه رنگی به دست آوردند؟
(لیتموس قرمز شد و متیل نارنجی صورتی شد).
بر اساس آزمایش های انجام شده، نتایج زیر را می گیریم:
صرف نظر از نوع اسید (آلی یا معدنی)، شاخص ها رنگ خود را یکسان تغییر می دهند. به این معنی که همه اسیدها دارای خواص مشابه هستند.
?
این به چه چیزی مرتبط است؟(با حضور اتم های هیدروژن).
اگر شما وقت دارید. کار در اسلاید 18
خلاصه کردن. انعکاس.
جمع بندی درس. درجه بندی.
جمله را ادامه دهید
امروز سر کلاس یاد گرفتم...
یاد گرفتم…
برام واضح نبود...
این برای من درس است...
باعث علاقه شد...
مشکلات زمانی به وجود آمد که ...
مشق شب. §20، ص. 102-107 فرمول و نام اسیدها را بیاموزید، تکلیف 6 ("کاربرگ")، تکلیف 1، ص 107 (کتاب درسی).