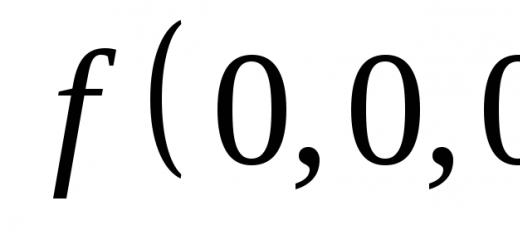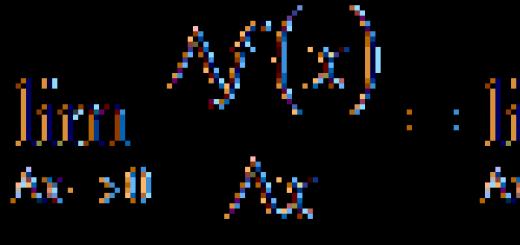گچ- یک ماده معدنی طبیعی از کلاس سولفات. از بین تمام سولفات های طبیعی، بیشترین اهمیت را در صنعت ساختمان دارد. در طبیعت به شکل دی هیدرات - سولفات کلسیم دی هیدرات CaSO 4 یافت می شود. 2H 2 O و در حالت بی آب - انیدریت CaSO4.
اساساً، گچ عمدتاً به عنوان ماده اولیه برای تولید چسباننده های گچ کم سوز و زیاد و به عنوان یک افزودنی که هنگام آسیاب کردن کلینکر سیمان پرتلند و انواع آن به منظور تنظیم زمان گیرش معرفی می شود، استفاده می شود.
جهت دیگر استفاده از گچ طبیعی، ساخت محصولات دیوار و پارتیشن است که به دلیل رسانایی حرارتی پایین آن است: در دمای 30 درجه سانتی گراد 0.28-0.34 W/(m.K).
دی هیدرات گچ طبیعی سنگی با منشا رسوبی است که عمدتاً از بلورهای بزرگ و کوچک CaSO4 تشکیل شده است. 2H 2 O. توده های کریستال گچ می توانند تشکیل شوند گل رز گچی. تشکیلات متراکم گچ نامیده می شود سنگ گچ.
تفاوت های ساختاری
بر اساس ظاهر و ساختار سنگ، آنها متمایز می شوند:
- کریستالگچ شفاف؛
- پویکیلیتیکیا گچ شنی - کریستال های پر از ماسه.
پویکیلیت(به انگلیسی: Poikilite) - کریستال یا دانه ای که حاوی مواد معدنی متعددی است که در طول رشد یک فرد به دست آمده است.
- سنگ گچ- کانی لایه ای با کریستال های شفاف صاف از ساختار لایه ای، افراد کاملاً هستند اندازه های بزرگ، شفاف (چشم مریین);
- سلنیت- گچ الیاف موازی، به رنگ زرد با درخشندگی ابریشمی
- گچ دانه ای؛
- سنگ سنگی
انواع کریستالی، فیبری، دانه ای و شنی گچ وجود دارد.
زیر تفاوتبه مجموعه ای از افراد معدنی از همان گونه های معدنی اشاره دارد که از نظر خصوصیات مورفولوژیکی متفاوت هستند. به عنوان مثال، تفاوت در گچ: "شیشه مارینو" - گچ لایه ای، سلنیت - گچ فیبری.
گچ توده های مرمر مانند پیوسته، تجمعات رگه ای و همچنین تک بلورها و دروزها را تشکیل می دهد. شکل ظاهری کریستال های آن معمولاً لایه ای، ستونی و سوزنی شکل است.
خواص فیزیکی سنگ گچ
شبکه کریستالی از دی هیدرات گچ و انیدریت

در شبکه کریستالی دی هیدرات گچ، هر اتم کلسیم توسط شش گروه پیچیده شامل چهار چهار وجهی و دو مولکول آب احاطه شده است. ساختار شبکه کریستالی این ترکیب لایه لایه است. لایه ها از یک طرف توسط یون های Ca 2 + و گروه های SO 4 - 2 و از سوی دیگر توسط مولکول های آب تشکیل می شوند. هر مولکول آب با یون های Ca2+ و چهار وجهی سولفات نزدیک است. در داخل لایه حاوی یون های Ca 2 + و SO 4 -2 پیوندهای نسبتاً قوی (یونی) وجود دارد، در حالی که در جهت لایه های حاوی مولکول های آب، پیوندهای لایه ها بسیار ضعیف تر است. بنابراین در طی عملیات حرارتی، گچ دی هیدرات به راحتی آب خود را از دست می دهد (فرایند آبگیری). در عمل، این فرآیند را می توان با درجات تکمیل متفاوت انجام داد و بسته به این، می توان چسب های گچی با اصلاحات مختلف با خواص مختلف به دست آورد.
در شبکه کریستالی انیدریت، یون های گوگرد در مراکز گروه های اکسیژن چهار وجهی قرار دارند و هر یون کلسیم توسط هشت یون احاطه شده است. در بیشتر موارد، انیدریت توده های پیوسته را تشکیل می دهد، اما بلورهای مکعبی، ستون کوتاه و سایر بلورها یافت می شوند.
گرم کردن گچ
در زیر لوله دمنده، گچ آب را از دست می دهد، تقسیم می شود و به مینای سفید تبدیل می شود. سه اثر روی منحنی های گرمایش گچ مشاهده می شود:
- در دمای 80-90 درجه سانتیگراد مقدار مشخصی H 2 0 آزاد می شود.
- در دمای 140 درجه سانتیگراد گچ به همی هیدرات تبدیل می شود.
- در دمای 140-220 درجه سانتیگراد رخ می دهد انتخاب کاملاب؛
- در دمای 400 درجه سانتی گراد، گچ برای همیشه می سوزد.
حلالیت گچ
گچ حلالیت قابل توجهی در آب دارد (حدود 2 گرم در لیتر در 20 درجه سانتی گراد). از ویژگی های قابل توجه گچ این است که حلالیت آن با افزایش دما در دمای 37-38 درجه سانتیگراد به حداکثر می رسد و سپس به سرعت کاهش می یابد.
بیشترین کاهش حلالیت در دمای بالاتر از 107 درجه سانتیگراد به دلیل تشکیل "همی هیدرات" - CaSO 4 رخ می دهد. 0.5H 2 O. حلالیت گچ در حضور الکترولیت های خاص (به عنوان مثال، NaCl، (NH 4) 2 SO 4 و اسیدهای معدنی افزایش می یابد.
از محلول، گچ به شکل کریستال های سوزنی شکل مشخص، سفید یا رنگی شده توسط ناخالصی ها متبلور می شود.
گچ از یونانی - گچ، به راحتی با خواص زیر مشخص می شود:
- سختی کم؛
- تصعید فراوان آب در یک لوله بسته؛
- در شعله یک لامپ الکلی سفید (کدر) می شود و به پودر خرد می شود ، به مینای سفید ذوب می شود که واکنش قلیایی ایجاد می کند.
- نسبتاً ضعیف در آب و اسیدها حل می شود.
انحلال انیدریت یک برهمکنش مستقیم بین آب و سولفات کلسیم است؛ اشباع زمانی اتفاق میافتد که انرژی یون هیدراته برابر با انرژی یون در شبکه شود. به طور معمول، چنین انحلال با انتشار کمی گرما همراه است (نه همیشه و نه برای همه نمک ها). عامل اصلی تأثیرگذار در این مورد دما است.
فرآیند انحلال نمک ها نیز به خواص حلال (آب)، کانی سازی، ترکیب و pH محیط بستگی دارد. بنابراین، حلالیت گچ با محتوای کلرید سدیم و نمک های منیزیم در آب افزایش می یابد. در آب مقطر، حلالیت گچ 2 گرم در لیتر است و در محلول های بسیار غلیظ NaCl (100 گرم در لیتر) یا MgCl (200 گرم در لیتر)، حلالیت گچ به ترتیب به 5/6 و 10 گرم در لیتر افزایش می یابد. .
گچ به خوبی در قلیاها و اسید هیدروکلریک حل می شود. با افزایش غلظت محلول قلیایی از 0.1 نیوتن. تا 1 n حلالیت گچ به شدت افزایش می یابد. بنابراین، بسته به کانیسازی و ترکیب حلال، سرعت انحلال گچ میتواند در محدودههای وسیعی متفاوت باشد، که باید هنگام شستشو از سنگ در نظر گرفته شود.
CaSO 4 + NaCl = NaSO 4 + CaCl 2
CaSO 4 + MgCl = MgSO 4 + CaCl 2
نوع گچ
سلنیت
سلنیت نوعی فیبری از گچ است که یک ماده معدنی نیمه شفاف است که از آلاباستر قوی تر است. نرم، سختی 2 در مقیاس Mohs (به راحتی با ناخن خراشیده می شود). ممکن است حاوی خاک رس، ماسه و به ندرت هماتیت، گوگرد و ناخالصی های آلی باشد.
درخشندگی ابریشمی دارد. پس از پولیش به لطف الیاف موازی، جلوه نوری رنگین کمانی زیبایی شبیه به اثر چشم گربه ای دارد.
طیف رنگی با سایه های صورتی، آبی، زرد و مرواریدی مایل به قرمز نشان داده می شود. همچنین می توانید سلنیت سفید کریستالی را پیدا کنید.

از این سنگ به عنوان یک سنگ زینتی برای ساخت جواهرات، مجسمهها و اشیای حکاکی شده هنری و خانگی استفاده میشود. به راحتی با سمباده سمباده شده و به خوبی جلا داده می شود. محصولات ساخته شده از سلنیت به راحتی مالش میشوند و به دلیل سختی کم جلا داده میشوند و پس از استفاده نیاز به پردازش مجدد دارند.
آلابستر
نام "آلاباستریت" از نام شهر آلاباسترون در مصر، جایی که سنگ از آن استخراج شده، گرفته شده است. آلابستر بسیار ارزشمند بود و برای ساختن ظروف کوچک برای عطر و گلدان برای پماد استفاده می شد. برش به ورق های نازک، آلاباستر کاملا شفاف است، بنابراین برای "لعاب" پنجره ها استفاده می شود.

امروزه آلاباستر ماده اولیه اصلی برای تولید گچ است - یک ماده چسبنده پودری که از عملیات حرارتی گچ دی هیدرات طبیعی CaSO 4 به دست می آید. 2H 2 O در دمای 100 درجه سانتیگراد و بالاتر.
بگذارید این را به شما یادآوری کنم سنگ سنگی- خالص ترین گچ ریزدانه، شبیه سنگ مرمر، سفید یا روشن.
انیدریت
انیدریت (از یونانی باستان "محروم از آب") سولفات کلسیم بی آب است. انیدریت می تواند سفید، مایل به آبی، خاکستری یا کمتر متمایل به قرمز باشد.
وقتی آب اضافه می شود، حجم آن حدود 30 درصد افزایش می یابد و به تدریج به دی هیدرات گچ تبدیل می شود.

رسوبات انیدریت در طبقات رسوبی عمدتاً در نتیجه کم آبی رسوبات گچ ایجاد می شود.
انیدریت گاهی اوقات به عنوان یک سنگ تزئینی و زینتی ارزان استفاده می شود، از نظر سختی بین جاسپر، یشم و عقیق از یک سو و سلنیت نرم و کلسیت از سوی دیگر قرار می گیرد.
امروزه از آن برای تولید چسباننده های گچی بدون سوز و پر سوز و همچنین به عنوان افزودنی برای تولید سیمان استفاده می شود.
گچ دوبل "دم کبوتر"، 7 سانتی متر، ترکمنستان
 گچشبه جزیره تامان، فدراسیون روسیه
گچشبه جزیره تامان، فدراسیون روسیه
 گچ، نمایش مونیخ، 2011
گچ، نمایش مونیخ، 2011
 گچاسپانیا 80-70*60 میلی متر
گچاسپانیا 80-70*60 میلی متر
 گچ، روی یک چوب چوبی رشد کرده است. استرالیا. مجموعه موزه Terra Mineralia. عکس از D. Tonkacheev
گچ، روی یک چوب چوبی رشد کرده است. استرالیا. مجموعه موزه Terra Mineralia. عکس از D. Tonkacheev
شبه شکلهای کلسیت، آراگونیت، مالاکیت، کوارتز و غیره روی گچ رایج هستند، مانند شبهمورفوسهای گچ روی سایر کانیها.
اصل و نسب
یک ماده معدنی با توزیع گسترده شرایط طبیعیبه طرق مختلف شکل می گیرد. منشا رسوبی (رسوب شیمیایی شیمیایی دریایی معمولی)، هیدروترمال با دمای پایین است که در غارهای کارستی و سولفاتاراها یافت می شود. در طول خشک شدن تالاب های دریایی و دریاچه های نمک از محلول های آبی غنی از سولفات رسوب می کند. لایهها، لایهها و عدسیهایی را در میان سنگهای رسوبی تشکیل میدهد که اغلب همراه با انیدریت، هالیت، سلستیت، گوگرد بومی، گاهی اوقات با قیر و نفت است. به مقدار قابل توجهی از طریق رسوب گذاری در استخرهای مرگبار دارای نمک دریاچه و دریا ته نشین می شود. در این حالت، گچ همراه با نمک طعام تنها در مراحل اولیه تبخیر، زمانی که غلظت سایر نمک های محلول هنوز بالا نیست، آزاد می شود. هنگامی که به غلظت معینی از نمک ها، به ویژه NaCl و به ویژه MgCl 2 رسید، انیدریت به جای گچ و سپس سایر نمک های محلول تر، به عنوان مثال، متبلور می شود. گچ در این حوضه ها باید متعلق به رسوبات شیمیایی قبلی باشد. در واقع، در بسیاری از نهشتههای نمک، لایههایی از گچ (و همچنین انیدریت)، با لایههایی از سنگ نمک، در قسمتهای پایینی نهشتهها قرار دارند و در برخی موارد تنها توسط سنگهای آهکی رسوبشده شیمیایی زیر آن قرار میگیرند.
توده های قابل توجهی از گچ در سنگ های رسوبی عمدتاً در نتیجه هیدراتاسیون انیدریت تشکیل می شوند که به نوبه خود در طی تبخیر رسوب می کنند. آب دریا; اغلب، هنگام تبخیر، گچ مستقیماً رسوب می کند. گچ از هیدراته شدن انیدریت در رسوبات تحت تأثیر آب های سطحیدر شرایط فشار خارجی کم (به طور متوسط تا عمق 100-150 متر) با توجه به واکنش: CaSO 4 + 2H 2 O = CaSO 4 × 2H 2 O. در این حالت، افزایش شدید حجم رخ می دهد (تا 30 درصد و در ارتباط با این اختلالات محلی متعدد و پیچیده در شرایط وقوع اقشار گچ دار. به این ترتیب، بیشتر ذخایر بزرگ گچ روی کره زمین به وجود آمد. در حفره های توده های جامد گچی، گاهی اوقات لانه هایی از بلورهای بزرگ و اغلب شفاف یافت می شود.
می تواند به عنوان سیمان در سنگ های رسوبی عمل کند. گچ رگه ای معمولاً محصول واکنش محلول های سولفاتی (که در اثر اکسیداسیون کانی های سولفیدی به وجود می آید) با سنگ های کربناته است. در سنگهای رسوبی در طی هوازدگی سولفیدها، تحت تأثیر اسید سولفوریک تشکیل شده در هنگام تجزیه پیریت به مارن و رسهای آهکی تشکیل می شود. در مناطق نیمه بیابانی و بیابانی، گچ اغلب به صورت رگه ها و گره هایی در پوسته هوازدگی سنگ ها با ترکیبات مختلف یافت می شود. در خاک های منطقه خشک، تشکیلات جدیدی از گچ ثانویه رسوب داده شده تشکیل می شود: تک بلورها، دوقلوها ("دم چلچله")، دروس، "رز گچی" و غیره.
گچ کاملاً در آب حل می شود (تا 2.2 گرم در لیتر) و با افزایش دما ابتدا حلالیت آن افزایش می یابد و بالاتر از 24 درجه سانتی گراد کاهش می یابد. به همین دلیل گچ وقتی از آب دریا رسوب می کند از هالیت جدا شده و لایه های مستقلی را تشکیل می دهد. در نیمه بیابان ها و بیابان ها با هوای خشک، تغییرات شدید دمای روزانه، خاک های شور و پر از گچ، صبح ها با افزایش دما، گچ شروع به حل شدن می کند و با بالا آمدن در محلول توسط نیروهای مویرگی، بر روی زمین رسوب می کند. سطح با تبخیر آب در عصر، با کاهش دما، کریستالیزاسیون متوقف می شود، اما به دلیل کمبود رطوبت، کریستال ها حل نمی شوند - در مناطقی با چنین شرایطی، کریستال های گچ به ویژه در مقادیر زیاد یافت می شود.
محل
در روسیه، اقشار ضخیم دارای گچ با سن پرمین در سراسر اورال غربی، در باشقیر و تاتارستان، در آرخانگلسک، ولوگدا، گورکی و سایر مناطق توزیع شده است. کانسارهای متعددی از سن ژوراسیک بالایی در شمال ایجاد شده است. قفقاز، داغستان. نمونه های جمع آوری قابل توجهی با کریستال های گچ از کانسار گاوردک (ترکمنستان) و نهشته های دیگر شناخته شده است. آسیای مرکزی(در تاجیکستان و ازبکستان)، در منطقه ولگای میانه، در رس های ژوراسیک منطقه کالوگا. در غارهای حرارتی معدن نایکا (مکزیک)، دانههایی از کریستالهای گچ با اندازه منحصر به فرد به طول 11 متر یافت شد.
کاربرد
سنگ گچ فیبری (سلنیت) به عنوان سنگ زینتی برای جواهرات ارزان قیمت استفاده می شود. از زمان های قدیم، جواهرات بزرگ - وسایل داخلی (گلدان، رومیزی، جوهردان و غیره) از آلاباستر ساخته شده است. گچ سوخته برای ریخته گری و قالب گیری (نقشه برجسته، قرنیز و غیره) به عنوان ماده اتصال دهنده در ساختمان سازی و پزشکی استفاده می شود.
برای تولید گچ ساختمانی، گچ با مقاومت بالا، مواد چسباننده گچ-سیمان-پوزولانی استفاده می شود.
- گچ همچنین نامی است که به سنگ های رسوبی که عمدتاً از این کانی تشکیل شده است، داده می شود. منشا آن تبخیری است.
گچ (انگلیسی) گچ) - سیآاسO 4 * 2اچ 2 O
طبقه بندی
| استرونز (ویرایش هشتم) | 6/C.22-20 |
|---|---|
| دانا (ویرایش هفتم) | 29.6.3.1 |
| دانا (ویرایش هشتم) | 29.6.3.1 |
| Hey's CIM Ref. | 25.4.3 |
مشخصات فیزیکی
| رنگ معدنی | بی رنگ تبدیل به سفید، اغلب توسط مواد معدنی ناخالص رنگ زرد، صورتی، قرمز، قهوه ای، و غیره. گاهی اوقات رنگ آمیزی بخش-منطقه ای یا توزیع اجزاء در مناطق رشد در داخل کریستال ها مشاهده می شود. بی رنگ در رفلکس های داخلی و با چشم غیر مسلح.. |
|---|---|
| رنگ ضربه ای | سفید. |
| شفافیت | شفاف، شفاف، مات |
| بدرخشید | شیشه ای، نزدیک به شیشه ای، ابریشمی، مرواریدی، مات |
| رخ | بسیار عالی، به راحتی توسط (010) بدست می آید، در برخی از نمونه ها تقریباً شبیه میکا است. در امتداد (100) روشن، تبدیل به یک شکستگی conchoidal. با توجه به (011)، یک شکستگی خرد شده (001) می دهد. |
| سختی (مقیاس Mohs) | 2 |
| پیچ خوردگی | صاف، مخروطی شکل |
| استحکام - قدرت | قابل انعطاف |
| چگالی (اندازه گیری شده) | 2.312 - 2.322 g/cm3 |
| چگالی (محاسبه شده) | 2.308 گرم بر سانتی متر مکعب |
| رادیواکتیویته (GRapi) | 0 |
| خواص الکتریکی ماده معدنی | خواص پیزوالکتریک را نشان نمی دهد. |
| خواص حرارتی | هنگامی که گرم می شود، آب خود را از دست می دهد و به یک توده پودری سفید تبدیل می شود. |
خواص نوری
| تایپ کنید | دو محوری (+) |
|---|---|
| ضریب شکست | nα = 1.519 - 1.521 nβ = 1.522 - 1.523 nγ = 1.529 - 1.530 |
| زاویه 2 ولت | اندازه گیری شده: 58 درجه، محاسبه شده: 58 درجه تا 68 درجه |
| حداکثر دوشکستگی | δ = 0.010 |
| تسکین نوری | کوتاه |
| پراکندگی محور نوری | قوی r > v مورب |
| لومینسانس | رایج و متنوع. رایج ترین رنگ های فلورسانس، آبی-آبی و سایه های زرد طلایی تا زرد است. کریستال های سلنیت اغلب فلورسانس «ساعت شنی» پهنه بندی شده را در مناطقی از خود نشان می دهند که ممکن است در نور معمولی مشهود باشد یا نباشد. |
خواص کریستالوگرافی
| گروه نقطه | 2/m - مونوکلینیک- منشوری |
|---|---|
| سنگونیا | مونوکلینیک |
| گزینه های سلول | a = 5.679 (5) Å، b = 15.202 (14) Å، c = 6.522 (6) Å β = 118.43 درجه |
| نگرش | a:b:c = 0.374:1:0.429 |
| تعداد واحدهای فرمول (Z) | 4 |
| حجم سلول واحد | V 495.15 ų (محاسبه شده از پارامترهای سلول واحد) |
| دوقلو | (100) ("دم چلچله")، بسیار رایج، با زاویه ورود مجدد که معمولاً توسط (111) تشکیل می شود. در (101) به عنوان دوقلوهای تماسی ("پروانه" یا "قلب شکل")، در امتداد (111); در (209); همچنین به عنوان دوقلوهای نفوذی صلیبی شکل. |
ترجمه به زبان های دیگر
پیوندها
کتابشناسی - فهرست کتب
- مالتسف V.A. "لانه" گچ افراد معدنی پیچیده هستند. - سنگ شناسی و کانی ها، 1376، N 2.
- Maltsev V. A. مواد معدنی سیستم غار کارست Cap-Coutan (جنوب شرقی ترکمنستان). - دنیای سنگ، 1993، شماره 2، صص 3-13 (5-30 به زبان انگلیسی)
- Russo G.V.، Shlyapintokh L.P.، Moshkii S.V.، Petrov T.G. 0b بررسی تبلور گچ در طی تولید استخراج اسید فسفریک. - مجموعه مقالات موسسه لنگیپرخیم، 1976، شماره. 26، ص. 95-104.
- Semenov V. B. Selenite. Sverdlovsk; انتشارات کتاب اورال میانه، 1984. - 192 ص.
- Linnaeus (1736) Systema Naturae of Linnaeus (به عنوان Marmor fugax).
- دیلامتری، جی.سی. (1812) Leçons de minéralogie. 8vo، پاریس: جلد 2: 380 (به عنوان Montmartrite).
- Reuss (1869) Annalen der Physik, Halle, Leipzig: 136: 135.
- Baumhauer (1875) Akademie der Wissenschaften، مونیخ، Sitzber.: 169.
- Beckenkamp (1882) Zeitschrift für Kristallographie، Mineralogie und Petrographie، لایپزیگ: 6: 450.
- Mügge (1883) Neues Jahrbuch für Mineralogie, Geologie und Paleontologie, Heidelberg, Stuttgart: II: 14.
- Reuss (1883) Akademie der Wissenschaften، برلین (Sitzungsberichte der): 259.
- Mügge (1884) Neues Jahrbuch für Mineralogie, Geologie und Paleontologie, Heidelberg, Stuttgart: I: 50.
- Des Cloizeaux (1886) Bulletin de la Société française de Minéralogie: 9: 175.
- دانا، E.S. (1892) سیستم کانی شناسی، ششم. نسخه، نیویورک: 933.
- Auerbach (1896) Annalen der Physik, Halle, Leipzig: 58: 357.
- Viola (1897) Zeitschrift für Kristallographie، Mineralogie und Petrographie، لایپزیگ: 28: 573.
- Mügge (1898) Neues Jahrbuch für Mineralogie, Geologie und Paleontologie, Heidelberg, Stuttgart: I: 90.
- Tutton (1909) Zeitschrift für Kristallographie، Mineralogie und Petrographie، لایپزیگ: 46: 135.
- Berek (1912) Jahrbuch Minerl., Beil.-Bd.: 33: 583.
- هاچینسون و تاتون (1913) Zeitschrift für Kristallographie، Mineralogie und Petrographie، لایپزیگ: 52: 223.
- کراوس و یانگ (1914) Centralblatt für Mineralogie, Geologie und Paleontologie, Stuttgart: 356.
- Grengg (1915) Mineralogische und petrographische Mitteilungen، وین: 33: 210.
- Rosický (1916) Ak. سسکا، رز.، کل. 2:25: نه. 13.
- Goldschmidt, V. (1918) Atlas der Krystallformen. 9 جلد، اطلس و متن: ج. 4:93.
- Gaudefroy (1919) Bulletin de la Société française de Minéralogie: 42: 284.
- ریچاردسون (1920) مجله کانی شناسی: 19: 77.
- Gross (1922) Zeitschrift für Kristallographie, Mineralogie und Petrographie, Leipzig: 57: 145.
- ملور، جی دبلیو. (1923) رساله ای جامع درباره شیمی معدنی و نظری. 16 جلد، لندن: 3: 767.
- Carobbi (1925) Ann. R. Osservat. وزوویانو: 2:125.
- دامر و تیتزه (1927) Die nutzbaren mineralien، اشتوتگارت، 2nd. نسخه.
- فوشگ (1927) کانی شناس آمریکایی: 12: 252.
- هیمل (1927) Centralblatt für Mineralogie, Geologie und Paleontologie, Stuttgart: 342.
- Matsuura (1927) مجله ژاپنی زمین شناسی و جغرافیا: 4: 65.
- Nagy (1928) Zeitschrift für Physik، برانزویک، برلین: 51: 410.
- Berger, et al (1929) Akademie der Wissenschaften, Leipzig, Ber.: 81: 171.
- هینتزه، کارل (1929) Handbuch der Mineralogie. برلین و لایپزیگ 6 جلد: 1, 4274. (محلات)
- Ramsdell and Partridge (1929) کانی شناس آمریکایی: 14:59.
- Josten (1932) Centralblatt für Mineralogie, Geologie und Paleontologie, Stuttgart: 432.
- پارسونز (1932) مطالعات دانشگاه تورنتو، سری زمین شناسی، شماره. 32:25.
- Gallitelli (1933) Periodico de Mineralogia-Roma: 4: 132.
- Gaubert (1933) Comptes redu de l'Académie des Sciences de Paris: 197: 72.
- بلیانکین و فئودوتیف (1934) Trav. inst. پتروگ ac sc U.R.S.S.، شماره 6:453.
- کاسپاری (1936) مجموعه مقالات انجمن سلطنتی لندن: 155A: 41.
- Terpstra (1936) Zeitschrift für Kristallographie، Mineralogie und Petrographie، لایپزیگ: 97: 229.
- ویزر و همکاران (1936) مجله آمریکاییانجمن شیمی: 58: 1261.
- Wooster (1936) Zeitschrift für Kristallographie، Mineralogie und Petrographie، لایپزیگ: 94: 375.
- Büssem and Gallitelli (1937) Zeitschrift für Kristallographie, Mineralogie und Petrographie, Leipzig: 96: 376.
- Gossner (1937) Forschritte der Mineralogie, Kristallographie und Petrographie, Jena: 21: 34.
- Gossner (1937) Zeitschrift für Kristallographie، Mineralogie und Petrographie، لایپزیگ: 96: 488.
- هیل (1937) مجله انجمن شیمی آمریکا: 59: 2242.
- د یونگ و بومان (1938) Zeitschrift für Kristallographie, Mineralogie und Petrographie, Leipzig: 100: 275.
- Posnjak (1939) مجله آمریکایی علوم: 35: 247.
- توکودی (1939) آن. Mus. نات. مجارستان، حداقل جئول پال.: 32: 12.
- تورتسف (1939) بول. آکادمی علوم U.S.S.R., Ser. جیول.، نه. 4:180.
- هاف (1940) مجله زمین شناسی: 48: 641.
- Acta Crystallographica: B38: 1074-1077.
- Bromehead (1943) مجله کانی شناسی: 26: 325.
- میروپلسکی و بورویک (1943) Comptes rendus de l’académie des Sciences de U.R.S.S.: 38: 33.
- برگ و سوشنیکوا (1946) بول. ac sc U.R.S.S.: 51: 535.
- Palache, C., Berman, H., & Frondel, C. (1951), The System of Mineralogy of James Dwight Dana and Edward Salisbury Dana, Yale University 1837-1892, Volume II. جان وایلی و پسران، شرکت، نیویورک، چاپ هفتم، بازبینی و بزرگنمایی شده، 1124 ص: 481-486.
- گرووز، A.W. (1958)، گچ و انیدریت، 108 ص. سازمان زمین شناسی خارج از کشور، لندن.
- هاردی، لس آنجلس (1967)، تعادل گچ-انیدریت در یک فشار اتمسفر: کانی شناس آمریکایی: 52: 171-200.
- گینز، ریچارد وی، اچ. کاترین، دبلیو. اسکینر، یوجین ای. فورد، برایان میسون، آبراهام روزنزوایگ (1997)، کانی شناسی جدید دانا: سیستم کانی شناسی جیمز دوایت دانا و ادوارد سالزبری دانا، ویرایش هشتم: 598 .
- Sarma، L.P.، P.S.R. Prasad و N. Ravikumar (1998)، طیفسنجی رامان انتقال فاز در گچ طبیعی: مجله طیفسنجی رامان: 29: 851-856.
GYPSUM - 1. Ca·2H 2 O. Mon. قرص های نازک و ضخیم. Sp. V. جغدها توسط (010)، جغد. توسط (100) و (110). Dv. مطابق (100) معمول - دم کبوتر. Ag.: دانه ای، برگی، پودری، فیبری، رگه ای، شعاعی سوزنی شکل. بی رنگ، سفید، زرد تا سیاه. Bl. شیشه. تلویزیون 1.5-2. Ud. V. 2.32. انعطاف پذیر اما کشسان نیست. به طور قابل توجهی در آب حل می شود. محاصره تشکیل می دهد. g.p. اغلب در اکسید شده ذخایر سنگ معدن؛ هیدروترم شناخته شده زمانی تشکیل شد تی 63.5 درجه سانتی گراد،
و در محلول های اشباع شده با NaCl، در تی 30 درجه سانتیگراد؛ در طول هیدراتاسیون انیدریت و همچنین تحت تأثیر محلولهای سولفات بر روی خاکهای کربناته در دوران مدرن. باس آب شور سولفات کلسیم به شکل گچ رسوب میکند؛ در زمانهای قدیم، تشکیلات عمدتاً انیدریتی و کمتر متداولتر از گچ شناخته میشد. مختلف: کریستالی G.; فیبر یا ؛ دانه دار یا شنی - poikilitic. 2. محاصره. g.p.، که عمدتاً از توده گچ تشکیل شده و در گرم گنجانده شده است. اقلام هالوژن با توجه به شرایط تشکیل، گاز می تواند اولیه (خود رسوب) باشد که به صورت شیمیایی تشکیل شده است. رسوب گذاری در حوضه های شور شده در مراحل اولیه هالوژنز،یا ثانویه دومی شامل هیدروکربن های توسعه یافته است که در طول هیدراتاسیون انیدریت در منطقه نزدیک به سطح ایجاد می شود: کلاه گچی;گچ متاسوماتیک (نمونه اصلی اقلام کربناته) و غیره گچ به صورت خام و کلسینه شده در صنعت ساختمان سازی، در تولید بایندر، گچ و گچ قالب گیری، استریش گچ، سیمان گچ و برای تولید گوگرد استفاده می شود.
فرهنگ لغت زمین شناسی: در 2 جلد. - م.: ندرا. ویرایش شده توسط K. N. Paffengoltz و همکاران.. 1978 .
(از یونانی gypsos -، آهک * آ.گچ؛ nگیپس؛ f.گچ، پیر و پلاتر؛ و.بله اوه) -
1)
کانی از کلاس سولفات، Ca(SO 4) 2H 2 O. به شکل خالص حاوی 32.56٪ CaO، 46.51٪ SO 3 و 20.93٪ H 2 O. مکانیکی است. ناخالصی ها چ. arr به صورت مواد آلی و رسی، سولفیدها و ... در سیستم مونوکلینیک متبلور می شود. اساس کریستالی است. ساختارها - دو گروه آنیونی (SO 4) 2-، متصل شده توسط کاتیون های Ca2 +. کریستال ها جدولی یا منشوری هستند که دوقلوها را تشکیل می دهند که به اصطلاح می گویند. دم کبوتر بسیار عالی. سنگدانه ها: دانه ای، برگی، پودری، ندول، رگه های فیبری، شعاعی سوزنی. جی خالص بی رنگ و شفاف است و در صورت وجود ناخالصی به رنگ خاکستری، زرد، صورتی، قهوه ای تا سیاه است. درخشش شیشه. تلویزیون 1.5-2. 2300 کیلوگرم بر متر مکعب. به طور قابل توجهی در آب حل می شود (2.05 گرم در لیتر در 20 درجه سانتی گراد). با توجه به منشأ چ. arr شیمیایی در دمای 63.5 درجه سانتیگراد و در محلولهای اشباع شده با NaCl - در دمای 30 درجه سانتیگراد رسوب می کند. وقتی یعنی. افزایش شوری در دریاهای در حال خشک شدن در تالاب ها و دریاچه های نمک، به جای هیدروکربن ها، سولفات بی آب، انیدریت شروع به رسوب می کند که به طور مشابه زمانی که هیدروکربن ها کم آب می شوند ظاهر می شود.هیدروژن همچنین در رسوبات سولفیدی با دمای پایین تشکیل می شود. انواع: سلنیت - سنگدانه های الیافی نیمه شفاف، ریخته شده در نور منعکس شده با درخشش ابریشمی زیبا. گچ اسپار - گچ لایه ای به شکل بلورهای شفاف ساختار لایه ای و غیره.
.
2)
فورج رسوبی نژاد، شامل عمدتا از کانی G. و ناخالصی ها (آهن، انیدریت، هیدروکسیدهای آهن، گوگرد و غیره). با توجه به شرایط تشکیل، گاز می تواند اولیه باشد که با روش های شیمیایی تشکیل می شود. ته نشینی در استخرهای شور در ابتدا. مراحل هالوژنز، یا ثانویه، ناشی از هیدراتاسیون انیدریت در منطقه نزدیک به سطح - کلاه گچی، متاسوماتیک. G. و دیگران کیفیت مواد خام گچ عمدتا تعیین می شود. محتوای سولفات کلسیم دی هیدرات (CaSO 4 · 2H 2 O)، در تجزیه. انواع سنگ گچ از 70 تا 90 درصد متغیر است.
G. به صورت خام و سوخته استفاده می شود. 50-52 درصد از سنگ گچ استخراج شده در اتحاد جماهیر شوروی برای تولید چسب گچ و غیره استفاده می شود. هدف (GOST 195-79)، به دست آمده از پخت گرم طبیعی، 44٪ گرم - در تولید سیمان پرتلند، که در آن گرم به عنوان یک افزودنی (3-5٪) برای تنظیم زمان گیرش سیمان استفاده می شود. و همچنین برای تولید ویژه. سیمان: سیمان منبسط کننده گچ- آلومینا، سیمان کششی و غیره. 2.5% از G. مصرف pp. برای تولید کودهای نیتروژن (سولفات آمونیوم) و برای خاکهای شور گچ. در متالورژی غیر آهنی، g به عنوان یک شار، عمدتا استفاده می شود. در ذوب نیکل؛ در تولید کاغذ - به عنوان پرکننده، در درجه اول. در بالاترین درجات مقاله تحریر. در برخی از کشورها (بریتانیا و غیره) از G. برای تولید اسید سولفوریک و سیمان استفاده می شود. توانایی G. در پردازش آسان، پولیش خوب و معمولاً دارای خواص تزئینی بالا، استفاده از آن را به عنوان شبیه ساز سنگ مرمر در تولید صفحات روکش برای کاربردهای داخلی ممکن می سازد. تکمیل ساختمان ها و به عنوان ماده ای برای تجزیه. صنایع دستی
به سمت جنوب مناطق اتحاد جماهیر شوروی در مردم. x-we از گچ رسی با محتوای CaSO 4 · 2H 2 O از 40 تا 90 درصد استفاده می کند. سنگ سست متشکل از خاک رس و ماسه به نام. خاکی G.، و در ماوراء قفقاز و Wed. آسیا - "" یا "گانچ". این سنگ ها به صورت خام برای گچ کاری خاک ها و به صورت کلسینه شده برای گچ کاری به عنوان قابض استفاده می شود.
در اتحاد جماهیر شوروی، بزرگترین ذخایر در مناطق Donbass، Tula، Kuibyshev، Perm RSFSR، در قفقاز و در خاورمیانه قرار دارد. آسیا. در 150 کانسار G. و 22 کانسار گچ رسی، دیواره خشک و گانچ، اکتشاف صنعتی انجام شده است. ذخایر دسته 4.2 میلیارد تن (1981). 11 ذخایر وجود دارد که ذخایر گچ آنها بیش از 50 میلیون تن است (از جمله Novomoskovskoye - 857.4 میلیون تن).
ذخایر زمین شناسی توسط معادن (مجتمع های صنعتی شدوکسکی، ساوریشسکی و غیره) و معادن (نووموسکوفسکی، آرتیوموفسکی، کامسکویه اوستیه و غیره) توسعه می یابند. در اتحاد جماهیر شوروی، 42 کانسار گچ و انیدریت و 6 کانسار سنگ گچ دار با تولید سالانه حدوداً بهره برداری می شود. 14 میلیون تن (1981)، که 60.2٪ - در قلمرو. RSFSR و 15.8٪ - اوکراین SSR. بزرگترین شرکت ها عبارتند از Novomoskovsky (2.33 میلیون تن)، Ergachinsky، Artyomovsky (هر کدام 1.0 میلیون تن) و Zalarinsky (0.85 میلیون تن).
ذخایر اثبات شده هیدروکربن های جهان 2.2 میلیارد تن برآورد شده است: 0.6 میلیارد تن در ایالات متحده آمریکا. 0.375 میلیارد تن در کانادا؛ 0.825 میلیارد تن در کشورهای اروپایی (فرانسه، آلمان، اسپانیا، ایتالیا، یوگسلاوی و یونان)؛ 0.09 میلیارد تن در کشورهای آسیایی؛ هر کدام 0.07 میلیارد تن در مکزیک و کشورهای آفریقایی. منابع گرجستان چندین برابر ذخایر اثبات شده آن است. تولید جهانی گاز در میان سرمایه داران. کشور 70 میلیون تن (1978) است که ایالات متحده آمریکا 20٪ (13.5 میلیون تن) و کانادا - 11٪ (7.9 میلیون تن) را تشکیل می دهد. در کشورهای اروپایی، 30.7 میلیون تن استخراج می شود، در آسیا - 11.9 میلیون تن. ادبیات: Vinogradov B.N.، پایه مواد اولیه صنعت کلاسورهای اتحاد جماهیر شوروی، M.، 1971; ویختر یا آی، تولید صحافی گچی، چاپ چهارم، م.، 1974. یو اس میکوشا.
دایره المعارف کوهستان. - م.: دایره المعارف شوروی. ویرایش شده توسط E. A. Kozlovsky. 1984-1991 .
مترادف ها:ببینید "Gypsum" در سایر لغت نامه ها چیست:
گچ- گچ و ... فرهنگ لغت املای روسی
گچ- گچ /… فرهنگ لغت صرفی- املا
گچ- – (از یونانی gypsos – گچ، آهک) – 1) گرم طبیعی – معدنی، سولفات کلسیم آبی CaSO4*2H2O. رنگ سفید، زرد، کرم؛ اغلب بی رنگ تلویزیون در کانی شناسی، مقیاس 1.5 - 2. متراکم 2300 کیلوگرم بر متر مکعب. متشکل از ch. ارر... دایره المعارف اصطلاحات، تعاریف و توضیحات مصالح ساختمانی- (ترکمنستان). گچ (از یونانی گچ گچ، آهک)، 1) معدنی، سولفات کلسیم آبی. بلورهای بی رنگ، خاکستری، سنگدانه ها. سختی 1.5 2; چگالی 2.3 گرم بر سانتی متر مکعب انواع: اسپار گچ (کریستال های شفاف)؛ ساتن اسپار یا ...... فرهنگ لغت دایره المعارف مصور
گچ- سنگ گچ، سولفات کلسیم، کلسیم سولفوریکوم، CaS04+2H20، یک ماده معدنی سفید نرم و به راحتی پودر می شود که در طبیعت به شکل رسوبات بزرگ یافت می شود. به طور مصنوعی از اثر اسید سولفوریک یا نمک های محلول در آب آن به دست می آید... ... دایره المعارف بزرگ پزشکی
- (از آهک گچ یونانی gypsos)، 1) کانی از کلاس سولفات، CaSO4.2H2O. بلورهای بی رنگ، سفید، خاکستری، سنگدانه ها. سختی 1.5 2; چگالی 2.3 g/cm³. انواع: اسپار گچ (کریستال های شفاف)؛ ساتن اسپار یا اورال... ... فرهنگ لغت دایره المعارفی بزرگ
گچ، گچ، مرد. (به یونانی: gypsos). 1. فقط واحد نمک معدنی کریستالی گوگرد آهک ب. قطعات سفید یا رنگ زرد، استفاده شده از جمله، در جراحی و خدمت به عنوان مواد برای آثار مجسمه سازی (معدنی). 2. بازیگران مجسمه سازی از... ... فرهنگ توضیحی اوشاکوف
گچ
گچ (eng. Gypsum) - معدنی، سولفات آبی کلسیم. ترکیب شیمیایی- Ca × 2H 2 O. سیستم مونوکلینیک. ساختار کریستالی لایه لایه است. دو ورقه از گروه های 2- آنیونی، نزدیک به یون های Ca2+، لایه های دوتایی را در امتداد صفحه (010) تشکیل می دهند. مولکول های H 2 O فضاهای بین این لایه های دوگانه را اشغال می کنند. این به راحتی ویژگی برش بسیار عالی گچ را توضیح می دهد. هر یون کلسیم توسط شش یون اکسیژن متعلق به گروه SO 4 و دو مولکول آب احاطه شده است. هر مولکول آب یک یون کلسیم را به یک یون اکسیژن در همان دولایه و به یون اکسیژن دیگر در لایه مجاور متصل می کند.
خواص
رنگ آن متفاوت است، اما معمولاً سفید، خاکستری، زرد، صورتی و غیره. کریستال های شفاف خالص بی رنگ هستند. ناخالصی ها را می توان در رنگ های مختلف رنگ آمیزی کرد. رنگ خط تیره سفید است. درخشش کریستال ها شیشه ای است، گاهی اوقات با رنگ مرواریدی به دلیل ریزترک های شکاف کامل. در سلنیت ابریشمی است. سختی 2 (استاندارد مقیاس موهس). رخ در یک جهت بسیار عالی است. کریستال های نازک و صفحات همجوشی انعطاف پذیر هستند. چگالی 2.31 - 2.33 g/cm3.
حلالیت قابل توجهی در آب دارد. ویژگی قابل توجه گچ این است که حلالیت آن با افزایش دما در 37-38 درجه به حداکثر می رسد و سپس به سرعت کاهش می یابد. بیشترین کاهش حلالیت در دماهای بالاتر از 107 درجه به دلیل تشکیل "همی هیدرات" - CaSO 4 × 1/2H 2 O رخ می دهد.
در دمای 107 درجه سانتیگراد، تا حدی آب را از دست می دهد و به پودر آلاباستر سفید (2CaSO 4 × H 2 O) تبدیل می شود که به طور قابل توجهی در آب محلول است. به دلیل تعداد کمتر مولکول های هیدراتاسیون، آلاباستر در طی پلیمریزاسیون منقبض نمی شود (تقریباً 1 درصد حجم آن افزایش می یابد). زیر مورد tr. آب را از دست می دهد، شکافته می شود و به مینای سفید تبدیل می شود. روی زغال سنگ در شعله کاهنده، CaS تولید می کند. در آب اسیدی شده با H 2 SO 4 بسیار بهتر از آب خالص حل می شود. با این حال، در غلظت H 2 SO 4 بالاتر از 75 گرم در لیتر. حلالیت به شدت کاهش می یابد. بسیار کمی در HCl محلول است.
اشکال مکان
کریستال ها، به دلیل رشد غالب چهره ها (010)، ظاهری جدولی، به ندرت ستونی یا منشوری دارند. از بین منشورها، رایج ترین آنها (110) و (111)، گاهی اوقات (120) و غیره است. وجه های (110) و (010) اغلب دارای جوجه کشی عمودی هستند. دوقلوهای فیوژن رایج هستند و در دو نوع هستند: 1) گالی (100) و 2) پاریسی (101). تشخیص آنها از یکدیگر همیشه آسان نیست. هر دوی آنها شبیه دم کبوتر هستند. دوقلوهای گالی با این واقعیت مشخص می شوند که لبه های منشور m (110) به موازات صفحه دوقلو قرار دارند و لبه های منشور l (111) یک زاویه بازگشتی را تشکیل می دهند، در حالی که در دوقلوهای پاریسی لبه های منشور Ι (111) موازی با درز دوقلو هستند.
این به شکل کریستال های بی رنگ یا سفید و رشدهای درونی آنها، گاهی اوقات توسط آخال ها و ناخالصی های جذب شده توسط آنها در طول رشد به رنگ های قهوه ای، آبی، زرد یا قرمز رنگ می شود. مشخصه رشدهای درونی به شکل "رز" و دوقلوها - به اصطلاح. "دم چلچله ها"). رگههایی از ساختار الیافی موازی (سلنیت) در سنگهای رسوبی رسی، و همچنین سنگدانههای ریزدانه متراکم و پیوسته شبیه سنگ مرمر (آلباستر) را تشکیل میدهد. گاهی به صورت سنگدانه های خاکی و توده های کریپتوکریستالی. همچنین سیمان ماسه سنگ را تشکیل می دهد.
شبه شکلهای کلسیت، آراگونیت، مالاکیت، کوارتز و غیره روی گچ رایج هستند، مانند شبهمورفوسهای گچ روی سایر کانیها.
اصل و نسب
یک کانی گسترده است که در شرایط طبیعی به روش های مختلف تشکیل می شود. منشا رسوبی (رسوب شیمیایی شیمیایی دریایی معمولی)، هیدروترمال با دمای پایین است که در غارهای کارستی و سولفاتاراها یافت می شود. در طول خشک شدن تالاب های دریایی و دریاچه های نمک از محلول های آبی غنی از سولفات رسوب می کند. در میان سنگ های رسوبی لایه ها، لایه های میانی و عدسی هایی را تشکیل می دهد که اغلب در ارتباط با انیدریت، هالیت، سلستین، گوگرد بومی، گاهی با قیر و روغن. به مقدار قابل توجهی از طریق رسوب گذاری در استخرهای مرگبار دارای نمک دریاچه و دریا ته نشین می شود. در این حالت، گچ همراه با نمک طعام تنها در مراحل اولیه تبخیر، زمانی که غلظت سایر نمک های محلول هنوز بالا نیست، آزاد می شود. هنگامی که به غلظت معینی از نمک ها، به ویژه NaCl و به ویژه MgCl 2 رسید، انیدریت به جای گچ و سپس سایر نمک های محلول تر، به عنوان مثال، متبلور می شود. گچ در این حوضه ها باید متعلق به رسوبات شیمیایی قبلی باشد. در واقع، در بسیاری از نهشتههای نمک، لایههایی از گچ (و همچنین انیدریت)، با لایههایی از سنگ نمک، در قسمتهای پایینی نهشتهها قرار دارند و در برخی موارد تنها توسط سنگهای آهکی رسوبشده شیمیایی زیر آن قرار میگیرند.
توده های قابل توجهی از گچ در سنگ های رسوبی عمدتاً در نتیجه هیدراتاسیون انیدریت تشکیل می شوند که به نوبه خود در طی تبخیر آب دریا رسوب می کنند. اغلب، هنگام تبخیر، گچ مستقیماً رسوب می کند. گچ در نتیجه هیدراته شدن انیدریت در رسوبات تحت تأثیر آبهای سطحی در شرایط فشار خارجی کم (به طور متوسط تا عمق 100-150 متر) بر اساس واکنش ایجاد می شود: CaSO 4 + 2H 2 O = CaSO 4 × 2H 2 O. در این مورد، افزایش شدید حجم (تا 30٪) و در ارتباط با این، اختلالات محلی متعدد و پیچیده در شرایط وقوع اقشار گچ دار. به این ترتیب، بیشتر ذخایر بزرگ گچ روی کره زمین به وجود آمد. در حفره های توده های جامد گچی، گاهی اوقات لانه هایی از بلورهای بزرگ و اغلب شفاف یافت می شود.
می تواند به عنوان سیمان در سنگ های رسوبی عمل کند. گچ رگه ای معمولاً محصول واکنش محلول های سولفاتی (که در اثر اکسیداسیون کانی های سولفیدی به وجود می آید) با سنگ های کربناته است. در سنگهای رسوبی در طی هوازدگی سولفیدها، تحت تأثیر اسید سولفوریک تشکیل شده در هنگام تجزیه پیریت به مارن و رسهای آهکی تشکیل می شود. در مناطق نیمه بیابانی و بیابانی، گچ اغلب به صورت رگه ها و گره هایی در پوسته هوازدگی سنگ ها با ترکیبات مختلف یافت می شود. در خاک های منطقه خشک، تشکیلات جدیدی از گچ ثانویه رسوب داده شده تشکیل می شود: تک بلورها، دوقلوها ("دم چلچله")، دروس، "رز گچی" و غیره.
گچ کاملاً در آب حل می شود (تا 2.2 گرم در لیتر) و با افزایش دما ابتدا حلالیت آن افزایش می یابد و بالاتر از 24 درجه سانتی گراد کاهش می یابد. به همین دلیل گچ وقتی از آب دریا رسوب می کند از هالیت جدا شده و لایه های مستقلی را تشکیل می دهد. در نیمه بیابان ها و بیابان ها با هوای خشک، تغییرات شدید دمای روزانه، خاک های شور و پر از گچ، صبح ها با افزایش دما، گچ شروع به حل شدن می کند و با بالا آمدن در محلول توسط نیروهای مویرگی، بر روی زمین رسوب می کند. سطح با تبخیر آب در عصر، با کاهش دما، کریستالیزاسیون متوقف می شود، اما به دلیل کمبود رطوبت، کریستال ها حل نمی شوند - در مناطقی با چنین شرایطی، کریستال های گچ به ویژه در مقادیر زیاد یافت می شود.
محل
در روسیه، اقشار ضخیم دارای گچ با سن پرمین در سراسر اورال غربی، در باشقیر و تاتارستان، در آرخانگلسک، ولوگدا، گورکی و سایر مناطق توزیع شده است. کانسارهای متعددی از سن ژوراسیک بالایی در شمال ایجاد شده است. قفقاز، داغستان. نمونههای مجموعهای قابل توجه با کریستالهای گچ از کانسار گاوردک (ترکمنستان) و ذخایر دیگر در آسیای مرکزی (در تاجیکستان و ازبکستان)، در منطقه ولگای میانه، در خاکهای ژوراسیک منطقه کالوگا شناخته شدهاند. در غارهای حرارتی معدن نایکا (مکزیک)، دانههایی از کریستالهای گچ با اندازه منحصر به فرد به طول 11 متر یافت شد.
کاربرد
سنگ گچ فیبری (سلنیت) به عنوان سنگ زینتی برای جواهرات ارزان قیمت استفاده می شود. از زمان های قدیم، جواهرات بزرگ - وسایل داخلی (گلدان، رومیزی، جوهردان و غیره) از آلاباستر ساخته شده است. گچ سوخته برای ریخته گری و قالب گیری (نقشه برجسته، قرنیز و غیره) به عنوان ماده اتصال دهنده در ساختمان سازی و پزشکی استفاده می شود.
برای تولید گچ ساختمانی، گچ با مقاومت بالا، مواد چسباننده گچ-سیمان-پوزولانی استفاده می شود.
- گچ همچنین نامی است که به سنگ های رسوبی که عمدتاً از این کانی تشکیل شده است، داده می شود. منشا آن تبخیری است.
گچ (eng. GYPSUM) - سیآاسO 4 2اچ 2 O
نام های دیگر، انواع
اسپار ابریشمی،
الینیت اورال،
اسپار گچ،
شیشه دوشیزه یا مارینو
- انگلیسی - گچی
- عربی - جص
- بلغاری - گچ
- مجارستانی – Gipsz
- هلندی - گیپس
- یونانی - Γύψος
- دانمارکی - گیپس
- عبری - גבס
- اسپانیایی - Yeso;Gypsita;Oulopholita
- ایتالیایی - Gesso؛ Acidovitriolosaturata؛ Geso
- کاتالان - گیکس
- کره ای - 석고
- لتونی – Ģipsis
- لاتین - گچی
- لیتوانیایی – گیپساس
- آلمانی - Gips; Atlasgips; Gipsrose; Gyps; Gypsit; Oulopholit
- لهستانی - گیپس
- پرتغالی - گیپسیتا
- رومانیایی – گیپس
- روسی – گچ
- اسلواکی – Sadrovec
- اسلوونیایی – سادرا
- فرانسوی - Gypse; Chaux sulfatée
- کرواتی – گیپس
- چک – سادرووچ
- سوئدی - گیپس
- اسپرانتو - Gipsoŝtono;Gipso
- استونیایی – کیپس
- ژاپنی - 石膏
نام:گچ
رنگ:بی رنگ تبدیل به سفید، اغلب توسط مواد معدنی ناخالص رنگ زرد، صورتی، قرمز، قهوه ای، و غیره. گاهی اوقات رنگ آمیزی بخش-منطقه ای یا توزیع اجزاء در مناطق رشد در داخل کریستال ها مشاهده می شود. بی رنگ در رفلکس های داخلی و با چشم غیر مسلح..
هدف کار: آشنایی با ابزار و روش های مطالعه گچ.
تجهیزات و مواد:فشار هیدرولیکی، دستگاه ویکا، لیوان و کاردک تهیه خمیر گچی، ترازو الکترونیکی، دستگاه سوتارتا، الک شماره 02، خط کش، کرونومتر، گچ.
مقررات ایمنی:برای محافظت از چشم در برابر اجسام خارجی کار آزمایشگاهیاستفاده از عینک ایمنی
بخش تئوری
چسب های معدنیمواد پودری به طور مصنوعی تولید می شوند که در صورت مخلوط شدن با آب، یک ماده پلاستیکی تشکیل می دهند که در نتیجه فرآیندهای فیزیکی و شیمیایی قادر به سفت شدن است، یعنی به حالت سنگ مانند تبدیل می شود. چسب های معدنی ساختمانی به سه دسته تقسیم می شوند:
چسب های هوا(آهک، گچ) با این واقعیت مشخص می شود که وقتی با آب مخلوط می شوند، سخت می شوند و فقط در مدت طولانی استحکام خود را حفظ می کنند. محیط هوا . اگر به طور سیستماتیک مرطوب شوند، قدرت خود را از دست داده و فرو می ریزند.
کلاسورهای هیدرولیک(سیمان پرتلند) با این واقعیت مشخص می شود که پس از اختلاط با آب و سخت شدن اولیه در هوا قابلیت سخت شدن بیشتر هم در هوا و هم در داخل محیط آبی، در حالی که قدرت آنها افزایش می یابد.
بایندرهای مقاوم در برابر اسید(سیمان فلوئوروسیلیکات کوارتز مقاوم به اسید) مخلوطی ریز آسیاب شده از ماسه کوارتز و فلوئوروسیلیکات سدیم است که با محلول آبی سیلیکات سدیم یا پتاسیم مخلوط شده است. این چسب ابتدا در هوا برای مدت طولانی سفت می شود مقاومت در برابر اثرات تهاجمی اسیدهای معدنی و آلی به جز هیدروژن فلوراید.
1. کلاسورهای هوا. گچ
چسباننده گچیآنها به 2 گروه تقسیم می شوند: کم آتش و پرتاب.
کم آتش چسباننده گچ با حرارت دادن دی هیدرات گچ (CaSO4*2H2O) تا دمای 150...160 درجه سانتی گراد به دست می آید. در این مورد، کم آبی جزئی گچ دو آب با انتقال آن به گچ نیمه آب رخ می دهد: CaSO4*2H2O → CaSO4*0.5H2O +l.5H2O. چسباننده های کم سوز عبارتند از: ساخت و ساز، قالب گیری، گچ با مقاومت بالا و طبی.ماده اولیه برای تولید بایندرهای کم سوز، سنگ گچ طبیعی (CaSO) است 4 *2H2O،) و همچنین ضایعات صنعتی حاوی سولفات کلسیم -CaSO4.
با شلیک بالاچسباننده (انیدریت).حرارتی دریافت کنید
با پختن دی هیدرات گچ (CaSO4*2H2O) در دمای بالاتر - 600...900 درجه سانتی گراد در این حالت دی هیدرات گچ به طور کامل آب متصل شده شیمیایی را از دست می دهد و در نتیجه سولفات کلسیم آبی - انیدرید CaSO4 تشکیل می شود.
چسباننده های با سوزش بالا عبارتند از: انیدریت ce-
ment و erich-gepsum.
ماده اولیه برای تولید بایندرهای پر سوز انیدریت است CaSO4و همچنین زباله های صنعتی حاوی سولفات کلسیم -CaSO4.
گچ ساختمانی. گچ ساختمانی یا آلاباستر
(GOST 125-79) به نام چسبنده هوا که با عملیات حرارتی به دست می آید دی هیدرات گچ طبیعی - سولفات کلسیم CaSO4*2H20 در دمای 150 - 180 درجه سانتیگراد تا تبدیل به گچ نیمه آب - سولفات کلسیم شود. CaSO 4*0.5H2Oو به دنبال آن آسیاب به پودر ریز تبدیل می شود:
تولید گچ ساختمانیشامل خرد کردن، تن-
آنها سنگ زنی و عملیات حرارتی سنگ گچ.
2 روش برای تولید گچ ساختمانی وجود دارد:
در حین شلیک در دستگاه باز که با اتمسفر در دمای 150-160 درجه سانتیگراد ارتباط برقرار می کند، زمانی که آب به صورت بخار از مواد خام خارج می شود و چسب های گچ عمدتاً از کریستال های کوچک تشکیل شده است. β - اصلاحات
در آسیاب های شفت یا هوا و سپس پخت محصول خرد شده در دمای 100 درجه سانتیگراد در دیگ های گچی یا کوره ها.
گچ ساختمانی (نیمه آبی) پودری سفید یا خاکستری است. رنگ گچ به میزان ناخالصی سنگ گچ و تمیزی پخت بستگی دارد. در تولید گچ، جایز است
از معرفی مواد افزودنی به منظور تنظیم زمان گیرش و بهبود خواص فیزیکی و مکانیکی گچ خودداری می کند.
یاد آوردن! - فرمول گچ ساختمانی - CaSO4*0.5H2O. فرمول دی هیدرات گچ طبیعی (که از آن گچ ساختمانی به دست می آید): CaSO4*2H2O.
واکنش برای تولید گچ ساختمانی:
CaSO4*2H2O→ CaSO4*0.5H2O +l.5H2O.
ارزیابی کیفیت گچ ساختمانی
کیفیت گچ ساختمان با شاخص های زیر تعیین می شود:
با توجه به ظرافت آسیاب؛
با توجه به ضخامت معمولی خمیر گچ؛
با توجه به زمان تنظیم؛
مقاومت فشاری.
بسته به کیفیت، گچ ساختمانی می تواند دو درجه باشد، جدول 4.1 را ببینید.
جدول 4.1 - انواع کیفیت گچ
بسته به درجه سنگ زنی، گچ ساختمانی دارای سه گروه است (جدول 4.2).
جدول 4.2 - گروه های گچ بر اساس درجه آسیاب
بسته به زمان گیرش، گچ ساختمانی دارای سه گروه است (جدول 4.3).
جدول 4.3 - گروه های گچ ساختمانی بسته به زمان گیرش
بسته به استحکام کششی، گچ دارای درجات زیر است (جدول 4.4).
جدول 4.4 - درجه های گچ بسته به مقاومت فشاری و خمشی نمونه
| درجه گچ | استحکام کششی بر حسب MPa، نه کمتر | برند گچ | برند گچ | استحکام کششی بر حسب MPa، نه کمتر | ||||
| در طول فشرده سازی | هنگام خم شدن | در طول فشرده سازی | هنگام خم شدن | در طول فشرده سازی | هنگام خم شدن | |||
| G-2 | 1,2 | G-6 | 5,0 | G-16 | 6,0 | |||
| G-3 | 1,8 | G-7 | 3,5 | G-19 | 6,5 | |||
| G-4 | 2,0 | G-10 | 4,5 | G-22 | 7,0 | |||
| G-5 | 2,5 | G-13 | 5,5 | G-25 | 8,0 |
گیرش و سفت شدن گچ ساختمانی. گیرش و سفت شدن گچ ساختمانی به این صورت است که گچ با آب مخلوط می شود خمیر پلاستیکی را تشکیل می دهد که سپس به بدنه ای سنگ مانند با استحکام خاصی تبدیل می شود. واکنش اصلی فرآیند به شکل زیر است:
CaSO4*0.5H2O +l.5H2O = CaSO4*2H2O.
در این حالت کریستال های هیپو هیدروژن از محلول آزاد می شود.
sa و برافزایش آنها. فرآیند سخت شدن گچ را می توان با خشک کردن در دمای زیر 65 درجه تسریع کرد.
شروع گیرش گچ نباید زودتر از 6 دقیقه اتفاق بیفتد. و حداکثر 30 دقیقه پس از شروع مخلوط کردن با آب. زمان گیرش و سخت شدن را می توان با معرفی NaCl، KCl، NaNO و سایر موادی که حلالیت را تغییر می دهند تنظیم کرد. CaSO4*0.5H2O در آب .
گچ قالب گیری . این گچ با ساخت و ساز متفاوت است
سنگ گچ ریزتر، استحکام بیشتر. می توانید آن را از
سنگ گچ حاوی حداقل 96% CaSO4*2H2O (یعنی ناخالصی بیش از 4٪)در هاضم ها در زمان چرخه معین و دمای معین . کیفیت آن از گچ ساختمانی بالاتر است. درست مانند گچ ساختمانی از تغییرات β CaSO4* 0.5H2O ( β-هی هیدرات) و با داده های زیر مشخص می شود:
ظرافت آسیاب با باقیمانده روی الک شماره 02 که بیشتر از 2.5٪ نیست مشخص می شود.
شروع تنظیم زودتر از 5 دقیقه نیست.
پایان تنظیم حداکثر 25 دقیقه است.
استحکام کششی بعد از 1 روز کمتر از 1.4 مگاپاسکال نیست و پس از 7 روز - کمتر از 2.5 مگاپاسکال نیست. (از نظر ضخامت سنگ زنی کوچکتر، افزایش استحکام و عدم وجود ناخالصی با گچ ساختمانی متفاوت است).
گچ قالب گیری برای ساخت قالب ها، مدل ها و محصولات در سرامیک های ساختمانی، مهندسی مکانیک و سایر صنایع استفاده می شود. محصولات ساخته شده از سفال چینی و توده سرامیکی در قالب های ساخته شده از گچ قالب گیری ریخته می شوند. قالب گچی باید به اندازه کافی قوی و در عین حال متخلخل باشد تا آب را بدون فرو ریختن از لغزش خارج کند.
گچ با مقاومت بالابا عملیات حرارتی سنگ گچ با عیار بالا در دستگاه مهر و موم شده تحت فشار 0.2 تا 0.3 مگاپاسکال در 124 0Сدر عرض 5 ساعت
متشکل از α-اصلاحات CaSO4*0.5H2O. قدرت آن به 15-40 مگاپاسکال می رسد. گچ با مقاومت بالا در مقادیر کم تولید می شود و در صنایع متالورژی برای ساخت قالب استفاده می شود.
سیمان انیدریتعمدتا از انیدریت CaSO4 ("مرده سوخته") تشکیل شده است. با افزودن کاتالیزورهایی که حلالیت آن را افزایش می دهد و شرایطی را برای هیدراتاسیون آن ایجاد می کند، "احیا" می شود. چنین کاتالیزورهایی عبارتند از CaO - 3...5٪ و غیره. سیمان انیدریت برای تهیه ملات سنگ تراشی و گچ، بتن، تولید مواد عایق حرارتی، سنگ مرمر مصنوعی و سایر محصولات تزئینی استفاده می شود.
استریش-گچ(گچ با سوزش زیاد) در دمای 800...1000 درجه سانتیگراد تشکیل می شود، از انیدریت CaSO4 و CaO (3..5٪) تشکیل شده است که در طی تجزیه CaSO4 تشکیل شده است. CaSO4→CaO+-SO3) و اجرا کرد
نقش یک کاتالیزور سخت کننده را بازی می کند. این عنصر به آرامی گیر می کند و سخت می شود.
گچ با پخت زیاد نوعی سیمان انیدریتی است. برای ملات های بنایی و گچ کاری، نصب کفپوش های موزاییکی و ... استفاده می شود.محصولات ساخته شده از این گچ در مقایسه با گچ ساختمانی در برابر یخ زدگی مقاوم تر، مقاومت در برابر آب افزایش یافته و کمتر در معرض تغییر شکل پلاستیک هستند.
کاربرد گچ
گچ ساختمانی – چسب سفید، سازگار با محیط زیست، با چسبندگی سریع و سخت شدن سریع.برای ساخت قطعات و محصولات ساختمانی، برای کف های خود تراز، ترکیبات چسب، قالب گیری، تولید قالببرای ریخته گری سرامیک های هنری و همچنین برای گچ کاری. گچ ضد آب نیست و برای کارهای خارجی مناسب نیست.، اما با افزودن سیمان، ضد آب می شود. گچ به طور گسترده در پزشکی استفاده می شود. پانل ها و پارتیشن های گچی صدا را به خوبی جذب می کنند. گچ در برابر آتش مقاوم است و گرما را به خوبی حفظ می کند. علاوه بر گچ ساختمانی از چسباننده های گچی دیگر (به مقدار محدود) استفاده می شود: گچ قالبی، گچ با مقاومت بالا.
نیاز آبی بایندرهای گچی
تقاضای آبچسب گچ با مقدار آب (به عنوان درصدی از جرم چسب) مورد نیاز برای به دست آوردن خمیر گچی با قوام استاندارد تعیین می شود.
از نظر تئوری، هیدراتاسیون گچ نیمه آبی نیاز دارد 18,6% آب از توده چسب گچ در عمل برای به دست آوردن مخلوط پلاستیکی قابل قالب گیری، گچ ساختمانی نیاز دارد 50...70 درصد آب، و با استحکام بالا - 30...40%. آب اضافی تبخیر می شود و منافذ ایجاد می کند، به همین دلیل است که محصولات گچ تخلخل بالایی دارند.