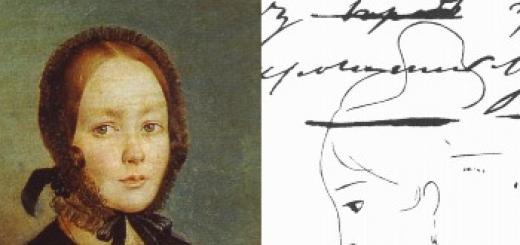ኦክስጅን ወደ ውስጥ ታየ የምድር ከባቢ አየርአረንጓዴ ተክሎች እና የፎቶሲንተቲክ ባክቴሪያዎች ብቅ ብቅ ማለት. ለኦክሲጅን ምስጋና ይግባውና ኤሮቢክ ፍጥረታት አተነፋፈስ ወይም ኦክሳይድ ያካሂዳሉ. በኢንዱስትሪ ውስጥ ኦክሲጅን ማግኘት አስፈላጊ ነው - በብረታ ብረት, በመድሃኒት, በአቪዬሽን, ብሔራዊ ኢኮኖሚእና ሌሎች ኢንዱስትሪዎች.
ንብረቶች
ኦክስጅን - ስምንተኛው አካል ወቅታዊ ሰንጠረዥሜንዴሌቭ. ማቃጠልን የሚደግፍ እና ንጥረ ነገሮችን የሚያመነጭ ጋዝ ነው.

ሩዝ. 1. ኦክስጅን በጊዜ ሰንጠረዥ.
ኦክስጅን በ1774 በይፋ ተገኘ። እንግሊዛዊው ኬሚስት ጆሴፍ ፕሪስትሊ ኤለመንቱን ከሜርኩሪክ ኦክሳይድ ለይቷል፡-
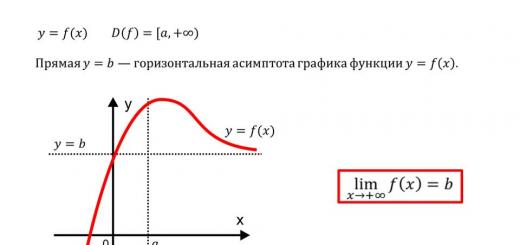
2HgO → 2Hg + O 2
ይሁን እንጂ ፕሪስትሊ ኦክስጅን የአየር ክፍል መሆኑን አያውቅም ነበር. በከባቢ አየር ውስጥ ያለው የኦክስጅን ባህሪያት እና መገኘት ከጊዜ በኋላ በፕሪስትሊ የሥራ ባልደረባው በፈረንሣይ ኬሚስት አንትዋን ላቮሲየር ተወስኗል.
የኦክስጅን አጠቃላይ ባህሪያት:
- ቀለም የሌለው ጋዝ;
- ምንም ሽታ ወይም ጣዕም የለውም;
- ከአየር የበለጠ ከባድ;
- ሞለኪውሉ ሁለት የኦክስጂን አተሞች (ኦ 2) ያካትታል.
- በፈሳሽ ሁኔታ ውስጥ ፈዛዛ ሰማያዊ ቀለም አለው;
- በውሃ ውስጥ በደንብ የማይሟሟ;
- ኃይለኛ ኦክሳይድ ወኪል ነው.

ሩዝ. 2. ፈሳሽ ኦክሲጅን.
ጋዝ በያዘ ዕቃ ውስጥ የሚቃጠለውን ስፖንሰር በማውረድ የኦክስጅን መኖር በቀላሉ ማረጋገጥ ይቻላል። ኦክሲጅን በሚኖርበት ጊዜ ችቦው በእሳት ነበልባል ውስጥ ይወጣል.
እንዴት ነው የሚያገኙት?
በኢንዱስትሪ ውስጥ እና ከተለያዩ ውህዶች ኦክስጅንን ለማምረት በርካታ የታወቁ ዘዴዎች አሉ። የላብራቶሪ ሁኔታዎች. በኢንዱስትሪ ውስጥ ኦክስጅን በአየር ግፊት እና በ -183 ዲግሪ ሴንቲ ግሬድ የሙቀት መጠን በማፍሰስ ይገኛል. ፈሳሽ አየር ለትነት ይጋለጣል, ማለትም. ቀስ በቀስ ማሞቅ. በ -196 ° ሴ ናይትሮጅን መትነን ይጀምራል, እና ኦክስጅን ፈሳሽ ሆኖ ይቆያል.
በቤተ ሙከራ ውስጥ ኦክሲጅን ከጨው, ሃይድሮጂን ፓርሞክሳይድ እና በኤሌክትሮላይዜስ ምክንያት ይፈጠራል. የጨው መበስበስ በሚሞቅበት ጊዜ ይከሰታል. ለምሳሌ የፖታስየም ክሎሬት ወይም ቤርቶላይት ጨው እስከ 500 ° ሴ ይሞቃል፣ እና ፖታስየም ፐርማንጋኔት ወይም ፖታስየም ፐርማንጋኔት እስከ 240 ° ሴ ይሞቃል።
- 2KClO 3 → 2KCl + 3O 2;
- 2KMnO 4 → K 2 MnO 4 + MnO 2 + O 2

ሩዝ. 3. ቤርቶሌት ጨው ማሞቅ.
ናይትሬትን ወይም ፖታስየም ናይትሬትን በማሞቅ ኦክሲጅን ማግኘት ይችላሉ፡-
2KNO 3 → 2KNO 2 + O 2
ሃይድሮጅን በፔርኦክሳይድ ሲበሰብስ ማንጋኒዝ (IV) ኦክሳይድ - MnO 2, የካርቦን ወይም የብረት ዱቄት እንደ ማነቃቂያ ጥቅም ላይ ይውላል. አጠቃላይ እኩልታእንደሚከተለው:
2H 2 O 2 → 2H 2 O + O 2።
የሶዲየም ሃይድሮክሳይድ መፍትሄ በኤሌክትሮላይዜሽን ውስጥ ይከናወናል. በውጤቱም, ውሃ እና ኦክስጅን ይፈጠራሉ.
4ናኦህ → (ኤሌክትሮሊሲስ) 4ና + 2ኤች 2 ኦ + ኦ 2 .
ኦክስጅን እንዲሁ ኤሌክትሮይዚስ በመጠቀም ከውሃ ተለይቷል ፣ ወደ ሃይድሮጂን እና ኦክሲጅን ይሰበሰባል።
2H 2 O → 2H 2 + O 2።
በኑክሌር ሰርጓጅ መርከቦች ላይ ኦክስጅን ከሶዲየም ፐሮክሳይድ - 2Na 2 O 2 + 2CO 2 → 2Na 2 CO 3 + O 2 ተገኝቷል። ዘዴው የሚስብ ነው, ከኦክስጅን መለቀቅ ጋር, ካርቦን ዳይኦክሳይድ ወደ ውስጥ ይገባል.
እንዴት መጠቀም እንደሚቻል
መሰብሰብ እና እውቅና መስጠት አስፈላጊ ነው ንፁህ ኦክስጅንን ለመልቀቅ, በኢንዱስትሪ ውስጥ ንጥረ ነገሮችን ለኦክሳይድ, እንዲሁም በጠፈር ውስጥ, በውሃ ውስጥ እና በጢስ ክፍሎች ውስጥ መተንፈስን ለመጠበቅ (ኦክስጅን ለእሳት አደጋ መከላከያ አስፈላጊ ነው). በመድኃኒት ውስጥ የኦክስጂን ሲሊንደሮች የመተንፈስ ችግር ያለባቸው ታካሚዎች ለመተንፈስ ይረዳሉ. በተጨማሪም ኦክስጅን የመተንፈሻ አካላት በሽታዎችን ለማከም ያገለግላል.
ኦክስጅን ነዳጅ ለማቃጠል ያገለግላል - የድንጋይ ከሰል, ዘይት, የተፈጥሮ ጋዝ. ኦክስጅን በብረታ ብረት እና ሜካኒካል ምህንድስና ውስጥ በስፋት ጥቅም ላይ ይውላል, ለምሳሌ, ለማቅለጥ, ለመቁረጥ እና ለመገጣጠም ብረት.
አማካኝ ደረጃ 4.9. አጠቃላይ የተሰጡ ደረጃዎች፡ 220
አየር የማይጠፋ የኦክስጂን ምንጭ ነው። ከእሱ ኦክስጅን ለማግኘት, ይህ ጋዝ ከናይትሮጅን እና ከሌሎች ጋዞች መለየት አለበት. ኦክስጅንን ለማምረት የኢንዱስትሪው ዘዴ በዚህ ሀሳብ ላይ የተመሰረተ ነው. ልዩ, ይልቁንም አስቸጋሪ መሳሪያዎችን በመጠቀም ነው የሚተገበረው. በመጀመሪያ አየሩ ወደ ፈሳሽነት እስኪቀየር ድረስ በጣም ይቀዘቅዛል. ከዚያም ፈሳሽ የአየር ሙቀት ቀስ በቀስ ይጨምራል. ናይትሮጅን ጋዝ በመጀመሪያ ከእሱ መለቀቅ ይጀምራል (ፈሳሽ ናይትሮጅን የሚፈላበት ነጥብ -196 ° ሴ ነው), እና ፈሳሹ በኦክስጅን የበለፀገ ነው.
በቤተ ሙከራ ውስጥ ኦክሲጅን ማግኘት. ኦክሲጅን ለማምረት የላቦራቶሪ ዘዴዎች በኬሚካላዊ ግብረመልሶች ላይ የተመሰረቱ ናቸው.
ጄ. ፕሪስትሊ ይህንን ጋዝ ያገኘው ሜርኩሪ (II) ኦክሳይድ ከሚባል ውህድ ነው። ሳይንቲስቱ የፀሐይ ብርሃንን በእቃው ላይ ያተኮረበትን የመስታወት መነፅር ተጠቅሟል።
በዘመናዊ ስሪት ይህ ሙከራ በስእል 54 ይታያል. ሲሞቅ ሜርኩሪ (||) ኦክሳይድ (ዱቄት) ቢጫ ቀለም) ወደ ሜርኩሪ እና ኦክስጅን ይቀየራል. ሜርኩሪ ወደ ውስጥ ይለቀቃል የጋዝ ሁኔታእና በብር ጠብታዎች መልክ የሙከራ ቱቦው ግድግዳዎች ላይ ይጨመቃል. በሁለተኛው የሙከራ ቱቦ ውስጥ ኦክስጅን ከውኃው በላይ ይሰበሰባል.
የፕሪስትሊ ዘዴ ከአሁን በኋላ ጥቅም ላይ አይውልም ምክንያቱም የሜርኩሪ ትነት መርዛማ ነው. ኦክስጅን የሚመረተው ከተነጋገርነው ጋር ተመሳሳይ የሆኑ ሌሎች ግብረመልሶችን በመጠቀም ነው። ብዙውን ጊዜ ሲሞቁ ይከሰታሉ.
ብዙ ሌሎች ከአንድ ንጥረ ነገር የተፈጠሩባቸው ምላሾች የመበስበስ ምላሽ ይባላሉ።
በቤተ ሙከራ ውስጥ ኦክስጅንን ለማግኘት የሚከተሉት ኦክስጅንን የያዙ ውህዶች ጥቅም ላይ ይውላሉ።
ፖታስየም permanganate KMnO4 (የተለመደው የፖታስየም ፐርማንጋኔት ስም፤ ቁስ ነገሩ የተለመደ ፀረ-ተባይ ነው)
ፖታስየም ክሎራይድ KClO3 (ትንሽ ስም - የቤርቶሌት ጨው ፣ ለፈረንሣይ ኬሚስት ክብር። ዘግይቶ XVIII - መጀመሪያ XIXቪ. ኬ.-ኤል. በርቶሌት)
![]()
አነስተኛ መጠን ያለው ማነቃቂያ - ማንጋኒዝ (IV) ኦክሳይድ MnO2 - ወደ ፖታስየም ክሎሬት ተጨምሯል ስለዚህም የግቢው መበስበስ በኦክሲጅን መውጣቱ ይከሰታል.
የ chalcogen hydrides H2E ሞለኪውሎች አወቃቀርየሞለኪውላር ምህዋር (MO) ዘዴን በመጠቀም መተንተን ይቻላል. እንደ ምሳሌ፣ የውሃ ሞለኪውል ሞለኪውላዊ ምህዋርን ንድፍ ተመልከት (ምስል 3)
ለግንባታ (ለበለጠ ዝርዝር መረጃ G. Gray "Electrons and Chemical Bonding")፣ ኤም. ማተሚያ ቤት "ሚር"፣ 1967፣ ገጽ 155-62 እና ጂ.ኤል. ሚሴየር፣ ዲ.ኤ. ታረር፣ "ኢንኦርጋኒክ ኬሚስትሪ"፣ ፕራንቲስ ሆል ኢንት. Inc ., 1991, p.153-57) የ H2O ሞለኪውል MO ንድፎችን, እኛ መጋጠሚያዎች አመጣጥ ከኦክስጅን አቶም ጋር በማጣመር, እና xz አውሮፕላን ውስጥ ሃይድሮጂን አቶሞች ማስቀመጥ (የበለስ. 3). የ2s- እና 2p-AO ኦክስጅን ከ1s-AO ሃይድሮጂን ጋር መደራረብ በስእል 4 ይታያል። ተመሳሳይ ሲምሜትሪ እና ተመሳሳይ ሃይሎች ያላቸው የሃይድሮጅን እና ኦክሲጅን ኦክሲጅን በ MOs ምስረታ ላይ ይሳተፋሉ። ሆኖም ፣ የ AO ረቂቅ ተሕዋስያን እንዲፈጠሩ ያበረከቱት አስተዋጽኦ የተለየ ነው ፣ ይህም በተዛማጅ ውስጥ በተለያዩ የቁጥር እሴቶች ውስጥ ይንጸባረቃል። መስመራዊ ጥምሮችጄ.ኤስ.ሲ. የ 1s-AO የሃይድሮጅን እና 2s- እና 2pz-AO የኦክስጅን መስተጋብር (መደራረብ) 2a1-bonding እና 4a1-antibonding MOs እንዲፈጠር ያደርጋል።
አራት “ካልኮጅን” ንጥረ ነገሮች (ማለትም፣ “መዳብ መውለድ”) የቡድን VI ዋና ንዑስ ቡድን ይመራሉ (በአዲሱ ምደባ - 16 ኛው ቡድን) ወቅታዊ ሰንጠረዥ. ከሰልፈር፣ ቴልዩሪየም እና ሴሊኒየም በተጨማሪ ኦክስጅንን ይጨምራሉ። በምድር ላይ በጣም የተለመደውን የዚህን ንጥረ ነገር ባህሪያት, እንዲሁም የኦክስጅንን አጠቃቀም እና ምርትን ጠለቅ ብለን እንመርምር.
የንጥረ ነገሮች ስርጭት
በታሰረ ቅርጽ, ኦክስጅን ወደ ውስጥ ይገባል የኬሚካል ስብጥርውሃ - መቶኛ 89% ገደማ ነው, እንዲሁም በሁሉም ህይወት ያላቸው ፍጥረታት ሕዋሳት - ተክሎች እና እንስሳት ስብጥር ውስጥ.
በአየር ውስጥ, ኦክስጅን O2 መልክ, በውስጡ ጥንቅር አምስተኛ የሚይዝ, እና የኦዞን መልክ - O3 ውስጥ ነጻ ሁኔታ ውስጥ ነው.
ኦክስጅን ኦ2 ቀለም የሌለው፣ ጣዕም የሌለው እና ሽታ የሌለው ጋዝ ነው። በውሃ ውስጥ በትንሹ የሚሟሟ. የማብሰያው ነጥብ 183 ዲግሪ ከዜሮ ሴልሺየስ በታች ነው. በፈሳሽ መልክ, ኦክሲጅን ሰማያዊ ቀለም አለው, እና በጠንካራ መልክ ይሠራል ሰማያዊ ክሪስታሎች. የኦክስጅን ክሪስታሎች የማቅለጫ ነጥብ 218.7 ዲግሪ ከዜሮ ሴልሺየስ በታች ነው።
ሲሞቅ, ይህ ንጥረ ነገር ከብዙዎች ጋር ምላሽ ይሰጣል ቀላል ንጥረ ነገሮች, ሁለቱም ብረቶች እና ብረቶች ያልሆኑ, ኦክሳይዶች የሚባሉትን - የንጥረ ነገሮች ውህዶች ከኦክስጅን ጋር. ከኦክሲጅን ጋር የሚገቡት ንጥረ ነገሮች ኦክሳይድ ይባላል.
ለምሳሌ,
4ና + O2= 2Na2O
2. በማንጋኒዝ ኦክሳይድ ውስጥ በሚሞቅበት ጊዜ በሃይድሮጂን ፓርሞክሳይድ መበስበስ በኩል, እሱም እንደ ማነቃቂያ ይሠራል.
3. በፖታስየም permanganate መበስበስ በኩል.
በኢንዱስትሪ ውስጥ ኦክስጅን በሚከተሉት መንገዶች ይመረታል.
1. ለቴክኒካዊ ዓላማዎች, ኦክስጅን ከአየር የተገኘ ሲሆን በውስጡም የተለመደው ይዘቱ 20% ገደማ ነው, ማለትም. አምስተኛው ክፍል. ይህንን ለማድረግ በመጀመሪያ አየሩ ይቃጠላል, ወደ 54% ገደማ ፈሳሽ ኦክሲጅን, 44% ፈሳሽ ናይትሮጅን እና 2% ፈሳሽ አርጎን የያዘ ድብልቅ ይሠራል. እነዚህ ጋዞች ከዚያም ፈሳሽ ኦክስጅን እና ፈሳሽ ናይትሮጅን ያለውን መፍላት ነጥቦች መካከል በአንጻራዊ ሁኔታ አነስተኛ ክልል በመጠቀም distillation ሂደት በመጠቀም ተለያይተዋል - ሲቀነስ 183 እና 198,5 ዲግሪ, በቅደም. ናይትሮጅን ከኦክሲጅን ቀድመው ይተናል.
ዘመናዊ መሳሪያዎች በማንኛውም የንጽህና ደረጃ ኦክስጅንን ማምረት ያረጋግጣል. በመለየት ጊዜ የሚገኘው ናይትሮጅን በምርቶቹ ውህደት ውስጥ እንደ ጥሬ ዕቃ ይጠቀማል.
2. በተጨማሪም በጣም ንጹህ ኦክሲጅን ያመነጫል. ይህ ዘዴ የበለጸጉ ሀብቶች እና ርካሽ የኤሌክትሪክ ኃይል ባለባቸው አገሮች ውስጥ ተስፋፍቷል.
የኦክስጅን አተገባበር
ኦክስጅን በፕላኔታችን ሕይወት ውስጥ በጣም አስፈላጊው አካል ነው። በከባቢ አየር ውስጥ ያለው ይህ ጋዝ በሂደቱ ውስጥ በእንስሳትና በሰዎች ይበላል.
ኦክስጅን ማግኘት ለሰው ልጅ እንቅስቃሴ እንደ መድሃኒት፣ ብየዳ እና ብረት መቁረጥ፣ ፍንዳታ፣ አቪዬሽን (ለሰው መተንፈስ እና ለሞተር ኦፕሬሽን) እና ለብረታ ብረት ስራዎች በጣም አስፈላጊ ነው።
በሂደት ላይ የኢኮኖሚ እንቅስቃሴበሰዎች ውስጥ ኦክሲጅን በብዛት ይበላል - ለምሳሌ የተለያዩ የነዳጅ ዓይነቶችን ሲያቃጥሉ: የተፈጥሮ ጋዝ, ሚቴን, የድንጋይ ከሰል, እንጨት. በነዚህ ሁሉ ሂደቶች ውስጥ ይመሰረታል, በተመሳሳይ ጊዜ, ተፈጥሮ በፀሐይ ብርሃን ተጽእኖ በአረንጓዴ ተክሎች ውስጥ የሚከሰተውን ፎቶሲንተሲስ በመጠቀም የዚህን ውህድ ተፈጥሯዊ ትስስር ሂደት አቅርቧል. በዚህ ሂደት ምክንያት ግሉኮስ ይፈጠራል, ከዚያም እፅዋቱ ሕብረ ሕዋሳትን ለመገንባት ይጠቀማል.
የኦክስጅን ግኝት ታሪክ የኦክስጂን ግኝት ምልክት ተደርጎበታል አዲስ ወቅትበኬሚስትሪ እድገት ውስጥ. ማቃጠል አየር እንደሚያስፈልገው ከጥንት ጀምሮ ይታወቃል. የንጥረ ነገሮችን የማቃጠል ሂደት ለረዥም ጊዜ ግልጽ አይደለም. በአልኬሚ ዘመን ፣ የፍሎጂስተን ፅንሰ-ሀሳብ በሰፊው ተስፋፍቷል ፣ በዚህ መሠረት ንጥረ ነገሮች ከእሳት ነበልባል ጋር ባለው ግንኙነት ምክንያት ይቃጠላሉ ፣ ማለትም ፣ በእሳቱ ውስጥ ካለው phlogiston ጋር። ኦክስጅን የተገኘው በእንግሊዛዊው ኬሚስት ጆሴፍ ፕሪስትሊ በ 70 ዎቹ በ 18 ኛው ክፍለ ዘመን ነበር. አንድ ኬሚስት ቀይ ሜርኩሪ(II) ኦክሳይድ ዱቄትን በማሞቅ ንጥረ ነገሩ እንዲበሰብስ በማድረግ ሜታሊክ ሜርኩሪ እና ቀለም የሌለው ጋዝ እንዲፈጠር አድርጓል፡-
2HgO t° → 2Hg + O2
ኦክሳይዶች- ኦክስጅንን የሚያካትቱ ሁለትዮሽ ውህዶች ጋዝ ወዳለበት ዕቃ ውስጥ የሚጤስ ስፕሊንት ሲገባ ደማቅ ነበልባል።ሳይንቲስቱ የሚጨስበት ስፕሊተር ፍሎጂስተን ወደ ጋዝ ውስጥ እንዳስገባ ያምን ነበር, እና ተቀጣጠለ. ዲ. ፕሪስትሊየተፈጠረውን ጋዝ ለመተንፈስ ሞከርኩ እና ለመተንፈስ ምን ያህል ቀላል እና ነፃ እንደሆነ ተደስቻለሁ። ከዚያም ሳይንቲስቱ ይህን ጋዝ የመተንፈስ ደስታ ለሁሉም ሰው እንደተሰጠ እንኳን አላሰበም. ዲ. ፕሪስትሊ የሙከራ ውጤቱን ለፈረንሳዊው የኬሚስትሪ ሊቅ አንትዋን ሎረንት ላቮሲየር አጋርቷል።በዚያን ጊዜ በደንብ የታገዘ ላቦራቶሪ ያለው፣ ኤ. ላቮይሲየር የዲ ፕሪስትሊ ሙከራዎችን ደጋግሞ አሻሽሏል። A. Lavoisier የተወሰነ የሜርኩሪ ኦክሳይድ ብስባሽ በሚፈጠርበት ጊዜ የሚወጣውን ጋዝ መጠን ለካ።ከዚያም ኬሚስቱ ሜርኩሪ (II) ኦክሳይድ እስኪሆን ድረስ ብረታማ ሜርኩሪን በታሸገ ዕቃ ውስጥ አሞቀው። በመጀመሪያው ሙከራ ውስጥ የተለቀቀው የጋዝ መጠን በሁለተኛው ሙከራ ውስጥ ከተቀላቀለው ጋዝ ጋር እኩል መሆኑን ተገንዝቧል. ስለዚህ, ሜርኩሪ በአየር ውስጥ ካለው አንዳንድ ንጥረ ነገር ጋር ምላሽ ይሰጣል. እና ይህ ተመሳሳይ ንጥረ ነገር በኦክሳይድ መበስበስ ወቅት ይለቀቃል. ላቮይሲየር ፍሎጂስተን ከሱ ጋር ምንም ግንኙነት እንደሌለው ለመደምደም የመጀመሪያው ነበር, እና የሚጤስ ስፕሊን ማቃጠል ምክንያቱ ባልታወቀ ጋዝ ነው, እሱም ከጊዜ በኋላ ኦክስጅን ይባላል. የኦክስጂን ግኝት የፍሎጂስተን ቲዎሪ ውድቀትን ያመለክታል!በቤተ ሙከራ ውስጥ ኦክስጅንን ለማምረት እና ለመሰብሰብ ዘዴዎች
ኦክሲጅን ለማምረት የላቦራቶሪ ዘዴዎች በጣም የተለያዩ ናቸው. ኦክስጅንን ማግኘት የሚቻልባቸው ብዙ ንጥረ ነገሮች አሉ. በጣም የተለመዱ ዘዴዎችን እንመልከት.1) የሜርኩሪ (II) ኦክሳይድ መበስበስ
በላብራቶሪ ውስጥ ኦክሲጅን ለማግኘት ከሚችሉት መንገዶች አንዱ ከላይ የተገለጸውን የኦክሳይድ መበስበስ ምላሽ በመጠቀም ማግኘት ነው። ሜርኩሪ (II).የሜርኩሪ ውህዶች እና የሜርኩሪ ትነት በራሱ ከፍተኛ መርዛማነት ምክንያት ይህ ዘዴ በጣም አልፎ አልፎ ጥቅም ላይ ይውላል.2) የፖታስየም permanganate መበስበስ
ፖታስየም permanganate(በዕለት ተዕለት ሕይወት ውስጥ ፖታስየም permanganate ብለን እንጠራዋለን) - ክሪስታል ንጥረ ነገርጥቁር ሐምራዊ ቀለም. ፖታስየም permanganate ሲሞቅ ኦክስጅን ይለቀቃል. አንዳንድ የፖታስየም ፐርጋናንትን ዱቄት ወደ የሙከራ ቱቦ ውስጥ አፍስሱ እና በሦስት እግር ውስጥ በአግድም ያስተካክሉት. በሙከራ ቱቦው ቀዳዳ አጠገብ አንድ የጥጥ ሱፍ ያስቀምጡ. የሙከራ ቱቦውን የጋዝ መውጫ ቱቦ በሚያስገባበት ማቆሚያ እንዘጋዋለን, ጫፉም ወደ መቀበያው እቃ ውስጥ ይወርዳል. የጋዝ መውጫ ቱቦው ወደ መቀበያው የታችኛው ክፍል መድረስ አለበት. የፖታስየም permanganate ቅንጣቶች ወደ መቀበያው ዕቃ ውስጥ እንዳይገቡ ለመከላከል የሙከራ ቱቦው መክፈቻ አጠገብ የሚገኝ የጥጥ ሱፍ ያስፈልጋል (በመበስበስ ወቅት የተለቀቀው ኦክስጅን የፐርማንጋኔትን ቅንጣቶች ይይዛል)። መሳሪያው በሚሰበሰብበት ጊዜ የሙከራ ቱቦውን ማሞቅ እንጀምራለን. የኦክስጅን መለቀቅ ይጀምራል. የፖታስየም permanganate መበስበስ ምላሽ እኩልታ፡-2KMnO4 t° → K2MnO4 + MnO2 + O2
የኦክስጅንን መኖር እንዴት ማወቅ ይቻላል? የፕሪስትሊ ዘዴን እንጠቀም። የእንጨት መሰንጠቂያውን እናበራው ፣ ትንሽ እንዲቃጠል እናድርገው ፣ ከዚያ እስኪጨስ ድረስ እናጥፋው። የጭስ ማውጫውን ኦክሲጅን ወዳለበት ዕቃ ውስጥ እናስቀምጠው። ችቦው በደመቀ ሁኔታ ያበራል! የጋዝ መውጫ ቱቦበድንገት ወደ መቀበያው የታችኛው ክፍል አልወረደም. ኦክስጅን ከአየር የበለጠ ከባድ ነው, ስለዚህ, በተቀባዩ ግርጌ ይሰበስባል, አየሩን ከእሱ ያፈላልጋል. ውሃን በማፈናቀል ኦክስጅንን መሰብሰብም ይቻላል. ይህንን ለማድረግ የጋዝ መውጫ ቱቦው በውሃ በተሞላ የሙከራ ቱቦ ውስጥ መውረድ እና ጉድጓዱ ወደታች ባለው ውሃ ወደ ክሪስታላይዘር ዝቅ ማድረግ አለበት። ኦክስጅን ወደ ውስጥ ሲገባ, ጋዝ ከመሞከሪያ ቱቦ ውስጥ ውሃን ያፈላልጋል.
የሃይድሮጅን ፔርኦክሳይድ መበስበስ
ሃይድሮጅን ፐርኦክሳይድ- ለሁሉም ሰው የሚታወቅ ንጥረ ነገር. በፋርማሲዎች ውስጥ "ሃይድሮጅን ፔርኦክሳይድ" በሚለው ስም ይሸጣል. ይህ ስም ጊዜው አልፎበታል፤ “ፐርኦክሳይድ” የሚለውን ቃል መጠቀም የበለጠ ትክክል ነው። የኬሚካል ቀመርሃይድሮጅን ፐርኦክሳይድ H2O2 ሃይድሮጅን በፔርኦክሳይድ በማከማቻ ጊዜ ቀስ በቀስ ወደ ውሃ እና ኦክሲጅን ይበሰብሳል. የመበስበስ ሂደቱን ለማፋጠን, ማሞቅ ወይም ማመልከት ይችላሉ ቀስቃሽ.ካታሊስት- የኬሚካላዊ ምላሽ ፍጥነትን የሚያፋጥን ንጥረ ነገር
ሃይድሮጅን በፔርኦክሳይድ ወደ ማሰሮው ውስጥ አፍስሱ እና ፈሳሹን ፈሳሽ ይጨምሩ። ማነቃቂያው ጥቁር ዱቄት - ማንጋኒዝ ኦክሳይድ ሊሆን ይችላል MnO2.ወዲያውኑ ድብልቅው በመለቀቁ ምክንያት አረፋ ይጀምራል ከፍተኛ መጠንኦክስጅን. የሚጤስ ስንጥቅ ወደ ብልቃጥ ውስጥ እናምጣ - በደመቀ ሁኔታ ያበራል። የሃይድሮጅን ፔርኦክሳይድ መበስበስ የምላሽ እኩልታ የሚከተለው ነው-
2H2O2 MnO2 → 2H2O + O2
እባክዎን ያስተውሉ፡ ምላሹን የሚያፋጥነው ቀስት ወይም ምልክት በላይ ተጽፏል «=», ምክንያቱም በምላሹ ጊዜ አይበላም, ነገር ግን ያፋጥነዋል.
የፖታስየም ክሎሬት መበስበስ
ፖታስየም ክሎሬት- ክሪስታል ንጥረ ነገር ነጭ. ርችቶችን እና ሌሎች የተለያዩ የፒሮቴክኒክ ምርቶችን ለማምረት ያገለግላል. ለዚህ ንጥረ ነገር ትንሽ ስም አለ - "Berthollet ጨው". ንጥረ ነገሩ ይህን ስም የተቀበለው ለመጀመሪያ ጊዜ የተዋቀረው ፈረንሳዊው ኬሚስት ክሎድ ሉዊ በርቶሌት ነው። የፖታስየም ክሎሬት ኬሚካላዊ ቀመር KСlO3 ነው.የፖታስየም ክሎራይድ በአነቃቂ ሁኔታ ሲሞቅ - ማንጋኒዝ ኦክሳይድ MnO2, በርቶሌት ጨው በሚከተለው እቅድ መሰረት ይበሰብሳል.2KClO3 t°፣ MnO2 → 2KCl + 3O2።
የናይትሬት መበስበስ
ናይትሬትስ- ions የያዙ ንጥረ ነገሮች ቁጥር 3⎺ግንኙነቶች የዚህ ክፍልእንደ ማዕድን ማዳበሪያዎች ጥቅም ላይ የዋለ እና በፒሮቴክኒክ ምርቶች ውስጥ ተካትቷል. ናይትሬትስ- ውህዶቹ በሙቀት ያልተረጋጉ ናቸው፣ እና ሲሞቁ ኦክስጅን ሲለቁ ይበሰብሳሉ፡- ሁሉም ኦክሲጅን ለማምረት የታሰቡት ዘዴዎች ተመሳሳይ መሆናቸውን ልብ ይበሉ። በሁሉም ሁኔታዎች, ይበልጥ ውስብስብ የሆኑ ንጥረ ነገሮች በሚበሰብስበት ጊዜ ኦክስጅን ይለቀቃል. የመበስበስ ምላሽ- የሚያስከትል ምላሽ ውስብስብ ንጥረ ነገሮችወደ ቀላል ቢ መበስበስ አጠቃላይ እይታየመበስበስ ምላሽ በደብዳቤ ንድፍ ሊገለጽ ይችላል-AB → A + B
በተለያዩ ምክንያቶች ተጽእኖ ስር የመበስበስ ምላሾች ሊከሰቱ ይችላሉ. ይህ ማሞቂያ, እርምጃ ሊሆን ይችላል የኤሌክትሪክ ፍሰት, ማነቃቂያ አጠቃቀም. ንጥረ ነገሮች በድንገት የሚበሰብሱባቸው ምላሾች አሉ።
በኢንዱስትሪ ውስጥ የኦክስጅን ምርት
በኢንዱስትሪ ውስጥ ኦክስጅን የሚገኘው ከአየር ላይ በመለየት ነው. አየር- የጋዞች ድብልቅ, ዋና ዋናዎቹ ክፍሎች በሰንጠረዥ ውስጥ ቀርበዋል. የዚህ ዘዴ ዋናው ነገር አየሩን በጥልቀት ማቀዝቀዝ, ወደ ፈሳሽነት በመለወጥ, በተለመደው ሁኔታ ውስጥ, የከባቢ አየር ግፊትስለ ሙቀት ሊደረስበት ይችላል -192 ° ሴ. ፈሳሽ ወደ ኦክሲጅን እና ናይትሮጅን መለየት የሚከናወነው በሚፈላ ሙቀታቸው ውስጥ ያለውን ልዩነት በመጠቀም ነው-ቲቢ. O2 = -183 ° ሴ; Bp.N2 = -196 ° ሴ(በተለመደው የከባቢ አየር ግፊት). ወደ gaseous ዙር አንድ ፈሳሽ ቀስ በቀስ በትነት ጋር, ተጨማሪ ያለው ናይትሮጅን ዝቅተኛ የሙቀት መጠንመፍላት, እና እንደ ተለቀቀ, ፈሳሹ በኦክስጅን የበለፀገ ይሆናል. ይህንን ሂደት ብዙ ጊዜ መድገም አስፈላጊውን ንፅህና ኦክሲጅን እና ናይትሮጅን ለማግኘት ያስችላል. ፈሳሾችን ወደ ክፍላቸው ክፍሎች የመለየት ይህ ዘዴ ይባላል ፈሳሽ አየርን ማስተካከል.- በቤተ ሙከራ ውስጥ ኦክስጅን የሚመነጨው በመበስበስ ምላሽ ነው
- የመበስበስ ምላሽ- በዚህ ምክንያት ውስብስብ ንጥረ ነገሮች ወደ ቀለል ያሉ ተበላሽተዋል
- ኦክስጅን በአየር ማፈናቀል ዘዴ ወይም በውሃ ማፈናቀል ዘዴ ሊሰበሰብ ይችላል
- ኦክሲጅንን ለመለየት፣ የሚጤስ ስፕሊንተር ጥቅም ላይ ይውላል፤ በውስጡም በብሩህ ያበራል።
- ካታሊስት- የሚያፋጥን ንጥረ ነገር ኬሚካላዊ ምላሽ, ነገር ግን በውስጡ አልበላም
ጤና ይስጥልኝ.. ዛሬ ስለ ኦክሲጅን እና እንዴት ማግኘት እንደሚችሉ እነግርዎታለሁ. ለእኔ ጥያቄዎች ካሉዎት በአንቀጹ ውስጥ በአስተያየቶቹ ውስጥ ሊጽፉ እንደሚችሉ ላስታውስዎ ። በኬሚስትሪ ውስጥ ማንኛውንም እርዳታ ከፈለጉ, . እርስዎን ለመርዳት ደስ ይለኛል.
ኦክስጅን በተፈጥሮ ውስጥ ይሰራጫል isotopes 16 O, 17 O, 18 O, በምድር ላይ የሚከተሉት መቶኛ ያላቸው - 99.76%, 0.048%, 0.192%, በቅደም ተከተል.
በነጻ ግዛት ውስጥ ኦክስጅን በ ውስጥ ይገኛል የሶስት መልክ allotropic ማሻሻያዎች : አቶሚክ ኦክስጅን - ኦ ኦ, ዳይኦክሲጅን - ኦ 2 እና ኦዞን - ኦ 3. በተጨማሪም የአቶሚክ ኦክሲጅን በሚከተለው መንገድ ሊገኝ ይችላል.
KClO 3 = KCl + 3O 0
KNO 3 = KNO 2 + O 0
ኦክስጅን ከ 1,400 በላይ የተለያዩ ማዕድናት እና ኦርጋኒክ ጉዳይበከባቢ አየር ውስጥ ይዘቱ 21% በድምጽ ነው. እና የሰው አካል እስከ 65% ኦክስጅን ይይዛል. ኦክስጅን ቀለም የሌለው እና ሽታ የሌለው ጋዝ ነው, በውሃ ውስጥ በትንሹ የሚሟሟ (3 ጥራዞች ኦክሲጅን በ 100 ጥራዞች በ 20 o C ውስጥ ይቀልጣሉ).
በቤተ ሙከራ ውስጥ ኦክስጅን የሚገኘው የተወሰኑ ንጥረ ነገሮችን በመጠኑ በማሞቅ ነው።
1) የማንጋኒዝ ውህዶች (+7) እና (+4) በሚበሰብሱበት ጊዜ፡-
2KMnO 4 → K 2 MnO 4 + MnO 2 + O 2
permanganate ማንጋኔት
ፖታስየም ፖታስየም
2MnO 2 → 2MnO + O 2
2) Perchlorates በሚበሰብሱበት ጊዜ;
2KClO 4 → KClO 2 + KCl + 3O 2
perchlorate
ፖታስየም
3) የበርቶሌት ጨው (ፖታስየም ክሎራይድ) በሚበሰብስበት ጊዜ..
በዚህ ሁኔታ አቶሚክ ኦክስጅን ይፈጠራል-
2KClO 3 → 2 KCl + 6O 0
ክሎሬት
ፖታስየም
4) በብርሃን ውስጥ hypochlorous acid ጨዎችን በመበስበስ ወቅት- hypochlorites;
2NaClO → 2NaCl + O 2
Ca(ClO) 2 → CaCl 2 + O 2
5) ናይትሬትስ ሲሞቅ.
በዚህ ሁኔታ, አቶሚክ ኦክስጅን ይፈጠራል. በእንቅስቃሴው ተከታታይ ውስጥ ባለው የናይትሬት ብረት አቀማመጥ ላይ በመመስረት የተለያዩ የምላሽ ምርቶች ይፈጠራሉ-
2ናኖ 3 → 2ናኖ 2 + ኦ 2
Ca(NO 3) 2 → CaO + 2NO 2 + O 2
2AgNO3 → 2Ag + 2NO2 + O2
6) በፔሮክሳይድ መበስበስ ወቅት;
2H 2 O 2 ↔ 2H 2 O + O 2
7) የቦዘኑ ብረቶች ኦክሳይዶችን ሲያሞቁ፡-
2Ag 2 O ↔ 4Ag + O 2
ይህ ሂደት በዕለት ተዕለት ሕይወት ውስጥ ጠቃሚ ነው. እውነታው ግን ከመዳብ ወይም ከብር የተሠሩ ምግቦች, ተፈጥሯዊ የኦክሳይድ ፊልም ሽፋን ያላቸው, ሲሞቁ ንቁ ኦክሲጅን ይፈጥራሉ, ይህም ፀረ-ባክቴሪያ ውጤት ነው. የቦዘኑ ብረቶች ጨዎችን በተለይም ናይትሬትስ መሟሟት ኦክሲጅን እንዲፈጠር ያደርጋል። ለምሳሌ የብር ናይትሬትን የማሟሟት አጠቃላይ ሂደት በደረጃዎች ሊወከል ይችላል፡-
AgNO 3 + H 2 O → AgOH + HNO 3
2AgOH → Ag 2 O + O 2
2Ag 2 O → 4Ag + O 2
ወይም በማጠቃለያ መልክ፡-
4AgNO 3 + 2H 2 O → 4Ag + 4HNO 3 + 7O 2
8) ክሮሚየም ጨዎችን ሲያሞቅ ከፍተኛ ዲግሪኦክሳይድ
4K 2Cr 2 O 7 → 4K 2 Cro 4 + 2Cr 2 O 3 + 3 O 2
bichromate chromate
ፖታስየም ፖታስየም
በኢንዱስትሪ ውስጥ ኦክስጅን ይገኛል-
1) የውሃ ኤሌክትሮሊቲክ መበስበስ;
2H 2 O → 2H 2 + O 2
2) መስተጋብር ካርበን ዳይኦክሳይድከፔሮክሳይድ ጋር;
CO 2 + K 2 O 2 → K 2 CO 3 + O 2
ይህ ዘዴ በገለልተኛ ስርዓቶች ውስጥ የመተንፈስ ችግርን ለመፍታት አስፈላጊ ቴክኒካዊ መፍትሄ ነው-የሰርጓጅ መርከቦች ፣ ማዕድን ማውጫዎች ፣ የጠፈር መንኮራኩሮች።
3) ኦዞን ከሚቀነሱ ወኪሎች ጋር ሲገናኝ፡-
ኦ 3 + 2 ኪጄ + ኤች 2 O → J 2 + 2KOH + O 2
 ልዩ ጠቀሜታ በፎቶሲንተሲስ ሂደት ውስጥ ኦክሲጅን ማምረት ነው.በእጽዋት ውስጥ የሚከሰት. በምድር ላይ ያሉ ሁሉም ህይወት በመሠረቱ በዚህ ሂደት ላይ የተመሰረተ ነው. ፎቶሲንተሲስ ውስብስብ ባለብዙ ደረጃ ሂደት ነው። ብርሃን መጀመሪያውን ይሰጠዋል. ፎቶሲንተሲስ ራሱ ሁለት ደረጃዎችን ያቀፈ ነው-ብርሃን እና ጨለማ። በብርሃን ምዕራፍ ውስጥ ፣ በእጽዋት ቅጠሎች ውስጥ ያለው የክሎሮፊል ቀለም “ብርሃንን የሚስብ” ውስብስብ ተብሎ የሚጠራ ፣ ኤሌክትሮኖችን ከውሃ ይወስዳል እና ወደ ሃይድሮጂን ions እና ኦክስጅን ይከፍላል ።
ልዩ ጠቀሜታ በፎቶሲንተሲስ ሂደት ውስጥ ኦክሲጅን ማምረት ነው.በእጽዋት ውስጥ የሚከሰት. በምድር ላይ ያሉ ሁሉም ህይወት በመሠረቱ በዚህ ሂደት ላይ የተመሰረተ ነው. ፎቶሲንተሲስ ውስብስብ ባለብዙ ደረጃ ሂደት ነው። ብርሃን መጀመሪያውን ይሰጠዋል. ፎቶሲንተሲስ ራሱ ሁለት ደረጃዎችን ያቀፈ ነው-ብርሃን እና ጨለማ። በብርሃን ምዕራፍ ውስጥ ፣ በእጽዋት ቅጠሎች ውስጥ ያለው የክሎሮፊል ቀለም “ብርሃንን የሚስብ” ውስብስብ ተብሎ የሚጠራ ፣ ኤሌክትሮኖችን ከውሃ ይወስዳል እና ወደ ሃይድሮጂን ions እና ኦክስጅን ይከፍላል ።
2H 2 O = 4e + 4H + O 2
የተከማቹ ፕሮቶኖች ለኤቲፒ ውህደት አስተዋጽኦ ያደርጋሉ
ADP + P = ATP
በጨለማው ወቅት, ካርቦን ዳይኦክሳይድ እና ውሃ ወደ ግሉኮስ ይለወጣሉ. እና ኦክስጅን እንደ ተረፈ ምርት ይለቀቃል፡-
6CO 2 + 6H 2 O = C 6 H 12 O 6 + O 2
blog.site፣ ቁሳቁሱን በሙሉ ወይም በከፊል ሲገለብጥ፣ ወደ ዋናው ምንጭ ማገናኛ ያስፈልጋል።